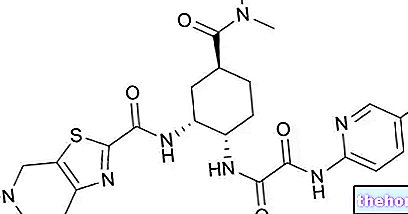
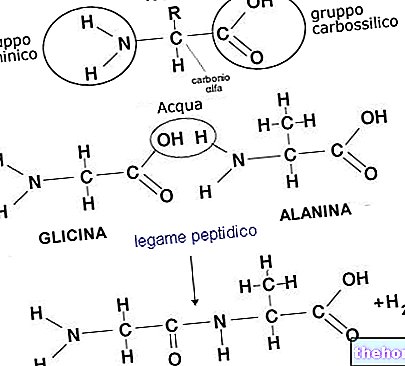
הַגדָרָה
אנזימים הם חלבונים המיוצרים בתאים צמחיים ובעלי חיים, הפועלים כזרזים המאיצים תגובות ביולוגיות מבלי להשתנות.
האנזימים פועלים על ידי שילוב עם חומר ספציפי כדי להפוך אותו לחומר אחר; דוגמאות קלאסיות ניתנות על ידי אנזימי עיכול הקיימים ברוק, בקיבה, בלבלב ובמעי הדק, המבצעים תפקיד חיוני בעיכול ומסייעים בפירוק המזון למרכיבים בסיסיים, שאחר כך יכולים להיספג ולהשתמש בגוף, מעובדים על ידי אנזימים אחרים או מופרש כפסולת.
לכל אנזים יש תפקיד ספציפי: זה שמפרק שומנים, למשל, אינו פועל על חלבונים או פחמימות. אנזימים חיוניים לרווחת האורגניזם החוסר, אפילו באנזים יחיד, יכול לגרום לבעיות חמורות.דוגמה ידועה היא פנילקטונוריה (PKU), מחלה המתאפיינת בחוסר יכולת לחילוף חומצת אמינו חיונית, פנילאלנין, שהצטברותה עלולה לגרום לעיוותים גופניים ומחלות נפש.
מחקר ביוכימי
אנזימים הם חלבונים מסוימים בעלי המאפיין להיות זרזים ביולוגיים, כלומר יש להם את היכולת לפרק את אנרגיית ההפעלה (Eatt) של תגובה, ולשנות את דרכה כך שתהליך איטי מבחינה קינטית יהיה מהיר יותר.
אנזימים מגבירים את הקינטיקה של תגובות תרמודינמיות אפשריות ובניגוד לזרזים, הם פחות או יותר ספציפיים: לכן הם בעלי סגוליות מצע.
האנזים אינו מעורב בסטואיכיומטריה של התגובה: כדי שזה יקרה, האתר הקטליטי הסופי חייב להיות זהה לאתר ההתחלתי.
בפעולה הקטליטי כמעט תמיד יש שלב איטי הקובע את מהירות התהליך.
כשאנחנו מדברים על אנזימים לא נכון לדבר על תגובות שיווי משקל, אנחנו מדברים, במקום זאת על מצב יציב (מצב בו נוצר ונצרך מטבוליט מסוים ברציפות, ושומר על ריכוזו כמעט קבוע לאורך זמן). תוצר של תגובה המזרזת על ידי אנזים אחד הוא בדרך כלל עצמו מגיב לתגובה שלאחר מכן, מזורז על ידי אנזים אחר וכן הלאה.
תהליכים המזרזים על ידי אנזימים מורכבים בדרך כלל מרצפים של תגובות.
ניתן לסכם תגובה גנרית המזרזת על ידי אנזים (E) כדלקמן:

E הוא האנזים
S הוא המצע;
ES מייצג את האדדוק בין האנזים למצע;
P הוא המוצר;
K הוא קבוע הקצב של התגובה.
אנזים (E) משתלב עם המצע (S) ליצירת התוספת (ES) עם קבוע קצב K1; הוא יכול להתנתק בחזרה ל- E + S, עם קבוע קצב K2, או, (אם "חי" מספיק זמן ) יכול להמשיך ליצירת P עם קבוע המהירות K3.
המוצר (P) יכול, בתורו, לשלב מחדש את האנזים ולתקן את האדוקט עם קבוע הקצב K4.
כאשר האנזים והמצע מעורבים, יש שבריר של זמן שבו המפגש בין שני המינים עדיין לא התרחש: כלומר, יש מרווח זמן קצר במיוחד (תלוי בתגובה) שבו יש אנזים ומצע. עדיין לא נפגשו; לאחר תקופה זו, האנזים והמצע באים במגע בכמויות הולכות וגוברות ונוצר תוסף ה- ES. לאחר מכן, האנזים פועל על המצע והמוצר משתחרר. לאחר מכן ניתן לומר כי c "הוא מרווח זמן ראשוני בו לא ניתן להגדיר את ריכוז תוסף ES; לאחר תקופה זו, יש להניח שמצב יציב נקבע, כלומר מהירות התהליכים המובילים להשגת התוספת שווה למהירות התהליכים המובילים להרס התוסף.
קבוע Michaelis-Menten (KM) הוא קבוע שיווי משקל (מתייחס לשיווי המשקל הראשון שתואר לעיל); ניתן לומר, בקירוב טוב (כי יש להתייחס גם ל- K3), כי KM מיוצג על ידי היחס בין הקבועים הקינטיים K2 ו- K1 (הכוונה להרס וליצירת ה- adduct ES בשיווי המשקל הראשון שתואר לעיל) .
דרך קבוע Michaelis-Menten יש לנו "אינדיקציה לזיקה בין אנזים למצע: אם ה- KM קטן c" הוא "זיקה גבוהה בין אנזים למצע, אז תוספת ES יציבה.
האנזימים כפופים לוויסות (או אפנון).
בעבר דיברו בעיקר על אפנון שלילי, כלומר עיכוב היכולות הקטליטיות של אנזים אך יכולה להיות גם אפנון חיובי, כלומר ישנם מינים המסוגלים לשפר את היכולות הקטליטיות של אנזים.
ישנם 4 סוגים של עכבות (המתקבלות מקירובים שנעשו במודל להתאמת נתוני ניסוי למשוואות מתמטיות):
- עיכוב תחרותי
- עיכוב לא תחרותי
- עיכוב בלתי תחרותי
- עיכוב תחרותי
אנו מדברים על עיכוב תחרותי כאשר מולקולה (מעכב) מסוגלת להתחרות במצע. לצורך דמיון מבני, המעכב יכול להגיב במקום המצע, ומכאן המינוח "עיכוב תחרותי". ההסתברות שהאנזים נקשר למעכב או למצע תלויה בריכוז של שניהם ובזיקתם לאנזים; קצב התגובה תלוי אפוא בגורמים אלה.
כדי להשיג את אותה קצב תגובה ללא נוכחותו של המעכב, יש צורך בריכוז מצע גבוה יותר.
הוכח ניסיונית, בנוכחות מעכב, קבוע מיכאליס-מנטן עולה.
באשר למקום זה, "העיכוב הלא תחרותי, האינטראקציה בין המולקולה שצריכה לתפקד כמאפנן (מעכב חיובי או שלילי) לבין" האנזים, מתרחשת באתר השונה מזה שבו האינטראקציה מתרחש. בין אנזים למצע; לכן אנו מדברים על אפנון אלוסטרי (מהיוונית allosteros → אתר אחר).
אם המעכב נקשר לאנזים, הוא יכול לגרום לשינוי במבנה האנזים וכתוצאה מכך יכול להפחית את היעילות שבה המצע נקשר לאנזים.
בתהליך מסוג זה, קבוע מיכאליס-מנטן נשאר קבוע מכיוון שערך זה תלוי בשיווי המשקל בין האנזים למצע ואף בנוכחות מעכב שיווי משקל זה אינו משתנה.
תופעת העיכוב הבלתי תחרותי היא נדירה; מעכב לא תחרותי הוא חומר המתחבר באופן הפיך לתוספת ה- ES המולידה את ה- ESI:

עיכוב מעודף מצע יכול לפעמים להיות בלתי תחרותי, שכן הדבר מתרחש כאשר מולקולת מצע שנייה נקשרת למכלול ה- ES, מה שמוביל למתחם ה- ESS.
מעכב תחרותי, לעומת זאת, יכול להיקשר רק לתוסף האנזים של המצע כמו במקרה הקודם: קישור המצע לאנזים החופשי גורם לשינוי קונפורמטיבי שהופך את האתר לנגיש למעכב.
הקבוע של Michaelis Menten יורד ככל שריכוז המעכב עולה: ככל הנראה, לכן, זיקתו של האנזים למצע עולה.
פרוטאז סרין
הם משפחה של אנזימים שאליהם שיימטוטריפסין וטריפסין שייכים.
כימוטריפסין הוא אנזים פרוטאוליטי והידרוליטי אשר חותך ימינה של חומצות אמינו הידרופוביות וארומטיות.
תוצר הגן המקודד לצ'ימוטריפסין אינו פעיל (הוא מופעל באמצעות פקודה); הצורה הלא פעילה של צ'ימוטריפסין מיוצגת על ידי שרשרת פוליפפטיד של 245 חומצות אמינו. לצ'ימוטריפסין צורה כדורית בשל חמישה גשרים של דיסולפיד ואינטראקציות קטנות אחרות (אלקטרוסטטיות, כוחות ואן דר ואלס, קשרי מימן וכו ').
הכימוטריפסין מיוצר על ידי תאי השימוזה של הלבלב שם הוא כלול בקרומים מיוחדים וגורש דרך צינור הלבלב לתוך המעי, בזמן עיכול המזון: צ'ימוטריפסין הוא למעשה אנזים עיכול. החלבונים וחומרים המזינים שאנו בולעים באמצעות הדיאטה נתונים לעיכול כדי לצמצם לשרשראות קטנות יותר ולהיספג ולהפוך לאנרגיה (למשל עמילאזים ופרוטאזים מפרקים חומרים מזינים לגלוקוז וחומצות אמינו המגיעות לתאים, דרך כלי הדם. הם מגיעים לווריד הפורטל ומשם מועברים לכבד ושם הם עוברים טיפול נוסף).
אנזימים מיוצרים בצורה לא פעילה ומופעלים רק כשהם מגיעים ל"אתר שבו עליהם לפעול "; ברגע שהפעולה שלהם מסתיימת, הם מושבתים. לא ניתן להפעיל מחדש את האנזים, לאחר שהושבת, כדי שתהיה לו "פעולה קטליטית נוספת, יש להחליפו על ידי" מולקולת אנזים אחרת. אם הכימיטריפסין היה מיוצר בצורה פעילה כבר בלבלב, הוא היה תוקף את השני: דלקת הלבלב הינה פתולוגיות עקב אנזימי עיכול שכבר מופעלים בלבלב (ולא באתרים הנדרשים); חלקם אם לא מטופלים בזמן, להוביל למוות.
בשימוטריפסין ובכל פרוטאזות הסרין, הפעולה הקטליטי נובעת מקיומו של אניון האלכוהול (-CH2O-) בשרשרת הצדדית של הסרין.
פרוטאזות סרין לוקחות את השם הזה דווקא מכיוון שהפעולה הקטליטי שלהם נובעת מסרין.
לאחר שכל האנזים ביצע את פעולתו, לפני שהוא יכול לפעול מחדש על המצע, יש לשחזר אותו במים; "שחרור" הסרין על ידי המים הוא השלב האיטי ביותר של התהליך, וזהו השלב הזה הקובע את מהירות הקטליזה.
הפעולה הקטליטי מתרחשת בשני שלבים:
- היווצרות של האניון בעל תכונות קטליטיות (אניון אלכוהוליט) והתקפה נוקלאופילית שלאחר מכן על פחמן הקרבוניל (C = O) עם מחשוף של קשר הפפטיד ויצירת האסטר;
- התקפת מים עם שחזור הזרז (מסוגל להפעיל שוב את פעולתו הקטליטי).
האנזימים השונים השייכים למשפחת הפרוטאזים הסרינים יכולים להיות מורכבים מחומצות אמינו שונות אך עבור כולן האתר הקטליטי מיוצג על ידי האניון האלכוהולי של שרשרת הצד של הסרין.
תת -משפחה של פרוטאזות סרין היא של האנזימים המעורבים בקרישה (המורכבת מהפיכת החלבון, מצורתם הלא פעילה ל"צורה אחרת פעילה). אנזימים אלה מבטיחים שהקרישה תהיה יעילה ככל האפשר ומוגבלת המרחב והזמן (קרישה חייבת להתרחש במהירות וחייבת להתרחש רק בסביבת האזור הפגוע). האנזימים המעורבים בקרישה מופעלים במפל (מהפעלת אנזים בודד מתקבלים מיליארדי אנזימים: כל אנזים מופעל , בתורו מפעיל אנזימים רבים אחרים).
פקקת היא פתולוגיה הנובעת מתפקוד לקוי של אנזימי קרישה: היא נגרמת על ידי הפעלה, ללא צורך (מכיוון שאין פגיעה), של האנזימים המשמשים בקרישה.
ישנם אנזימים מאפיינים (רגולטוריים) ואנזימים מעכבים לאנזימים אחרים: אינטראקציה עם האחרונים, הם מווסתים או מעכבים את פעילותם; אפילו תוצר של אנזים יכול להיות מעכב לאנזים. ישנם גם אנזימים שעובדים ככל שהמצע קיים יותר.
ליזוזים
לואיג'י פסטר גילה, בהתעטשות על צלחת פטרי, כי בריר יש אנזים המסוגל להרוג חיידקים: ליזוזים; מהיוונית: ליסו = איזה גודל; זימו = אנזים.
ליזוזים מסוגל לפרק את דופן התא של חיידקים. חיידקים, ויצורים חד -תאיים באופן כללי, זקוקים למבנים עמידים מבחינה מכנית המגבילים את צורתם; בתוך החיידקים יש לחץ אוסמוטי גבוה מאוד ולכן הם מושכים מים. קרום הפלזמה היה מתפוצץ אם לא היה דופן תא המתנגדת לכניסת מים ומגבילה את נפח החיידק.
דופן התא מורכבת משרשרת פוליסכריד שבה מתחלפות מולקולות של N-acetyl-glucosamine (NAG) ומולקולות של N-acetyl-muramic חומצה (NAM); הקשר בין NAG ל- NAM נשבר על ידי הידרוליזה. קבוצת הקרבוקסיל של NAM, בדופן התא, עוסקת בקשר פפטיד עם חומצת אמינו.
בין השרשראות השונות נוצרים גשרים המורכבים מקשרים פסאודו-פפטידיים: ההסתעפות נובעת ממולקולת הליזין; המבנה בכללותו מסועף מאוד וזה נותן לו יציבות גבוהה.
ליזוזים הוא אנטיביוטיקה (הורג חיידקים): הוא פועל על ידי יצירת סדק בדופן החיידקים; כאשר מבנה זה (שהוא עמיד מכנית) נשבר, החיידק שואב מים עד שהוא מתפרץ. ליזוזים מצליח לשבור את הקשר β-1,4 הגלוקוזידי בין NAM ל- NAG.
האתר הקטליטי של הליזוזיים מיוצג על ידי חריץ העובר לאורך האנזים בו מוחדרת שרשרת הפוליסכרידים: שש טבעות גלוקוזידיות של השרשרת ממוקמות בחריץ.
במיקום השלישי של החריץ c "הוא חנק: במיקום זה ניתן להציב רק NAG אחד, מכיוון שה- NAM, שהוא בעל ממדים גבוהים יותר, אינו יכול להיכנס. האתר הקטליטי בפועל הוא בין עמדות ארבע לחמש: מכיוון שיש NAG במיקום השלישי, החיתוך יתרחש בין NAM ל- NAG (ולא להיפך); החיתוך, לפיכך, הוא ספציפי.
ה- pH האופטימלי עבור הליזוזים לעבודה הוא חמישה. באתר הקטליטי של האנזים, כלומר בין עמדות ארבע לחמישה, ישנן שרשראות הצד של חומצה אספרטית וחומצה גלוטמית.
תואר הומולוגיה: מודד את הזוגיות (כלומר דמיון) בין מבני חלבון.
קיים קשר הדוק בין ליזוזים לקטוז-סינתז.
לקטוז סינתטאז מסנתז לקטוז (שהוא סוכר החלב העיקרי): לקטוז הוא גלוקוזיד גלקטוזיל בו c "הוא קשר β-1,4 גלוקוזידי בין גלקטוז לגלוקוז.
לכן, סינתטאז הלקטוז מזרז את התגובה ההפוכה לתגובה המזרזת על ידי ליזוזים (שבמקום זה מפצל את הקשר הגלוקוזידי β-1,4)
הלקטוז סינתטאז הוא דימר, כלומר הוא מורכב משתי שרשראות חלבון, שאחת מהן בעלת תכונות קטליטי והיא דומה לליזוזיים והשנייה היא יחידת משנה רגולטורית.
במהלך ההריון, גליקופרוטאינים מסונתזים על ידי תאי בלוטת החלב על ידי פעולת גלטוזיל-טרנפראז (יש לו "הומולוגיה רצפית של 40% עם ליזוזים): אנזים זה מסוגל להעביר קבוצת גלקטוזיל ממבנה בעל אנרגיה גבוהה ל מבנה גליקופרוטאין. במהלך ההריון נגרמת ביטוי הגן המקודד לגלאקטוזיסיל טרנספראז (יש גם ביטוי של גנים אחרים שנותנים מוצרים אחרים): יש עלייה בגודל השד מכיוון שהוא מופעל בלוטת החלב (בעבר לא פעילה) שחייבת לייצר חלב. במהלך הלידה, α-lactalbumin מיוצר שהוא חלבון רגולטורי: הוא מסוגל לווסת את היכולת הקטליטי של גלקטוזיל טרנספראז (על ידי אפליה של המצע). Galactosyl-transferase שונה על ידי α-lactalalbumin מסוגל להעביר גלקטוזיל למולקולת גלוקוז: יצירת קשר β-1,4 גליקוזידי ומתן לקטוז (סינתזה לקטוז).
מכאן שגלקטוז טרנספז מכין את בלוטת החלב לפני הלידה ומייצר חלב לאחר הלידה.
כדי לייצר גליקופרוטאינים, גלקטוזיל טרנספראז נקשר לגלקטוזיל ול- NAG; במהלך הלידה האלבומין הלקטלי נקשר ל- galactosyltransferase מה שהופך אותו לזהות גלוקוז וכבר לא NAG לתת לקטוז.







.jpg)