כְּלָלִיוּת
מחלת וילסון, המכונה גם ניוון hepatolenticular, היא הפרעה גנטית נדירה המאופיינת בהצטברות נחושת ברקמות ובאיברי הגוף.

זוהי מחלה קטלנית.לכן, יש צורך בטיפול טיפולי המסיר נחושת מהרקמות ומונע הצטברות שלה.
כך גם מחלת וילסון
מחלת וילסון, הידועה גם בשם ניוון hepatolenticular, היא מחלה גנטית תורשתית הגורמת להצטברות מוגזמת של נחושת באיברים וברקמות מסוימות.
זוהי מחלה נדירה, הפוגעת באחד מכל 30,000 איש.
הצטברות הנחושת נובעת מפגם בחילוף החומרים שלו. למעשה הנחושת הנספגת בתזונה אינה מופרשת כראוי, ולכן היא נשארת בגוף ומופקדת בעיקר ב:
- כָּבֵד;
- מוֹחַ.
ובמידה פחותה, גם ב:
- קַרנִית;
- כליות;
- בדים אחרים.
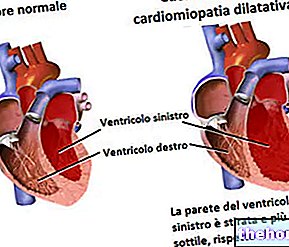
כמויות מוגזמות של נחושת באזורים אלה גורמות נזק לתאים. ההשפעות החמורות ביותר נמצאות בכבד ובמוח. במוח, הגרעין העדתי הוא זה שסובל מההשלכות הגדולות ביותר: מכאן השם האלטרנטיבי של ניוון הפטולנטיקולרי.
גורם ל
הגורם למחלת וילסון הוא "שינוי בגן ATP7B, הממוקם בכרומוזום 13, שכבר אינו מבצע את תפקודו התקין.
תפקידו של הגן ATP7B הוא לקדם את הפרשת העודף הנמצא בתאים באמצעות המרה, כאשר ATP7B נכשל, נחושת מצטברת במינונים כה גדולים עד שהוא בורח מהתאים וזורם לדם. נחושת מגיעה לרקמות הגוף השונות.
פתוגנזה
נחושת נצרכת בתזונה. ספיגתו מתרחשת במעי: כאן הוא נקשר לאלבומין (חלבון פלזמה) ומגיע לכבד. בשלב זה:
אצל אדם בריא:
- ATP7B מקדם את הקשר בין נחושת לסרולופלסמין. Ceruloplasmin הוא חלבון פלזמה המשמש להובלה והפרשת נחושת.
אולם אצל אדם הלוקה במחלת וילסון:
- ATP7B לא עובד. לכן הוא אינו מעדיף את הקשר בין נחושת לסרולופלסמין.
- נחושת נשארת קשורה לאלבומין, אינה מופרשת ומצטברת בתאי הכבד.
- תאי הכבד רוויים בתוכם כל כושר אחסון נחושת.
- לכן מתחם הנחושת-אלבומין מוגזם. לכן הוא בורח מההפטוציטים ונכנס לדם.
- דרך הדם, נחושת מגיעה לרקמות הגוף האחרות.
האיבר הראשון שמשלם את ההשלכות הוא אפוא הכבד; המוח, הכליות והקרנית עוקבים.

מדוע נחושת מתפשטת לטקסטיל?
אצל אנשים הסובלים ממחלת וילסון, נחושת מסתובבת בדם הקשור לאלבומין. הקשר הנחושת-אלבומיני הוא הרבה יותר עמיד מזה שבין נחושת לסרולופלסמין. למעשה, אין זיקה מועטה בין שני c הראשון ". כאשר הנחושת המורכבת מאלבומין מגיעה לרקמות ולאיברים השונים, הוא נתקל בחומרים שיש להם זיקה רבה יותר אליהם ונקשר אליהם. התוצאות הן שתיים:
- רקמות ואיברים מועשרים בנחושת.
- ריכוז הנחושת (cupremia) בדם יורד.

מתוך ויקיפדיה - לאמא ולאבא יש אלל מוטציה. בשל אופיו הרצסיבי של אלל זה, הם אינם מגלים כל מחלה, אך הם נשאים בריאים. שני ההורים יכולים להעביר אלל מוטציה אחד לילד כל אחד. במקרה זה, הילד יהיה הומוזיגי עבור האלל הנתון ויגלה את המחלה. בכל המקרים האחרים, הימצאותו של אלל בריא אחד או שניהם אינה גורמת להפרעה.
יְרוּשָׁה
מחלת וילסון היא מחלה תורשתית אוטוזומלית רצסיבית.
- אוטוסומלי, מכיוון שהגן ATP7B ממוקם בכרומוזום 13, כרומוזום שאינו מין.
- רצסיבי, כיוון שהאלל המוטה, הקובע את המחלה, הוא רצסיבי בהשוואה לבריא. כדי לחלות, אדם חייב להיות בעל שני אללים מוטנטים. למעשה, אלל יחיד שעבר מוטציה אינו מספיק כדי לגרום למחלה. אחד מכל 100 אנשים בסביבות נושאים אלל ATP7B שונה הדמות מסבירה בבירור מושג זה.
תסמינים
למידע נוסף: תסמיני מחלת וילסון
למרות שמדובר במחלה גנטית תורשתית, כבר בגילאים הראשונים אין הפרעות. התסמינים הראשונים, המבוססים על הכבד, מופיעים בסביבות גיל 6. בדרך כלל זהו הזמן המינימלי שלוקח להצטבר נחושת בכמויות מזיקות. במקרים מסוימים ההתחלה יכולה להתרחש בסוף גיל ההתבגרות או אפילו בסביבות גיל 30-40. עם הזמן, הפרעות מופיעות גם ברקמות אחרות.
תסמיני כבד
הכבד הוא האיבר הראשון שנפגע, מכיוון שהוא המחוז הראשון אליו מגיע הנחושת הנספגת מהתזונה. בריאות הכבד מתדרדרת בהדרגה. האבולוציה מתחילה בדרך כלל בגיל ההתבגרות ועוקבת אחר הקורס הבא:
- דַלֶקֶת הַכָּבֵד.
- שחמת חמורה לא.
- שחמת חמורה.
מצב שהוגדר על ידי הרופא נוצר עם המונח אי ספיקת כבד: הכבד כבר אינו מסוגל לבצע את תפקידיו.
סימנים אופייניים לאי ספיקת כבד הם:
- צַהֶבֶת.
- כאבי בטן.
- הוא התכופף.
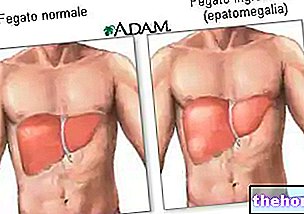
- הגדלת הכבד (הפטומגליה)
- הגדלת הטחול (splenomegaly)
סימפטומטולוגיה של המוח
נחושת מגיעה למוח רק כשהכבד כבר לא יכול לשמור אותו מוגבל לתאים שלו.
הפקדות במוח גורמות לנזק נוירולוגי בעל אופי אחר:
- מחלות פיזיות.
- רעד של הגפיים.
- איטיות בתנועה.
- קושי בדיבור (דיסארטריה).
- קושי בכתיבה.
- קושי בבליעה (דיספגיה).
- חוסר יציבות בהליכה.
- מִיגרֶנָה.
- אֶפִּילֶפּסִיָה.
- חולשת שרירים ונוקשות.
- הפרעות התנהגות.
- מצב הרוח משתנה.
- דִכָּאוֹן.
- חוסר יכולת להתרכז.
- האישיות משתנה.
- דמנציה.
אם המטופל אינו מטופל, הנזק הנוירולוגי מחמיר יותר ויותר: האדם הופך להיות תלוי לחלוטין באחרים, להאכיל ולנוע.
בדים אחרים

יתר על כן, נחושת יכולה להיות מופקדת גם בכליות. נוצר נזק לכליות, וכתוצאה מכך:
- Aminoaciduria. נוכחות חומצות אמינו בשתן.
- גליקוזוריה. נוכחות גלוקוז בשתן.
- פוספטוריה. נוכחות זרחן בשתן
- אוריקוסוריה. נוכחות של חומצת שתן בשתן.
- קלצ'וריה. נוכחות של סידן בשתן.
בתנאים רגילים, כל החומרים האבודים האלה ייספגו מחדש. לכן, הצטברות הכליות של הנחושת משנה את המבנה ואת הספיגה החוזרת של חומרים שעדיין מועילים לאורגניזם.
תסמינים אפשריים נוספים של מחלת וילסון הם:
- אֲנֶמִיָה.
- דלקת הלבלב.
- בעיות מחזור.
- הַפָּלָה.
- אוסטאופורוזיס מוקדם.
אִבחוּן
אם יש חשד למחלת וילסון, בדיקות אבחון שימושיות הן:
- בדיקות דם, לבדיקה:
- ריכוזי ceruloplasmin. רמה נמוכה, מתחת ל 20 מ"ג / 100 מ"ל, מעידה על המחלה. הערך הנורמלי הוא 30 מ"ג / 100 מ"ל.
- ריכוז הנחושת (cupremia). אם זה פחות מהרגיל, זה מעיד על המחלה.
- אנמיה המוליטית אפשרית.
- תפקודי הכבד והכליות, באמצעות הסמנים המתאימים שלהם (טרנסמינאזות, אזוטמיה וכו ')
- ניתוח שתן, להערכת כמות הנחושת הקיימת (cupruria). רמות גבוהות מהרגיל מעידות על המחלה. בדרך כלל, אנשים עם המצב מפרישים כ -100 מיקרוגרם נחושת בשתן כל 24 שעות.
- בדיקה אופטומטרית, לאיתור הימצאות טבעת קייזר-פליישר.
- ביופסיה של הכבד, למדידת תכולת הנחושת בתאי הכבד. רמת הנחושת הפתולוגית היא מעל 100 מיקרוגרם לגרם כבד. הוא שימושי גם להערכת מצב שחמת הכבד.
- בדיקת MRI של המוח, להערכת בריאות הגרעין העדתי, שאנו זוכרים שהוא אזור המוח המושפע מהצטברות נחושת.
- בדיקת DNA גנטית.
נוכחות בו זמנית של:
- טבעת קייזר-פליישר.
- סימנים לשחמת הכבד.
- נגע של הגרעין העדתי.
אין להשאיר ספק בנוגע לאבחון.
פרמטר נמדד
קופראמיה
110 מיקרוגרם / מ"ל
<100μg / ml
קופוריה
100 מיקרוגרם / 24 שעות
>> 100 מיקרוגרם / 24 שעות
Ceruloplasmin
30 מ"ג / מ"ל
<20 מ"ג / מ"ל
תֶרַפּיָה
ראה גם: תרופות לאי ספיקת יותרת הכליה
מחלת וילסון, ללא טיפול, היא קטלנית. מוות יכול להתרחש אפילו כמה שנים לאחר הופעת התסמינים הראשונים. החולה נתון להחמרה הדרגתית במצבו, הופך להיות תלוי יותר ויותר באחרים, ובהיעדר טיפול ספציפי, נזק לכבד ולמוח יכול להיות בלתי הפיך.
הטיפול מורכב מ:
- הפחתת מצבורי נחושת בכבד.
- בדוק את ספיגת הנחושת במעי.
- הפחת את הכנסת הנחושת הנלקחת עם הדיאטה.
- השתלת כבד.
הפחתת מצבורי נחושת
זהו השלב החשוב ביותר להצלת חיי המטופל. הוא מבוסס על ניהול של:
- פניצילאמין.
- טרינטינה.
פניצילאמין היא התרופה המועדפת עליה. הניהול שלה מתרחש דרך הפה ויש ליטול אותו לכל החיים. הוא מייצג חומר מסוג chelating המסוגל לבטל עודף נחושת ולהוביל אותו לכליות להפרשה. עם זאת, זה יכול לגרום לתופעות לא רצויות בכליה עצמה. במקרים אלה, מומלץ להפסיק את הטיפול כדי לפתור את הבעיות שעלו, ולאמץ אלטרנטיבה המבוססת על טרינטין.
טרינטין הוא גם חומר לידה. הוא מנוהל דרך הפה ומתנהג כמו פניצילאמין. הוא לא יעיל באותה מידה, אך גם תופעות הלוואי פחותות.
בדוק את ספיגת הנחושת במעי
אפשר להפחית את ספיגת הנחושת על ידי נטילת אבץ, דבר שמונע הצטברות נחושת בכבד. מתן אבץ מומלץ כאשר מחלת וילסון נמצאת בשלביה הראשונים. במילים אחרות, כאשר הנחושת עדיין לא פלשה לרקמות האחרות. הטיפול יעיל בשילוב עם טיפול פניצילמין.
הפחת את הכנסת נחושת
צריכת מזונות מסוימים העשירים בנחושת צריכה להיות מוגבלת, כגון:
- אֱגוזי מלך.
- כָּבֵד.
- פטריות.
- שוקולד.
- פירות ים.
בסך הכל, צריכת התזונה היומית של נחושת לא תעלה על 2 מ"ג.
השתלת כבד
זהו הטיפול הנדרש אם:
- נזק לכבד הוא בלתי הפיך. במקרה זה, אנו מדברים על שחמת חמורה.
- טיפולים קודמים לא היו יעילים.
פּרוֹגנוֹזָה
ככל שהטיפול יתחיל מוקדם יותר, כך הפרוגנוזה ואיכות החיים תהיה טובה יותר.
התערבות מאוחרת פירושה הגבלה ושיפור חלקי של נזק הכבד והמוח עקב עודף נחושת. חלק מהפונקציות, למעשה, נשארות נפגעות ללא תקנה.
במקרים חמורים, הפתרון היחיד לפרוגנוזה טובה יותר הוא השתלת כבד.



















.jpg)