רכיבים פעילים: Econazole (econazole nitrate), Triamcinolone (triamcinolone acetonide)
פיביזון 1% + 0.1% תחליב עור
אינדיקציות מדוע משתמשים ב- Pevisone? לשם מה זה?
קטגוריה פרמצבטית
נגזרות אימידאזול וטריאזול, אגודות
אינדיקציות תרפויטיות
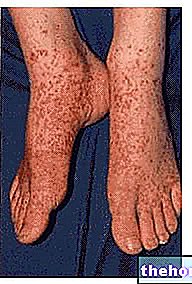
מיקוזיס של העור המאופיין בנוכחות מרכיב דלקתי חמור או על ידי ביטויים אלרגיים (אדמומיות, שלפוחיות, גלדים, גירוד והתקלפות).
התוויות נגד כאשר אין להשתמש ב- Pevisone
רגישות יתר לחומר הפעיל או לכל אחד מהחומרים הנלווים.
כמו כל המוצרים המכילים סטרואידים מקומיים, אין להשתמש ב- PEVISONE לאנשים הסובלים מבעיות עור ספציפיות כגון שחפת, אבעבועות רוח, הרפס סימפלקס או דלקות עור ויראליות אחרות. אין ליישם אותו על אתרי עור שבהם ניתן חיסון זה עתה. זה אסור גם לנבדקים אלרגיים לחנקת אקונאזול ו / או קורטיקוסטרואידים.
אמצעי זהירות לשימוש מה שאתה צריך לדעת לפני נטילת פביזון
לשימוש חיצוני בלבד. PEVISONE אינו מיועד לשימוש עיניים או דרך הפה. במקרה של רגישות או תגובת גירוי, יש להפסיק את השימוש במוצר. קורטיקוסטרואידים המורחים על העור עשויים להיספג בכמות מספקת לייצור תופעות מערכתיות, כולל דיכוי יותרת הכליה.ניתן להגדיל את הספיגה המערכתית על ידי גורמים שונים כגון יישום על פני שטח גדול של פני העור, יישום על עור פגום, יישום עם חבישת עור סתום וטיפול ממושך.
חולים ילדים עשויים להפגין רגישות רבה יותר לקורטיקוסטרואידים ולדיכוי ציר ההיפותלמוס-יותרת המוח-האדרנל (HPA) כתוצאה מתסמונת הגוף / יחס מסת הגוף. יש להיזהר בעת שימוש ב- PEVISONE. יש להפסיק את הטיפול בילדים אם מתרחשים סימנים לדיכוי ציר HPA או תסמונת קושינג.
קורטיקוסטרואידים אקטואליים קשורים לדילול עור וניוון, striae, telangiectasias ו purpura.
סטרואידים מקומיים עשויים להוביל לסיכון מוגבר לדלקות -על דרמטולוגיות או לזיהומים אופורטוניסטיים.
אינטראקציות אילו תרופות או מזונות יכולים לשנות את ההשפעה של Pevisone
ספר לרופא או לרוקח אם נטלת תרופות אחרות לאחרונה, גם תרופות ללא מרשם.
היו דיווחים על אינטראקציות עם נוגדי קרישה דרך הפה, כגון warfarin ו- acenocoumarol. בחולים המקבלים תרופות נוגדות קרישה דרך הפה, יש לנקוט משנה זהירות ולפקח על השפעתם נוגדת הקרישה בתדירות גבוהה יותר.
אזהרות חשוב לדעת כי:
הריון והנקה
שאל את הרופא או הרוקח שלך לייעוץ לפני נטילת תרופה כלשהי
בשל ספיגה מערכתית, אין להשתמש ב- PEVISONE במהלך השליש הראשון להריון אלא אם כן הורה הרופא שלך.
ניתן להשתמש ב- PEVISONE במהלך השליש השני והשלישי להריון אם התועלת הפוטנציאלית לאם עולה על הסיכונים האפשריים לעובר.
אין להשתמש בתרופות מסוג זה בכמויות גדולות, על שטחים גדולים של פני העור או לפרק זמן ממושך בחולים בהריון.
השפעה על כושר הנהיגה והשימוש במכונות
אתה לא שם לב.
מידע חשוב על חלק מהמרכיבים
PEVISONE מכיל בוטילהידרוקסיאניזול. זה יכול לגרום לתגובות עור מקומיות (למשל מגע דרמטיטיס) או גירוי בעיניים ובריריות.
PEVISONE מכיל חומצה בנזואית. מגרה מעט את העור, העיניים והריריות.
מינון, אופן וזמן הניהול אופן השימוש ב- Pevisone: מינון
PEVISONE יש למרוח בוקר וערב על משטח העור הפגוע בעיסוי קל.
משך הטיפול ב- PEVISONE לא יעלה על שמונה ימים; לדעת הרופא, לאחר מכן יימשך הטיפול עד להחלמה סופית רק עם האנטי פטרייתי.
מנת יתר מה לעשות אם נטלת יותר מדי פביזון
PEVISONE מיועד ליישום עור בלבד.
במקרה של מגע עם העיניים, יש לשטוף במים נקיים או עם מי מלח ולפנות לטיפול רפואי אם התסמינים ממשיכים. במקרה של בליעה / צריכת PEVISONE בשוגג, הודע לרופא מיד או פנה לבית החולים הקרוב.
אם יש לך שאלות בנוגע לשימוש ב- PEVISONE, שאל את הרופא או הרוקח.
תופעות לוואי מהן תופעות הלוואי של פביזון
כמו כל התרופות, PEVISONE יכול לגרום לתופעות לוואי, אם כי לא כולם מקבלים אותן.
תגובות הלוואי הנפוצות ביותר הן: תחושת צריבה בעור, גירוי בעור ואריתמה. תגובות נוספות שדווחו בעקבות מחקרים קליניים וניסיון לאחר השיווק הן: דרמטיטיס במגע, ניוון עור, גירוד, קילוף עור, נזקי עור, טלנגיאקטזיה, כאבים ונפיחות באתר היישום.
באופן מקומי, על העור המטופל, לפעמים יכולים להתרחש יובש, דלקת מקומית, התפרצויות אקנה, כתמים בהירים או צמיחת שיער.
עם זאת, הופעה של תופעות לא רצויות עשויה להיות מועדפת כאשר שטחי עור גדולים מטופלים במינונים גבוהים ולפרקי זמן ממושכים, או אם האזורים המטופלים נשמרים מכוסים בתחבושת.
אם התסמינים המקומיים הללו משמעותיים, רצוי להפסיק את הטיפול ולהתייעץ עם הרופא.
השימוש, במיוחד אם ממושך, במוצרים לשימוש מקומי יכול לגרום לתופעות רגישות המתבטאות באדמומיות ובגרד עז.אם זה קורה, יש צורך להפסיק את הטיפול ולפנות לרופא.
דיווח על תופעות לוואי
אם אתה נתקל בתופעות לוואי כלשהן, שוחח עם הרופא או הרוקח. זה כולל כל תופעות לוואי אפשריות שאינן מופיעות בעלון זה. תוכל גם לדווח על תופעות לוואי ישירות דרך אתר הדיווח הלאומי בכתובת https://www.aifa.gov.it/content/segnalazioni-reazioni-avverse. על ידי דיווח על תופעות לוואי תוכל לסייע במידע נוסף על בטיחות התרופה.
תפוגה ושמירה
תפוגה: עיין בתאריך התפוגה המצוין על האריזה.
תאריך התפוגה מתייחס למוצר באריזה שלמה, מאוחסן נכון.
אזהרה: אין להשתמש בתרופה לאחר תאריך התפוגה המצוין על האריזה.
אסור להשליך תרופות דרך שפכים או פסולת ביתית. שאל את הרוקח כיצד להיפטר מתרופות שאינך משתמש בהן יותר. הדבר יעזור להגן על הסביבה.
שמור על תרופה זו מחוץ לטווח הראייה והישג ידם של ילדים.
הרכב וצורה פרמצבטית
הרכב
100 גרם חלב דרמטולוגי מכילים: אקונאזול חנקתי 1 גרם; triamcinolone acetonide g 0.10. חומרים עזר: פוליאתילן גליקול פלמיטו סטיראט, פוליאוקסיאתילן אולאי גליצריד, פרפין נוזלי, בוטילהידרוקסיאניזול, חומצה בנזואית, מים מטוהרים.
טופס פארמי
תחליב עור: בקבוק של 30 מ"ל
עלון המקור: AIFA (סוכנות התרופות האיטלקית). תוכן שפורסם בינואר 2016. ייתכן שהמידע הנוכחי אינו מעודכן.
כדי לקבל גישה לגרסה העדכנית ביותר, מומלץ לגשת לאתר AIFA (סוכנות התרופות האיטלקית). כתב ויתור ומידע שימושי.
01.0 שם התרופה
פיביזון 1% + 0.1% תחליב עור
02.0 הרכב איכותי וכמותי
100 גרם של תחליב עור מכילים: אקונאזול חנקתי 1 גרם; triamcinolone acetonide 0.10 גרם.
מרכיבים עם השפעות ידועות: בוטילהידרוקסיאניזול, חומצה בנזואית.
לרשימת החומרים המלאים, ראה סעיף 6.1.
03.0 טופס פרמצבטי
תחליב עור לשימוש בעור.
04.0 מידע קליני
04.1 אינדיקציות טיפוליות
Pevisone מסומן בטיפול במיקוזים הנגרמים על ידי דרמטופיטים, שמרים ועובשים, המאופיינים בנוכחות של מרכיב דלקתי חמור או על ידי ביטויים אלרגיים כגון אקזמה מיקוטית, אקזמה מרגנטו של חברה, הרפס סירקטין, אינטרטריגו, folliculitis trichophytic, מיקו של הזקן , דרמטיטיס וכו '.
04.2 מינון ושיטת הניהול
מִנוּן
יש למרוח Pevisone בוקר וערב על משטח העור הפגוע בעיסוי קל.
משך הטיפול לא יעלה על שמונה ימים; לפי הצורך, הטיפול יימשך עד להחלמה סופית רק עם האנטי פטרייתי.
אוכלוסיית ילדים
אין נתונים זמינים.
04.3 התוויות נגד
רגישות יתר לחומרים הפעילים, לקורטיקוסטרואידים או לכל אחד מהחומרים המפורטים בסעיף 6.1.
בדומה לכל המוצרים המכילים סטרואידים לשימוש מקומי, גם ל- Pevisone יש התווית במצבי עור ספציפיים כגון שחפת, אבעבועות רוח, הרפס סימפלקס או זיהומים ויראליים אחרים בעור, או באתרים בהם ניתנה חיסון זה עתה.
04.4 אזהרות מיוחדות ואמצעי זהירות מתאימים לשימוש
לשימוש חיצוני בלבד. Pevisone אינו מיועד לשימוש עיניים או דרך הפה.
במקרה של רגישות או תגובת גירוי, הפסק את השימוש בתרופה.
קורטיקוסטרואידים המורחים על העור יכולים להיספג בכמות מספקת כדי לייצר תופעות מערכתיות, כולל דיכוי יותרת הכליה. ניתן להגדיל את הספיגה המערכתית על ידי גורמים שונים כגון יישום על פני שטח גדול של משטח העור, יישום על עור פגום, יישום עם תחבושת עור סתומה וטיפול ממושך.
קורטיקוסטרואידים אקטואליים קשורים לדילול עור וניוון, striae, telangiectasias ו purpura.
מטופלים בילדים עשויים להפגין רגישות רבה יותר לדיכוי ציר ההיפותלמוס-יותרת המוח-יותרת המוח (HPA) הנגרמת על ידי קורטיקוסטרואידים בהשוואה לשטח מבוגר / יחס מסת גוף.
יש לנקוט משנה זהירות כאשר Pevisone ניתנת לחולי ילדים ויש להפסיק את הטיפול אם מתרחשים סימנים לדיכוי ציר HPA או תסמונת קושינג.
קורטיקוסטרואידים מקומיים קשורים לדילול עור וניוון, striae, telangiectasias ו purpura.
קורטיקוסטרואידים מקומיים עשויים להוביל לסיכון מוגבר לזיהומי -על דרמטולוגיים או לזיהומים אופורטוניסטיים.
אוכלוסיית ילדים
אין נתונים זמינים.
מידע חשוב על חלק מהמרכיבים:
Pevisone מכיל hydroxyanisole butylated. זה יכול לגרום לתגובות עור מקומיות (למשל מגע דרמטיטיס) או גירוי בעיניים ובריריות.
פביזון מכיל חומצה בנזואית. מגרה מעט את העור, העיניים והריריות.
04.5 אינטראקציות עם מוצרי תרופות אחרים וצורות אינטראקציה אחרות
Econazole הוא מעכב ידוע של ציטוכרונות CYP3A4 ו- CYP2C9. למרות זמינות מערכתית מוגבלת לאחר יישום עורני, עלולות להתרחש אינטראקציות רלוונטיות מבחינה קלינית עם תרופות רפואיות אחרות, וחלקן דווחו בחולים שקיבלו נוגדי קרישה דרך הפה, כגון warfarin ו- acenocoumarol. בחולים המטופלים בטיפול נוגד קרישה דרך הפה, יש לנקוט משנה זהירות ולפקח על ה- INR בתדירות גבוהה יותר.ייתכן שיהיה צורך בהתאמת המינון של התרופה הנוגדת קרישה במהלך הטיפול ב- Pevisone ולאחר הפסקת הטיפול.
04.6 הריון והנקה
הֵרָיוֹן
אין מחקרים הולמים ומבוקרים, ואין נתונים אפידמיולוגיים על ההשפעות הבלתי רצויות הנובעות משימוש ב- Pevisone בהריון.
יש להשתמש ב- Pevisone רק בשליש הראשון של ההריון אם הרופא סבור שזה נחוץ לבריאות המטופלת.
ניתן להשתמש בפביזון במהלך השליש השני והשלישי להריון אם התועלת הפוטנציאלית לאם עולה על הסיכונים האפשריים לעובר.
אין להשתמש בתרופות מסוג זה בכמויות גדולות, על שטחים גדולים של פני העור או לתקופה ממושכת בחולים בהריון.
מחקרים בבעלי חיים הראו רעילות פוריות (פטוטוקסיות עם אקונאזול וטרטוגניות עם טריאמיצינולון) (ראה סעיף 5.3). עם זאת, הסיכון בבני אדם אינו ידוע.
אקונאזול חנקתי
מחקרים בבעלי חיים הראו רעילות פוריות (ראה סעיף 5.3). אצל גברים, לאחר יישום מקומי על עור שלם, הספיגה המערכתית של אקונאזול ירודה (
טריאמיצינולון אצטוניד
מחקרים בבעלי חיים הראו רעילות פוריות (ראה סעיף 5.3). הנתונים המעטים הקיימים בספרות מצביעים על כך שעד 5% מהטריאמצינולון המיושם על העור נספג באופן סיסטמי בבני אדם.
זמן האכלה
אין מחקרים מתאימים ומבוקרים על מתן מקומי של Pevisone במהלך ההנקה. לא ידוע אם מתן מקומי של Pevisone יכול לגרום לספיגה מערכתית מספקת בכדי לייצר כמויות ניתנות לגילוי בחלב אם. יש לנקוט משנה זהירות כאשר מתן Pevisone לנשים אשר לְהַנִיק.
אקונאזול חנקתי
לאחר מתן אוראלי של חנקת אקונאזול לחולדות מניקות, אקונאזול ו / או מטבוליטים מופרשים בחלב ונמצאו בגורים סיעודיים. לא ידוע אם מתן מקומי של חנקת אקונאזול עלול לגרום לספיגה מערכתית מספקת בכדי לייצר כמויות ניתנות לחלב אם.
טריאמיצינולון אצטוניד
אין מחקרים בבעלי חיים לאיתור טריאמיצינולון במהלך ההנקה. לא ידוע אם מתן מקומי של טריאמצינולון יכול לגרום לספיגה מערכתית מספקת בכדי לייצר כמויות ניתנות לחלב אם.
פוריות
אקונאזול חנקתי
תוצאות ממחקרי רבייה בבעלי חיים לא הראו השפעות על הפוריות (ראה סעיף 5.3).
טריאמיצינולון אצטוניד
אין נתונים זמינים.
04.7 השפעות על יכולת הנהיגה וההתנהלות במכונות
לא ידוע.
04.8 תופעות לא רצויות
נתוני ניסוי קליני
הבטיחות של Pevisone [econazole nitrate (1%) ו- triamcinolone acetonide (0.1%)] הוערכה בקרב 182 מבוגרים שהשתתפו ב -4 מחקרים קליניים. בהתבסס על נתוני הבטיחות שנאספו ממחקרים קליניים אלה, התגובות השליליות של תופעות הלוואי הנפוצות ביותר (שכיחות ≥ 1%) היו (עם שכיחות%): תחושת צריבה בעור (1.6%), גירוי בעור (1.6%).
בטיחות Pevisone הוערכה גם ב -101 ילדים (בגילאי 3 חודשים עד 10 שנים) שהשתתפו במחקר קליני. תופעת הלוואי הנפוצה ביותר (שכיחות ≥ 1%) הייתה (עם שכיחות%): אריתמה (1.0%).
באופן כללי, פרופיל הבטיחות של Pevisone דומה למבוגרים ולילדים.
הטבלה שלהלן מציגה את תופעות הלוואי החלות של Pevisone, הנובעות הן ממחקרים קליניים (מבוגרים וילדים) והן מניסיון לאחר השיווק, כולל תגובות הלוואי שכבר הוזכרו לעיל.
התדרים מדווחים בהתאם לאמנה הבאה: שכיח מאוד (≥ 1/10); נפוץ (≥1 / 100,
טבלה 1: תגובות שליליות של תרופות
באופן מקומי, על העור המטופל, לפעמים יכולים להתרחש יובש, פוליקוליטיס, התפרצויות אקנה, היפרטריכוזה והיפופגמנטציה.
עם זאת, הופעה של תופעות לא רצויות עשויה להיות מועדפת כאשר שטחי עור גדולים מטופלים במינונים גבוהים ולפרקי זמן ממושכים, או אם האזורים המטופלים נשמרים מכוסים בתחבושת.
דיווח על חשדות לתגובות שליליות
דיווח על תגובות שליליות החשודות המתרחשות לאחר אישור המוצר הוא חשוב מאחר והוא מאפשר ניטור מתמשך של איזון התועלת / הסיכון של המוצר. רופאים מתבקשים לדווח על כל חשד לתגובות שליליות באמצעות מערכת הדיווח הלאומית. "כתובת https: //www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
04.9 מנת יתר
Pevisone מיועד ליישום עור בלבד. קורטיקוסטרואידים המורחים על העור, כולל טריאמצינולון, יכולים להיספג בכמות מספקת כדי לייצר השפעות מערכתיות. במקרה של בליעה בשוגג עלולות להופיע בחילות, הקאות ושלשולים ולטפל בטיפול סימפטומטי. אם Pevisone מוחל בטעות על העיניים, יש לשטוף במים או עם מי מלח ולפנות לטיפול רפואי אם התסמינים ממשיכים.
05.0 נכסים פרמקולוגיים
05.1 תכונות פרמקודינמיות
קבוצה פרמקותרפית: נגזרות אימידאזול וטריאזול, שילובים.
קוד ATC: D01AC20.
Pevisone מבצעת את פעולתה הודות להשפעות המשולבות של אקונאזול (אנטי פטרייתי) וקורטיקוסטרואיד (אנטי דלקתי). הראשון, שחדר לתא המיקוטי, משנה את מערכות הממברנה שלו עם הופעה והצטברות של מוצרי פירוק וכתוצאה מכך חסימה של חילוף החומרים של "RNA, חלבונים ושומנים. הקורטיזון מעכב את התפתחות כל התופעות האופייניות לדלקת, כגון היפרתרמיה מקומית, אדמומיות ובצקת.
שני המרכיבים נמצאים בפביזון במערכות יחסים כאלה שלא יפריעו למנגנון הפעולה של זה.
המחקרים הקליניים שבוצעו הוכיחו את התועלת של השימוש בשילוב ביחס לשימוש בתכשיר האנטי פטרייתי בלבד במקרים בהם הדבר מצוין.
05.2 "תכונות פרמקוקינטיות
אקונאזול חנקתי
קְלִיטָה
ספיגה מערכתית של אקונאזול נמוכה במיוחד לאחר יישום מקומי על העור. ריכוזי ממוצע של פלזמה / סרום של אקונאזול ו / או מטבוליטים שלו נצפו 1-2 ימים לאחר הטיפול ושהשכבה הקרנית חורגת מהריכוז המעכב המינימלי של דרמטופיטים וריכוזים מעכבים מגיעים באמצע הדרמיס.
הפצה
Econazole ו / או המטבוליטים שלו במחזוריות המערכתית נקשרים מאוד (> 98%) לחלבונים בסרום.
ביו טרנספורמציה
Econazole המגיעה למחזור הדם המערכתי עוברת חילוף חומרים נרחב על ידי חמצון של טבעת האימידאזול ואחריה O-dealkylation ו- glucuronation.
חיסול
אקונאזול ומטבוליטים שלה מסולקים דרך הכליות והצואה.
טריאמיצינולון אצטוניד
קְלִיטָה
מידת הספיגה המתרפקת של קורטיקוסטרואידים מקומיים נקבעת על ידי גורמים רבים, כולל הרכב, תקינות מחסום העור ושימוש בחבישות חסימות. קורטיקוסטרואידים מקומיים יכולים להיספג מעור שלם. דלקות ו / או תהליכים פתולוגיים אחרים של העור מגבירים את הספיגה הפרוטואנית.התחבושות הכובשות מגבירות משמעותית את הספיגה הפרוטוקנית של קורטיקוסטרואידים מקומיים.
הפצה
לקורטיקוסטרואידים מקומיים, לאחר שנספגו דרך העור, יש פרמקוקינטיקה דומה לקורטיקוסטרואידים הניתנים באופן שיטתי.
ביו טרנספורמציה
קורטיקוסטרואידים עוברים חילוף חומרים בעיקר בכבד.
חיסול
קורטיקוסטרואידים מופרשים לאחר מכן דרך הכליה. כמה סטרואידים מקומיים ומטבוליטים שלהם מופרשים גם הם במרה.
05.3 נתוני בטיחות פרה -קליניים
אקונאזול חנקתי
ההשפעות נצפו במחקרים פרה -קליניים בחשיפות הנחשבות במידה מספקת מעבר לחשיפה האנושית המקסימלית.
מחקרי רעילות חריפה מראים שולי בטיחות גדולים. במינונים גבוהים (50 מ"ג / ק"ג / יום) מחקרי רעילות במינון חוזר הכבד זוהה כאיבר מטרה עם רעילות מינימלית והחלמה מלאה.
לא נצפו רעילות אקטואליות משמעותיות, פוטוטוקסיות, גירוי בעור מקומי, גירוי בנרתיק או רגישות. נצפתה גירוי קל בעיניים.
קרצינוגנזה / מוטגנזה
מחקרים מסרטנים לא נערכו בשל תקופת הניהול הקצרה המוצעת במסלול שעלול להוביל להתפתחות תצורות גידול.
בבדיקות שונות לא הייתה נוכחות או הגבלה של השפעות גנוטוקסיות (סטיות כרומוזומליות מבניות).
רעילות רבייה
תוצאות מחקרים בבעלי חיים הראו רעילות פוריות.
פוריות
תוצאות מחקרי הרבייה עם אקונאזול לא הראו כל השפעה על הפוריות.
הֵרָיוֹן
הישרדות ילודה נמוכה ורעילות עוברית היו קשורים רק לרעילות אימהית. במחקרים בבעלי חיים, ניטראט אקונאזול לא הראה השפעות טרטוגניות, אך עובריות וטוטוקסיות במכרסמים, במינון התת -עורי האימהי של 20 מ"ג / ק"ג ליום ובמינון אוראלי של 10 מ"ג / ק"ג ליום. המשמעות של נתונים אלה אצל האדם לא ידוע.
טריאמיצינולון אצטוניד
כמקובל בקורטיקוסטרואידים אחרים, הקטלניות עולה עם משך החשיפה במודלים של בעלי חיים, כאשר סיבת המוות העיקרית קשורה לספטימיה ככל הנראה עקב דיכוי מנגנון התגובה החיסונית של החיה.
קרצינוגנזה / מוטגנזה
לא בוצעו מחקרים ארוכי טווח בבעלי חיים על מנת להעריך את הפוטנציאל המסרטן של סטרואידים מקומיים. במחקר בן 104 שבועות בחולדות זכרים, טריאמיצינולון אצטוניד גרם לשכיחות מוגברת של אדנומה hepatocellular ואדנומה / קרצינומה בשילוב במינון רעיל של ≥5 מק"ג / ק"ג. תוצאות אלו נחשבו לייצוג אפקט מסוג e. כנראה במעורבות של קולטני גלוקוקורטיקואיד אין נתונים אחרים על carginogenesis.
Triamcinolone acetonide היה חיובי בבדיקת המיקרו -גרעין (בדיקת מוטגנזה).
רעילות רבייה
טריאמיצינולון (בתוך ומחוץ לטווח הטיפולי) נקשר לחיך שסוע בצאצאים כאשר הוא ניתן לעכברים, חולדות, ארנבים ואוגרים בהריון והיפופלזיה ריאתית בחולדות. בפרימטים לא אנושיים, מתן טריאמצינולון (במינוני מערכת העצבים המרכזית מערכת, פגמים בצינור העצבי, הפרעות גולגולת ושלד ופיגור בצמיחה.
פוריות
אין נתונים זמינים.
הֵרָיוֹן
אין נתונים זמינים.
06.0 מידע פרמצבטי
06.1 מרכיבים
פוליאתילן גליקול פלמיטו סטיראט, פוליאוקסיאתילן גליצריד אולאי, פרפין נוזלי, בוטילהידרוקסיאניזול, חומצה בנזואית, מים מטוהרים.
06.2 חוסר התאמה
לא ידוע.
06.3 תקופת תוקף
המוצר תקף לשנתיים.
הנתונים מתייחסים למוצר באריזה שלמה ומאוחסנת כהלכה.
06.4 אמצעי זהירות מיוחדים לאחסון
יש לאחסן בטמפרטורה שלא תעלה על 25 מעלות צלזיוס.
06.5 אופי האריזה המיידית ותכולת האריזה
בקבוק פוליאתילן בצפיפות גבוהה המכיל 30 מ"ל של תחליב עור.
06.6 הוראות שימוש וטיפול
אין הוראות מיוחדות לסילוק.
מחזיק רשות השיווק 07.0
Janssen-Cilag SpA
Via M. Buonarroti, 23
20093 COLOGNO MONZESE (מילאנו)
08.0 מספר אישור השיווק
AIC n. 025036029
09.0 תאריך האישור הראשון או חידוש האישור
תאריך האישור הראשון: יוני 2000
תאריך החידוש האחרון: יוני 2010
10.0 תאריך עיון הטקסט
קביעת AIFA מיום 14 באוקטובר 2015














-crocchette-di-pesce-vegane.jpg)