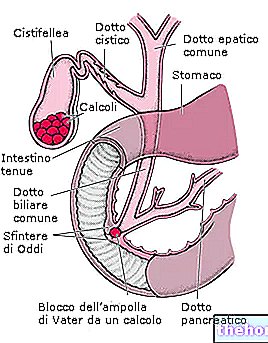
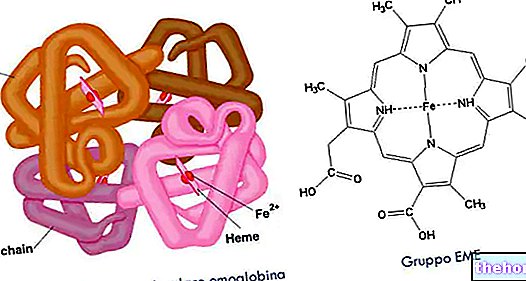
על מנת להיות מסוגל לדבר בצורה מובנת של "המוגלובין (Hb), כדאי לדאוג לראשון מיוגלובין (Mb) הדומה מאוד להמוגלובין אך הוא הרבה יותר פשוט. בין המוגלובין למיוגלובין יש יחסי קרבה קרובים: שניהם חלבונים מצומדים וקבוצת התותבות שלהם (חלק שאינו חלבון) היא הקבוצה heme.
מיוגלובין הוא חלבון כדורי המורכב משרשרת אחת המונה כמאה וחמישים חומצות אמינו (תלוי באורגניזם) ומשקלו המולקולרי הוא כ -18 ק"ג.
כאמור, הוא מצויד בקבוצת heme שמוכנסת לחלק הידרופובי (או ליפופילי) של החלבון, המורכבת מקפלים המיוחסים למבני α-helix של החלבונים הסיבים.
מיוגלובין מורכב בעיקר מקטעי α-helices, הנמצאים במספר שמונה ומורכב, כמעט אך ורק, משאריות לא קוטביות (leucine, valine, methionine and phenylalanine) בעוד שאריות קוטביות נעדרות כמעט (חומצה אספרטית, חומצה גלוטמית, ליזין) וארגינין); שאריות הקוטב היחידות הן שני היסטידינים, הממלאים תפקיד מהותי בהתקשרות החמצן לקבוצת החם.
קבוצת ההמה היא קבוצת כרומופורים (נספגת בגלוי) והיא הקבוצה התפקודית של מיוגלובין.
ראו גם: המוגלובין מסוכרר - המוגלובין בשתן
קצת כימיה

הקשר בין פרוטופורפירין לברזל הוא קשר טיפוסי של תרכובות תיאום שהן תרכובות כימיות שבהן אטום (או יון) מרכזי יוצר קשרים עם מינים כימיים אחרים במספר הגדול יותר ממספר החמצון שלו (מטען חשמלי). במקרה של heme, קשרים אלה הינם הפיכים וחלשים.
מספר התיאום (מספר קשרי הקואורדינציה) של ברזל הוא שש: יכולות להיות שש מולקולות סביב הברזל החולקות את האלקטרונים המקשרים.
כדי ליצור מתחם קואורדינציה נדרש שני אורביטלים בעלי אוריינטציה נכונה: האחד מסוגל "לרכוש" אלקטרונים והשני מסוגל לתרום אותם.
בהמה, ברזל יוצר ארבעה קשרים מישוריים עם ארבעת אטומי החנקן במרכז הטבעת הפרוטו-פורפירין וקשר חמישי עם חנקן היסטידין פרוקסימלי; לברזל יש את הקשר התיאום החופשי השישי והוא יכול להיקשר לחמצן.
כאשר הברזל הוא בצורת יון חופשי, סוג האורביטלים שלו ד לכולם אותה אנרגיה; במיוגלובין, יון הברזל נקשר לפרוטופורפירין ולהיסטידין: מינים אלה מפריעים מגנטית לאורביטלים ד קצת ברזל; היקף ההפרעה יהיה שונה באורביטלים השונים ד בהתאם לאוריינטציה המרחבית שלהם ושל המינים המטרידים. מכיוון שהאנרגיה הכוללת של האורביטלים חייבת להיות קבועה, ההפרעה גורמת להפרדה אנרגטית בין האורביטלים השונים: האנרגיה שנרכשת על ידי כמה אורביטלים מקבילה לאנרגיה שאבדה האחרים.
אם ההפרדה המתרחשת בין האורביטלים אינה גדולה במיוחד, עדיף סידור אלקטרוני בספין גבוה: האלקטרונים המחייבים מנסים לסדר את עצמם בספינים מקבילים בכמה שיותר רמות משנה (ריבוי מקסימלי); אם, לעומת זאת, ההפרעה חזקה מאוד ויש הפרדה גדולה בין האורביטלים, ייתכן שיהיה נוח יותר לשייך את אלקטרונים הקשר באנרביטלים הנמוכים (ספין נמוך).
כאשר ברזל נקשר לחמצן, המולקולה מניחה סידור ספין נמוך בעוד שכאשר לברזל יש את הקשר התיאום השישי חינם, למולקולה יש סידור ספין גבוה.
הודות להבדל הספין הזה, באמצעות ניתוח ספקטרלי של מיוגלובין, אנו מסוגלים להבין אם חמצן (MbO2) קשור אליו או לא (Mb).
מיוגלובין הוא חלבון שריר אופייני (אך אינו נמצא רק בשרירים).
מיוגלובין מופק מלווייתן הזרע בו הוא נמצא בכמויות גדולות ואז מטוהר.
לבלוגים יש נשימה כמו של בני אדם: בעלי ריאות הם חייבים לספוג אוויר בתהליך הנשימה; לווייתן הזרע חייב להכניס כמה שיותר חמצן לשרירים שמסוגלים לצבור חמצן על ידי קישורו למיוגלובין הקיים בהם; החמצן משתחרר לאחר מכן באיטיות כאשר החומוס טבול מכיוון שחילוף החומרים שלו דורש חמצן: כמות גדולה יותר של חמצן אותו לווייתן הזרע מסוגל לספוג וככל שיותר חמצן זמין במהלך הצלילה.
מיוגלובין קושר חמצן בצורה הפיכה והוא קיים ברקמות הפריפריה באחוזים גדולים יותר ככל שהרקמה רגילה יותר לעבודה עם אספקת חמצן המרוחקת בזמן.
<--- מיוגלובין הוא חלבון הנמצא בשרירים, שתפקידו הוא בדיוק תפקידו של "מאגר" חמצן.
מה שהופך את הבשר לאדום פחות או יותר הוא תכולת ההמופרוטאינים (זהו האם שהופך את הבשר לאדום).
להמוגלובין יש קווי דמיון מבניים רבים למיוגלובין והוא מסוגל לקשור חמצן מולקולרי בצורה הפיכה; אך, בעוד שמיוגלובין מוגבל לשרירים ורקמות היקפיות באופן כללי, המוגלובין מצוי באריתרוציטים או בתאי דם אדומים (הם תאי פסאודו, כלומר, הם אינם תאים אמיתיים) המהווים 40% מהדם.
בניגוד למיוגלובין, עבודתו של המוגלובין היא לקחת חמצן לריאות, לשחרר אותו לתאים היכן שהוא נחוץ, לקחת פחמן דו חמצני ולשחרר אותו לריאות שם המחזור מתחיל מחדש.
L "הֵמוֹגלוֹבִּין זהו טטרמטר, כלומר, הוא מורכב מארבע שרשראות פוליפפטיד כל אחת עם קבוצת heme ושתי זהות שתיים (בבן אדם יש שתי שרשראות אלפא ושתי שרשראות בטא).
תפקידו העיקרי של המוגלובין הוא הובלת חמצן; תפקיד נוסף של הדם בו המוגלובין מעורב הוא הובלת חומרים לרקמות.
בנתיב מהריאות (עשיר בחמצן) לרקמות המוגלובין נושא חמצן (במקביל החומרים האחרים מגיעים לרקמות) בעוד שבדרך ההפוכה הוא נושא עמו את הפסולת שנאספת על ידי הרקמות, במיוחד הפחמן דו חמצני המיוצר במטבוליזם.
בהתפתחות של בן אנוש ישנם גנים המתבטאים רק לפרק זמן מסוים; מסיבה זו ישנם המוגלובין שונים: עוברי, עוברי, של הגבר הבוגר.
השרשראות המרכיבות את ההמוגלובין השונות הללו הן בעלות מבנים שונים אך עם כמה קווי דמיון למעשה התפקוד שהם מבצעים פחות או יותר זהה.
הסבר לנוכחותן של כמה שרשראות שונות הוא כדלקמן: במהלך התהליך האבולוציוני של אורגניזמים, אפילו המוגלובין התפתח בהתמחות בהעברת חמצן מאזורים העשירים בו לאזורים חסרים. בהתחלה " מהשרשרת האבולוציונית המוגלובין העביר חמצן באורגניזמים קטנים; במהלך האבולוציה האורגניזמים הגיעו למימדים גדולים יותר, ולכן המוגלובין שונה כדי שיוכל להעביר חמצן לאזורים רחוקים יותר מהנקודה שבה הוא היה עשיר בו; לעשות זאת הם מקודדים, במהלך התהליך האבולוציוני, מבנים חדשים של השרשראות המרכיבים את ההמוגלובין.
מיוגלובין קושר חמצן אפילו בלחצים צנועים; ברקמות ההיקפיות יש לחץ (PO2) של כ -30 מ"מ כספית: מיוגלובין בלחץ זה אינו משחרר חמצן, כך שהוא לא יהיה יעיל כמוביל חמצן. המוגלובין, לעומת זאת. , יש לו התנהגות אלסטית יותר: הוא קושר חמצן ללחצים גבוהים ומשחרר אותו כאשר הלחץ יורד.
כאשר חלבון פעיל מבחינה תפקודית, הוא יכול לשנות מעט את צורתו; לדוגמה, למיוגלובין מחומצן יש צורה שונה ממיוגלובין שאינו מחומצן ומוטציה זו אינה משפיעה על שכניו.
המצב שונה במקרה של חלבונים קשורים כגון המוגלובין: כאשר שרשרת מחמצנת היא נגרמת לשנות את צורתה אך שינוי זה הוא תלת מימדי ולכן גם השרשראות האחרות של הטטרמטר מושפעות. העובדה שהשרשראות מקושרות אחד עם השני., מציע כי השינוי של אחד משפיע על השכנים האחרים גם אם במידה שונה; כאשר שרשרת מחמצנת, השרשראות האחרות של הטטרמטר מניחות "גישה פחות עוינת" כלפי חמצן: הקושי שבו שרשרת אותו החמצנים יורדים כאשר השרשראות הקרובות אליו מחמצנות בתורן. אותו דבר לגבי דיאוקסיגנציה.
המבנה הרביעי של הדיאוקסיהמוגלובין נקרא הצורה T (מתוחה) ואילו המבנה של אוקסימוגלובין נקרא הצורה R (משוחררת); במצב המתוח יש סדרה של אינטראקציות אלקטרוסטטיות די חזקות בין חומצות אמינו חומציות וחומצות אמינו בסיסיות שמובילות למבנה קשיח של deoxyhemoglobin (זו הסיבה "הצורה המתוחה"), בעוד שכאשר חמצן מקושר, הישות של אלה האינטראקציות פוחתות (ומכאן ה"צורה המשוחררת "). יתר על כן, בהיעדר חמצן, מטען ההיסטידין (ראה מבנה) מתייצב על ידי המטען ההפוך של החומצה האספרטית בעוד שנוכחות חמצן קיימת נטייה מצד החלבון לאבד פרוטון; כל זה כרוך בכך שהמוגלובין מחומצן הוא חומצה חזקה יותר מהמוגלובין נטול חמצון: אפקט bohr.
בהתאם ל- pH, קבוצת ההם נקשרת פחות או יותר לחמצן: בסביבה חומצית המוגלובין משחרר חמצן ביתר קלות (הצורה המתוחה יציבה) בעוד שבסביבה בסיסית הקשר עם חמצן קשה יותר.

כל המוגלובין משחרר 0.7 פרוטונים לשומה של חמצן (O2) שנכנס.
אפקט הבוהר מאפשר להמוגלובין לשפר את יכולתו לשאת חמצן.
ההמוגלובין העובר מהריאות לרקמות חייב לאזן את עצמו כפונקציה של לחץ, pH וטמפרטורה.
בואו נראה את השפעת הטמפרטורה.
הטמפרטורה ב- alveoli הריאתי נמוכה בכ -1-1.5 מעלות צלזיוס מהטמפרטורה החיצונית בעוד שבשרירים הטמפרטורה היא כ -36.5-37 ° C; ככל שהטמפרטורה עולה, גורם הרוויה יורד (באותו לחץ): זה קורה מכיוון שהאנרגיה הקינטית עולה והדיסוציאציה מועדפת.

ישנם גורמים נוספים שיכולים להשפיע על יכולתו של המוגלובין להיקשר לחמצן, אחד מהם הוא ריכוז 2,3 ביספוספוגליצרט.
2,3 ביספוספוגליצראט הוא מטבולי המצוי באריתרוציטים בריכוז של 4-5 מ"מ (בשום חלק אחר של האורגניזם הוא אינו קיים בריכוז כה גבוה).
ב- pH פיזיולוגי, 2,3 ביספוספוגליצרט מופחת ומכיל חמישה מטענים שליליים; הוא דבוק בין שתי שרשראות הבטא של המוגלובין מכיוון שרשראות אלו בעלות ריכוז גבוה של מטענים חיוביים. האינטראקציות האלקטרוסטטיות בין שרשראות הבטא לבין 2,3 הביספוספוגליצראט מעניקות נוקשות מסוימת למערכת: מתקבל מבנה מתוח בעל זיקה מועטה לחמצן; במהלך החמצון, 2,3 הביספוספוגליצרט גורש לאחר מכן.
באריתרוציטים c "הוא מכשיר מיוחד הממיר 1,3 ביספוספוגליצרט (המיוצר על ידי מטבוליזם) ל -2,3 ביספוספוגליצרט כך שהוא מגיע לריכוז של 4-5 מ"מ ולכן המוגלובין מסוגל להחליף את" החמצן ברקמות.
ההמוגלובין המגיע לרקמה נמצא במצב המשוחרר (קשור לחמצן), אך בקרבת הרקמה הוא קרבוקסילי ועובר למצב המתוח: לחלבון במצב זה יש נטייה פחותה להיקשר עם חמצן, בכבוד למצב המשוחרר, לכן המוגלובין משחרר חמצן לרקמה; יתר על כן, על ידי תגובה בין מים לפחמן דו חמצני, יש ייצור של יוני H +, ולכן חמצן נוסף עקב אפקט הבוהר.
פחמן דו חמצני מתפזר לתוך האריתרוציט העובר דרך קרום הפלזמה; מכיוון שאריתרוציטים מהווים כ -40% מהדם, עלינו לצפות שרק 40% מפחמן דו חמצני המתפזר מהרקמות נכנס אליהם, למעשה 90% מפחמן דו חמצני נכנס לאריתרוציטים מכיוון שהם מכילים אנזים הממיר פחמן דו חמצני. בחומצה פחמנית, זה גורם לריכוז נייח של פחמן דו חמצני באריתרוציטים נמוך ולכן קצב הכניסה גבוה.

תופעה נוספת המתרחשת כאשר אריתרוציט מגיע לרקמה היא הבאה: לפי שיפוע, "HCO3- (נגזרת של פחמן דו חמצני) עוזב את" האריתרוציט וכדי לאזן את תפוקת המטען השלילי, יש לנו את הכניסה של כלוריד אשר קובע עלייה בלחץ האוסמוטי: לאיזון וריאציה זו יש גם כניסת מים הגורמת להתנפחות האריתרוציט (אפקט המבורגר) .התופעה ההפוכה מתרחשת כאשר אריתרוציט מגיע לאלוואולי הריאתי: דפלציה של האריתרוציטים (אפקט HALDANE) לכן אריתרוציטים הוורידים (המופנים לריאות) הם עגולים יותר מאשר העורקים.








-e-ruscogenina.jpg)