רכיבים פעילים: Golimumab
פתרון סימפוני 50 מ"ג להזרקה בעט מלא מראש
תוספות אריזה של סימפוני זמינות למידות האריזה:- פתרון סימפוני 50 מ"ג להזרקה בעט מלא מראש
- פתרון סימפוני 100 מ"ג להזרקה בעט מלא מראש
אינדיקציות מדוע משתמשים ב- Simponi? לשם מה זה?
סימפוני מכיל חומר פעיל הנקרא golimumab.
סימפוני שייכת לקבוצת תרופות הנקראות 'חוסמי TNF'. הוא משמש למבוגרים לטיפול במחלות הדלקתיות הבאות:
- דלקת מפרקים שגרונית
- דלקת מפרקים פסוריאטית
- ספונדילוארתריטיס צירית, כולל ספונדיליטיס אנקילוזינג וספונדילוארתריטיס צירית לא רדיוגרפית
- קוליטיס כיבית
בילדים במשקל של 40 ק"ג לפחות, סימפוני משמש לטיפול בדלקת מפרקים אידיופטית לנוער רב -מפרקית.
סימפוני פועל על ידי חסימת פעולת חלבון הנקרא "גורם נמק הגידול אלפא" (TNF-α). חלבון זה מעורב בתהליכים הדלקתיים של הגוף ועל ידי חסימתו ניתן להפחית את הדלקת בגוף.
דלקת מפרקים שגרונית
דלקת מפרקים שגרונית הינה מחלת מפרקים דלקתית. אם יש לך דלקת מפרקים שגרונית פעילה, תחילה תטופל בתרופות אחרות. אם אינך מגיב כראוי לתרופות אלו, תטופל עם סימפוני בשילוב עם תרופה אחרת הנקראת מתוטרקסט עבור:
- הפחת את הסימנים והתסמינים של המחלה.
- האט את הנזק לעצמות ולמפרקים.
- שיפור התפקוד הגופני.
דלקת מפרקים פסוריאטית
דלקת מפרקים פסוריאטית היא מחלת מפרקים דלקתית, המלווה בדרך כלל בפסוריאזיס, מחלת עור דלקתית. אם יש לך דלקת מפרקים פסוריאטית פעילה, תחילה תטופל בתרופות אחרות. אם לא תגיב כראוי לתרופות אלו, תטופל בסימפוני. עבור:
- הפחת את הסימנים והתסמינים של המחלה.
- האט את הנזק לעצמות ולמפרקים.
- שיפור התפקוד הגופני.
ספונדיליטיס אנקילוזינג וספונדילוארתריטיס צירית לא רדיוגרפית
ספונדיליטיס אנקילוזינג וספונדילוארתריטיס צירית לא רדיוגרפית הינן מחלות דלקתיות בעמוד השדרה. אם יש לך ספונדיליטיס ankylosing או spondyloarthritis צירית לא רדיוגרפית, תחילה תטופל בתרופות אחרות. אם אינך מגיב כראוי לתרופות אלה, אתה תטופל באמצעות סימפוני ל:
- הפחת את הסימנים והתסמינים של המחלה.
- שיפור התפקוד הגופני.
קוליטיס כיבית
קוליטיס כיבית היא מחלת מעי דלקתית. אם יש לך קוליטיס כיבית תקבל תחילה תרופות אחרות. אם לא תגיב כראוי לתרופות אלו, תינתן לך סימפוני לטיפול במחלה שלך.
דלקת מפרקים אידיופטית לנוער רב -מפרקית
דלקת מפרקים אידיופטית לנוער פוליארטיקולרית הינה מחלה דלקתית הגורמת לכאבים ולנפיחות במפרקים אצל ילדים. אם לילדכם יש דלקת מפרקים אידיופטית לנוער רב -מפרקי, לילד תינתן תחילה תרופות אחרות. אם ילדך אינו מגיב כראוי לתרופות אלו, תינתן לילדך סימפוני בשילוב עם מתוטרקסט לטיפול במחלה.
התוויות נגד כאשר אין להשתמש ב- Simponi
אין להשתמש בסימפוני:
- אם אתה אלרגי (רגיש) לגולימומאב או לכל אחד ממרכיבי התרופה האחרים (רשום בסעיף 6).
- אם יש לך שחפת (TB) או כל זיהום חמור אחר.
- אם יש לך אי ספיקת לב בינונית או חמורה.
אם אינך בטוח אם כל התנאים לעיל חלים עליך, דבר עם הרופא, הרוקח או האחות לפני השימוש ב- Simponi.
אמצעי זהירות לשימוש מה שאתה צריך לדעת לפני נטילת סימפוני
שוחח עם הרופא, הרוקח או האחות לפני השימוש ב- Simponi.
זיהומים
ספר לרופא שלך מיד אם כבר היו לך סימפטומים של זיהום במהלך או לאחר הטיפול ב- Simponi. סימפטומים של זיהום כוללים חום, שיעול, קוצר נשימה, תסמינים דמויי שפעת, שלשולים, פצעים, בעיות שיניים או תחושת צריבה בעת מתן שתן.
- אתה יכול לקבל זיהומים ביתר קלות באמצעות Simponi.
- זיהומים יכולים להתקדם מהר יותר ולהיות חמורים יותר. כמו כן, זיהומים מהעבר יכולים לחזור.
שחפת (שחפת)
ספר לרופא שלך מיד אם אתה מבחין בסימפטומים של שחפת במהלך הטיפול. התסמינים של שחפת כוללים שיעול מתמשך, ירידה במשקל, תחושת עייפות, חום או הזעות לילה.
- מספר מקרים של שחפת דווחו בחולים שטופלו ב- Simponi, במקרים נדירים אפילו בחולים שטופלו בתרופות לטיפול בשחפת. הרופא שלך יבצע בדיקות כדי לבדוק אם יש לך שחפת. הרופא ירשום את הבדיקות הללו בכרטיס ההתראה של המטופל.
- חשוב מאוד שתודיע לרופא אם חלת בשחפת בעבר, או אם הגעת למגע הדוק עם מישהו שחלה או חווה שחפת.
- אם הרופא שלך חושב שאתה בסיכון לשחפת, ייתכן שתטופל בתרופות נגד שחפת לפני שתקבל סימפוני.
וירוס הפטיטיס B (HBV)
- דווח לרופא אם אתה נשא או סובל מהפטיטיס B או שהיה לך לפני שתקבל סימפוני
- ספר לרופא אם אתה חושב שאתה עלול להיות בסיכון לחלות בהפטיטיס B.
- הרופא שלך צריך להעריך אם יש לך הפטיטיס B.
- טיפול בחוסמי TNF כגון סימפוני יכול לגרום לנגיף הפטיטיס B להיות מופעל מחדש בחולים הנושאים וירוס זה, אשר במקרים מסוימים עלול לגרום למוות.
זיהומים פטרייתיים פולשניים
ספר לרופא שלך מיד אם אתה גר או טיילת באזור בו שכיחות זיהומים הנגרמים על ידי סוגים מסוימים של פטריות שיכולים להשפיע על הריאות או על חלקים אחרים של הגוף (הנקראים היסטופלסמוזיס, coccidioidomycosis או blastomycosis). שאל את הרופא אם אתה לא יודע אם זיהומים פטרייתיים אלה שכיחים באזור בו התגוררת או טיילת.
סרטן ולימפומה
ספר לרופא אם יש לך או סבל ממחלת לימפומה (סוג של סרטן דם) או סוגים אחרים של סרטן לפני שניתן לך סימפוני.
- אם אתה משתמש ב- Simponi או בחוסמי TNF אחרים אתה עלול להגדיל את הסיכון לפתח לימפומה או סוג אחר של סרטן.
- חולים עם דלקת מפרקים שגרונית קשה או מצבים דלקתיים אחרים שסבלו ממחלה זו זמן רב עשויים להיות בעלי סיכון גבוה מהממוצע לפתח לימפומה.
- סרטן, כולל סרטן חריג, לפעמים קטלני, דווחו בקרב ילדים וחולים המתבגרים הנוטלים תרופות חוסמות TNF.
- במקרים נדירים נצפתה סוג ספציפי וחמור של לימפומה הנקראת לימפומה של תאי T hepatosplenic בחולים הנוטלים חוסמי TNF אחרים. רוב החולים היו בני נוער או צעירים מבוגרים. צורה זו של סרטן הביאה בדרך כלל למוות. כמעט כל החולים האלה קיבלו גם תרופות הידועות בשם azathioprine או 6-mercaptopurine. ספר לרופא אם אתה נוטל אזתיופרין או 6-מרקפטופורין עם סימפוני.
- חולים עם אסתמה מתמשכת קשה, מחלת ריאות חסימתית כרונית (COPD) או מעשנים כבדים עשויים להיות בעלי סיכון מוגבר לסרטן בעזרת טיפול סימפוני. אם יש לך אסתמה מתמשכת חמורה, COPD או שאתה מעשן כבד, עליך לדון עם הרופא שלך האם טיפול עם חוסם TNF מתאים.
- חלק מהחולים שטופלו ב- golimumab פיתחו סוגים מסוימים של סרטן עור. אם אתה חווה שינוי כלשהו במראה העור או בגידולים בעור במהלך הטיפול או לאחריו, אנא פנה לרופא.
אִי סְפִיקַת הַלֵב
ספר לרופא שלך מיד אם אתה מבחין בסימפטומים חדשים או מחמירים של אי ספיקת לב. תסמינים של אי ספיקת לב כוללים קוצר נשימה או נפיחות בכפות הרגליים.
- דווח על מקרים של התפרצות חדשה או החמרה באי ספיקת לב עם חוסמי TNF, כולל סימפוני. חלק מהחולים האלה מתו.
- אם יש לך אי ספיקת לב קלה ואתה מטופל עם סימפוני, הרופא שלך יעקוב אחריך.
מחלת מערכת העצבים
ספר לרופא שלך מיד אם אובחנת אי פעם עם תסמונת של מחלת demyelinating, או כגון טרשת נפוצה. התסמינים עשויים לכלול שינויים בראייה, חולשה בזרועות וברגליים, קהות או עקצוצים בכל חלק בגוף. הרופא שלך יחליט אם עליך ליטול סימפוני.
פעולות או הליכים דנטליים
- ספר לרופא אם אתה עומד לבצע פעולות או הליכים דנטליים.
- ספר לרופא המנתח או לרופא השיניים המבצע את ההליך שאתה מטופל עם סימפוני על ידי הצגת כרטיס ההתראה של המטופל.
מחלות אוטואימוניות
ספר לרופא אם אתה מפתח תסמינים של מחלה הנקראת זאבת. התסמינים כוללים פריחה מתמשכת, חום, כאבי פרקים ועייפות.
- במקרים נדירים, אנשים שטופלו בחוסמי TNF פיתחו זאבת.
מחלות הדם
בחלק מהחולים, הגוף עלול שלא לייצר מספיק תאי דם המסייעים לגוף להילחם בזיהומים או לסייע להפסיק דימום. אם יש לך חום מתמשך שאינך מבין, חבורה או דימום קל או נראה חיוור, פנה לרופא מיד.הרופא שלך עשוי להחליט להפסיק את הטיפול.
אם אינך בטוח אם כל התנאים לעיל חלים עליך, דבר עם הרופא או הרוקח לפני השימוש ב- Simponi.
חיסונים
ספר לרופא אם חוסנת לאחרונה או שאתה מתכוון להתחסן.
- אסור לך לקבל חיסונים (חיים) מסוימים בזמן שאתה מטופל ב- Simponi.
- כמה חיסונים עלולים לגרום לזיהומים. אם קיבלת סימפוני בהריון, ייתכן שלתינוקך יש סיכון מוגבר ללקות בזיהום זה במשך כחצי שנה לאחר המנה האחרונה שהתקבלה במהלך ההריון. חשוב ליידע את רופא הילדים שלך ואנשי מקצוע בתחום הבריאות על השימוש ב- Simponi. יכול להחליט מתי הילד צריך לקבל חיסונים כלשהם.
שוחח עם הרופא של ילדך בנוגע לחיסונים לילדך. במידת האפשר, ילדך צריך להיות מעודכן בכל החיסונים לפני השימוש ב- Simponi.
גורמים טיפוליים זיהומיים
שוחח עם הרופא שלך אם נטלת לאחרונה או מתכנן לקחת טיפול באמצעות חומר טיפולי זיהומי (כגון החדרת BCG המשמשת לטיפול בסרטן).
תגובות אלרגיות
ספר לרופא מיד אם אתה מפתח תסמינים של תגובה אלרגית לאחר הטיפול ב- Simponi. סימפטומים של תגובה אלרגית עשויים לכלול נפיחות בפנים, בשפתיים, בפה או בגרון שעלולות לגרום לקשיי בליעה או נשימה, פריחות בעור, כוורות, נפיחות בידיים, ברגליים ובקרסוליים.
- חלק מהתגובות הללו עלולות להיות קשות או לעיתים רחוקות מסכנות חיים.
- חלק מהתגובות הללו מתרחשות לאחר הניהול הראשון של סימפוני.
ילדים ומתבגרים
סימפוני אינו מומלץ לילדים השוקלים פחות מ -40 ק"ג עם דלקת מפרקים אידיופטית לנוער רב -מפרקית או לילדים ומתבגרים מתחת לגיל 18 לכל מצב אחר.
אינטראקציות אילו תרופות או מזונות יכולים לשנות את ההשפעה של סימפוני
- ספר לרופא או לרוקח שלך אם אתה נוטל, נטלת לאחרונה או עשוי ליטול תרופות אחרות, כולל תרופות אחרות לטיפול בדלקת מפרקים שגרונית, דלקת מפרקים אידיופטית לנוער רב-מפרקית, דלקת מפרקים פסוריאטית, ספונדיליטיס אנקילוזינג, דלקת צירית spondyloarthritis לא רדיוגרפית או קוליטיס כיבית.
- אתה לא צריך לקחת Simponi עם תרופות המכילות את החומר הפעיל anakinra או abatacept. תרופות אלו משמשות לטיפול במחלות ראומטיות.
- ספר לרופא או לרוקח אם אתה נוטל תרופות אחרות המשפיעות על המערכת החיסונית.
- לא ניתן לטפל בה בחיסונים (חיים) מסוימים בזמן השימוש בסימפוני.
אם אינך בטוח אם כל התנאים לעיל חלים עליך, דבר עם הרופא או הרוקח לפני השימוש ב- Simponi.
אזהרות חשוב לדעת כי:
הריון והנקה
שוחח עם הרופא שלך לפני השימוש בסימפוני אם:
- את בהריון או מתכננת להיכנס להריון בעת השימוש בסימפוני. ההשפעות של תרופה זו בנשים בהריון אינן ידועות. השימוש Simponi בנשים בהריון אינו מומלץ. אם אתה אמור להיות מטופל ב- Simponi, עליך להימנע מהריון על ידי שימוש באמצעי מניעה נאותים במהלך הטיפול ולפחות 6 חודשים לאחר הזרקת Simponi האחרונה שלך.
- לפני ההנקה, הטיפול האחרון בסימפוני חייב להיות לפחות 6 חודשים קודם לכן. עליך להפסיק להניק אם תינתן לך סימפוני.
- אם קיבלת סימפוני במהלך ההריון, ייתכן שלתינוקך יש סיכון מוגבר ללקות בזיהום. חשוב לספר לרופא הילדים ולאנשי מקצוע בתחום הבריאות על השימוש שלך בסימפוני לפני שהתינוק שלך יקבל חיסונים (למידע נוסף ראו את הסעיף בנושא חיסונים).
אם הינך בהריון או מניקה, חושבת שאת בהריון או מתכננת ללדת, פנה לייעוץ מהרופא או הרוקח לפני נטילת התרופה.
נהיגה ושימוש במכונות
סימפוני עלול לפגוע מעט ביכולת הנהיגה והשימוש בכלים או במכונות. אתה עלול להרגיש סחרחורת לאחר השימוש ב- Simponi. במקרה זה אין לנהוג או להשתמש בכלים או מכונות.
סימפוני מכיל לטקס וסורביטול
רגישות לטקס
רגישות לטקס חלק אחד של העט הממולא, המכסה המכסה את המחט, מכיל לטקס. מאחר ולטקס יכול לגרום לתגובות אלרגיות קשות, דווח לרופא לפני השימוש בסימפוני, אם אתה או המטפל שלך אלרגיים לטקס.
חוסר סובלנות לסורביטול
סימפוני מכיל סורביטול (E420). אם אמרו לך הרופא כי יש לך "אי סבילות לסוכרים מסוימים, פנה לרופא לפני נטילת התרופה.
מינון ושיטת השימוש אופן השימוש בסימפוני: מינון
השתמש תמיד בתרופה זו בדיוק כפי שהרופא או הרוקח אמרו לך. אם יש לך ספק, עליך לפנות לרופא או לרוקח.
כמה נותנים סימפוני
דלקת מפרקים שגרונית, דלקת מפרקים פסוריאטית וספונדילוארתריטיס צירית, כולל ספונדיליטיס אנקילוזינג וספנדילוארתריטיס צירית לא רדיוגרפית:
- המינון המומלץ הוא 50 מ"ג (התוכן של עט אחד מלא) הניתן פעם בחודש, באותו היום בכל חודש.
- שוחח עם הרופא שלך לפני נטילת המנה הרביעית. הרופא שלך יחליט אם להמשיך את הטיפול ב- Simponi.
- אם אתה שוקל יותר מ -100 ק"ג, ניתן להגדיל את המינון ל -100 מ"ג (התוכן של 2 עטים מלאים מראש), שניתן פעם בחודש, תמיד באותו היום בכל חודש.
דלקת פרקים אידיופטית לנוער:
- המינון המומלץ הוא 50 מ"ג הניתן פעם בחודש, באותו היום בכל חודש.
- שוחח עם הרופא של ילדך לפני שילדך לוקח את המנה הרביעית. הרופא של ילדכם יחליט אם להמשיך את הטיפול בסימפוני.
קוליטיס כיבית
- הטבלה להלן מראה כיצד תשתמש בדרך כלל בתרופה זו.
- בחולים ששוקלים פחות מ -80 ק"ג, 50 מ"ג (התוכן של עט אחד מלא) 4 שבועות לאחר הטיפול האחרון שלך, ולאחר מכן כל 4 שבועות לאחר מכן.
- בחולים במשקל 80 ק"ג ומעלה, 100 מ"ג (תוכן 2 עטים מלאים מראש) 4 שבועות לאחר הטיפול האחרון, ולאחר מכן כל 4 שבועות לאחר מכן.
כיצד ניתן סימפוני
- סימפוני ניתנת בהזרקה מתחת לעור (תת עורית).
- בהתחלה הרופא או הצוות הסיעודי יזריקו סימפוני, אולם אתה והרופא שלך עשויים להחליט שאתה יכול להזריק סימפוני בעצמך, במקרה זה תקבל הדרכה כיצד להזריק סימפוני בעצמך.
שוחח עם הרופא שלך אם יש לך שאלות בנוגע לניהול עצמי של זריקה. בסוף עלון זה תמצא "הוראות ניהול" מפורטות.
אם שכחת להשתמש בסימפוני
אם שכחת להשתמש ב- Simponi ביום שנקבע, הזרק את המנה החמיצה ברגע שאתה זוכר.
אין להשתמש במינון כפול כדי לפצות על מנה שנשכחה.
מתי להזריק את המנה הבאה:
- אם איחרת פחות משבועיים, הזריק את המנה החמיצה ברגע שתזכור ותמשיך לעקוב אחר לוח הזמנים המקורי שלך.
- אם איחרת יותר משבועיים, הזריק את המינון שנשכח ברגע שאתה זוכר וספר לרופא או לרוקח ושאל מתי עליך ליטול את המנה הבאה.
אם אינך בטוח מה לעשות, שאל את הרופא, הרוקח או האחות שלך.
אם תפסיק להשתמש בסימפוני
אם אתה שוקל להפסיק את סימפוני, דבר עם הרופא או הרוקח תחילה.
אם יש לך שאלות נוספות לגבי השימוש בתרופה זו, פנה לרופא או לרוקח.
מנת יתר מה לעשות אם נטלת יותר מדי סימפוני
אם השתמשת או נתת יותר מדי סימפוני (הזרקת יותר מדי במנה אחת, או השתמשת בה לעתים קרובות מדי), דווח לרופא או לרוקח מיד. קח תמיד את הקרטון החיצוני ואת העלון הזה, גם אם הוא ריק.
תופעות לוואי מהן תופעות הלוואי של סימפוני
כמו כל התרופות, תרופה זו עלולה לגרום לתופעות לוואי, אם כי לא כולם מקבלים אותן. חלק מהחולים עלולים לחוות תופעות לוואי חמורות אשר עשויות לדרוש טיפול רפואי. הסיכון לחלק מתופעות הלוואי גבוה יותר במינון של 100 מ"ג בהשוואה למינון של 50 מ"ג. תופעות לוואי עלולות להתרחש גם מספר חודשים לאחר הזריקה האחרונה.
ספר לרופא מיד אם אתה מבחין באחת מתופעות הלוואי החמורות הבאות של סימפוני הכוללות:
- תגובות אלרגיות שעלולות להיות קשות, או לעתים רחוקות, מסכנות חיים (נדירות).סימפטומים של תגובה אלרגית עשויים לכלול נפיחות בפנים, בשפתיים, בפה או בגרון שעלולות לגרום לקשיי בליעה או נשימה, פריחות בעור, כוורות, נפיחות בידיים, ברגליים או בקרסוליים. חלק מהתגובות הללו התרחשו לאחר הניהול הראשון של סימפוני.
- זיהומים חמורים (כולל שחפת, זיהומים חיידקיים כולל זיהומים חמורים בדם ודלקת ריאות, זיהומים פטרייתיים חמורים וזיהומים אופורטוניסטיים אחרים) (שכיח). סימפטומים של זיהום עשויים לכלול חום, עייפות, שיעול (מתמשך), קוצר נשימה, תסמינים דמויי שפעת, ירידה במשקל, הזעות לילה, שלשולים, פצעים, בעיות שיניים ותחושת צריבה בעת מתן שתן.
- הפעלה מחדש של וירוס הפטיטיס B אם אתה נשא או שחלת בעבר בהפטיטיס B (נדיר). התסמינים עשויים לכלול הצהבה של העור והעיניים, שתן חום כהה, כאבים בצד ימין של הבטן, חום, תחושת לא טוב, חולשה ותחושת עייפות רבה.
- מחלת מערכת העצבים כגון טרשת נפוצה (נדירה). סימפטומים של מחלת מערכת העצבים עשויים לכלול שינויים בראייה, חולשה בזרועות או ברגליים, קהות או עקצוצים בכל חלק בגוף.
- סרטן בלוטות הלימפה (לימפומה) (נדיר). סימפטומים של לימפומה יכולים לכלול בלוטות לימפה נפוחות, ירידה במשקל או חום.
- אי ספיקת לב (נדיר). תסמינים של אי ספיקת לב יכולים לכלול קוצר נשימה או נפיחות בכפות הרגליים.
- סימנים להפרעות במערכת החיסון הנקראות: - זאבת (נדירה). התסמינים עשויים לכלול כאבי פרקים או פריחה בלחיים או בזרועות הרגישות לשמש. - סרקואידוזיס (נדיר). התסמינים עשויים לכלול שיעול מתמשך, קוצר נשימה, כאבים בחזה, חום, בלוטות לימפה נפוחות, ירידה במשקל, פריחות בעור וראייה מטושטשת.
- נפיחות של כלי דם קטנים (וסקוליטיס) (נדיר). התסמינים עשויים לכלול חום, כאבי ראש, ירידה במשקל, הזעות לילה, פריחה ובעיות עצבים כגון קהות ועקצוצים.
- סרטן העור (נדיר). תסמיני סרטן העור עשויים לכלול שינויים במראה העור או בצמיחות על העור.
- מחלת דם (נפוצה). סימפטומים של מחלת דם עשויים לכלול חום שאינו חולף, נטייה חזקה לחבורות או לדמם או מראה חיוור מאוד.
- סרטן הדם (לוקמיה) (נדיר). סימפטומים של לוקמיה יכולים לכלול חום, תחושת עייפות, זיהומים תכופים, חבורות והזעות לילה.
ספר לרופא שלך מיד אם אתה מבחין באחד מהתסמינים המפורטים לעיל.
תופעות הלוואי הנוספות הבאות נצפו עם סימפוני:
תופעות לוואי שכיחות מאוד (עשויות להשפיע על יותר מ -1 מתוך 10 אנשים):
- דלקות בדרכי הנשימה העליונות, כאב גרון או צרידות, קור
תופעות לוואי שכיחות (עשויות להשפיע על עד 1 מתוך 10 אנשים):
- בדיקות כבד חריגות (אנזימי כבד מוגברים), שנמצאו במהלך בדיקות דם שנעשו על ידי הרופא שלך
- סחרחורת
- כְּאֵב רֹאשׁ
- תחושת קהות או עקצוצים
- זיהומים פטרייתיים שטחיים
- מוּרְסָה
- זיהומים חיידקיים (כגון צלוליטיס)
- הפחתת כדוריות הדם האדומות
- בדיקת דם חיובית של זאבת
- תגובות אלרגיות
- קִלקוּל קֵבָה
- כאב בטן
- תחושת בחילה (בחילה)
- לְהַשְׁפִּיעַ
- בְּרוֹנכִיטִיס
- דלקת סינוסים
- הרפס בפנים
- לחץ דם גבוה
- חום
- אסטמה, קוצר נשימה, צפצופים
- הפרעות בקיבה ובמעיים הכוללות דלקת בפנים הקיבה והמעי הגס העלולות לגרום לחום
- כאבים וכיבים בפה
- תגובות באתר ההזרקה (כולל אדמומיות, קשיות, כאבים, חבורות, גירוד, עקצוץ וגירוי)
- איבוד שיער
- פריחה ועור מגרד
- קשיי שינה
- דִכָּאוֹן
- תחושת חולשה
- שברים בעצמות
- כאב בחזה
תופעות לוואי לא שכיחות (עשויות לפגוע בעד אחד מכל 100 אנשים):
- זיהום בכליות
- סרטן, כולל סרטן העור וגושים לא סרטניים או המונים קטנים, כולל שומות
- שלפוחיות עור
- פסוריאזיס (כולל כפות הידיים ו / או כפות הרגליים ו / או בצורה של פוסטולות עור)
- הפחתת טסיות דם
- הפחתת כדוריות הדם הלבנות
- הפחתה משולבת של טסיות דם, כדוריות דם אדומות ותאי דם לבנים
- הפרעות בבלוטת התריס
- עלייה ברמות הסוכר בדם
- עלייה ברמות הכולסטרול בדם
- הפרעות שיווי משקל
- הפרעות ראייה
- תחושה של דופק לא סדיר
- צמצום כלי הדם בלב
- קרישי דם
- אוֹדֶם
- עצירות
- דלקת כרונית של הריאות
- חומצה ריפלוקס
- אבנים במרה
- בעיות בכבד
- הפרעות בחזה
- הפרעות במחזור החודשי
תופעות לוואי נדירות (עשויות להשפיע על עד 1 מתוך 1,000 אנשים):
- חוסר יכולת של מח העצם לייצר תאי דם
- זיהום במפרקים או ברקמות שמסביב
- ריפוי קשה
- דלקת בכלי הדם של האיברים הפנימיים
- לוקמיה
- מלנומה (סוג של סרטן העור)
- עור מתקלף
- הפרעות אימונולוגיות שיכולות להשפיע על הריאות, העור ובלוטות הלימפה (נפוצות מאוד כסרקואידוזיס)
- כאב ושינוי צבע באצבעות או בהונות
- הפרעות טעם
- הפרעות בשלפוחית השתן
- בעיות כליה
- דלקת בכלי הדם בעור הגורמת לפריחה
תופעות לוואי עם תדירות לא ידועות:
- קרצינומה של תאי מרקל (סוג של סרטן העור)
- סרטן דם נדיר הפוגע בעיקר בצעירים (לימפומה של תאי T hepatosplenic)
דיווח על תופעות לוואי
אם אתה נתקל בתופעות לוואי כלשהן, שוחח עם הרופא, הרוקח או האחות שלך. זה כולל את כל תופעות הלוואי האפשריות שאינן מופיעות בעלון זה. תוכל גם לדווח על תופעות לוואי ישירות באמצעות מערכת הדיווח הלאומית הרשומה בנספח V. תופעות לוואי תוכל לעזור לספק מידע נוסף על בטיחות התרופה.
תפוגה ושמירה
- שמור את התרופה הרחק מעיני ילדים.
- אין להשתמש בתרופה זו לאחר תאריך התפוגה אשר מצוין על התווית והקרטון לאחר "EXP". תאריך התפוגה מתייחס ליום האחרון של אותו חודש.
- שומרים במקרר (2 ° C-8 ° C). אל תקפא.
- שמור את העט המלא בקרטון החיצוני כדי להגן על התרופה מפני אור.
- אין להשתמש בתרופה אם אתה מבחין כי הנוזל אינו בהיר עד צהוב בהיר, הוא עכור או מכיל חלקיקים זרים.
- אין לזרוק תרופות דרך שפכים או פסולת ביתית. שאל את הרופא או הרוקח כיצד עליך לזרוק תרופות שאינך משתמש בהן יותר. הדבר יעזור להגן על הסביבה.
מידע אחר
מה מכיל סימפוני
המרכיב הפעיל הוא golimumab. עט אחד של 0.5 מ"ל מלא מראש מכיל 50 מ"ג גולימומאב.
המרכיבים הנוספים הם סורביטול (E420), L-histidine, L-histidine monohydrochloride מונוהידראט, פוליסורבט 80 ומים לזריקות.
סימפוני נראה ותוכן האריזה
סימפוני מסופק כפתרון להזרקה בעט מלא חד פעמי. ניתן להשיג את Simponi באריזות המכילות עט אחד ומילוי המכילים 3 (3 אריזות של 1) עטים מלאים מראש. לא כל גודל האריזה עשוי להיות משווק.
הפתרון ברור עד מעט סמיך (מבריק כמו פנינה), חסר צבע עד צהוב בהיר ויכול להכיל חלקיקי חלבון קטנים שקופים או לבנים. אין להשתמש ב- Simponi אם הפתרון שינה את צבעו, עכור או אם הוא מכיל חלקיקים זרים גלויים.
עלון המקור: AIFA (סוכנות התרופות האיטלקית). תוכן שפורסם בינואר 2016. ייתכן שהמידע הנוכחי אינו מעודכן.
כדי לקבל גישה לגרסה העדכנית ביותר, מומלץ לגשת לאתר AIFA (סוכנות התרופות האיטלקית). כתב ויתור ומידע שימושי.
01.0 שם התרופה
פתרון הזרקת סימפוני 50 מג
02.0 הרכב איכותי וכמותי
פתרון סימפוני 50 מ"ג להזרקה בעט מלא מראש
עט אחד של 0.5 מ"ל מלא מכיל 50 מ"ג golimumab *.
פתרון סימפוני 50 מ"ג להזרקה במזרק מלא
מזרק אחד הממלא 0.5 מ"ל מכיל 50 מ"ג גולימומאב *.
* נוגדן חד שבטי אנושי מסוג IgG1? מיוצר מקו תאים היברידומה עכברים בטכנולוגיית DNA רקומביננטי.
חומר עזר בעל השפעה ידועה:
כל עט מלא מכיל: 20.5 מ"ג סורביטול למינון של 50 מ"ג.
כל מזרק מלא מכיל: 20.5 מ"ג סורביטול למינון של 50 מ"ג.
לרשימת החומרים המלאים, ראה סעיף 6.1.
03.0 טופס פרמצבטי
פתרון להזרקה בעט מלא (הזרקה), SmartJect
פתרון להזרקה במזרק מלא (הזרקה)
הפתרון ברור עד מעט סמיך, חסר צבע עד צהוב בהיר.
04.0 מידע קליני
04.1 אינדיקציות טיפוליות
דלקת מפרקים שגרונית (RA)
סימפוני, בשילוב עם מתוטרקסט (MTX), מיועדת ל:
• הטיפול בדלקת מפרקים שגרונית פעילה בינונית עד חמורה בחולים מבוגרים כאשר התגובה לתרופות אנטי-ראומטיות המשנות מחלות, כולל MTX, לא הייתה מספקת.
• טיפול בדלקת מפרקים שגרונית חמורה, פעילה ומתקדמת במבוגרים שטרם טופלו ב- MTX.
הוכח כי סימפוני, בשיתוף עם MTX, מפחית את קצב התקדמות הנזק המשותף הנמדד על ידי צילומי רנטגן ומשפר את התפקוד הגופני.
דלקת פרקים אידיופטית לנוער
דלקת מפרקים אידיופטית לנוער פוליארטיקולרית (PIA)
סימפוני בשילוב עם MTX מיועדת לטיפול בדלקת מפרקים אידיופטית לנוער רב -מפרקית בילדים במשקל של 40 ק"ג לפחות שהגיבו בצורה לא מספקת לטיפול MTX קודם.
דלקת מפרקים פסוריאטית (AP)
סימפוני, לבד או בשילוב עם מתוטרקסט (MTX), מיועד לטיפול בדלקת מפרקים פסוריאטית פעילה ומתקדמת במבוגרים כאשר התגובה לטיפולים קודמים ב- DMARD לא הייתה מספקת. הוכח כי סימפוני מפחית את קצב התקדמות התרופה. נזק למפרקים היקפיים, כפי שנמדד על ידי צילומי רנטגן בחולים עם תת-סוגים סימטריים של מחלות פוליארטיקולריות (ראה סעיף 5.1) ולשיפור התפקוד הגופני.
ספונדילוארתריטיס צירית
ספונדיליטיס אנקילוזינג (AS)
סימפוני מיועדת לטיפול בספונדיליטיס ספונדיליטיס חמורה ופעילה אצל מבוגרים שלא הגיבו כראוי לטיפולים קונבנציונליים.
ספונדילוארתריטיס צירית לא רדיוגרפית (מספר צירי צירי)
סימפוני מיועדת לטיפול בחולים מבוגרים עם ספונדי-ארתריטיס אקסיאלית אקטיבית שאינה רדיוגרפית עם סימנים אובייקטיביים לדלקת כפי שמעידים עלייה מוגברת ב- C-reactive protein (CRP) ו / או דימות תהודה מגנטית (MRI). או שאינם סובלים לתרופות נוגדות דלקת לא סטרואידיות (NSAIDs).
קוליטיס כיבית (CU)
סימפוני מיועד לטיפול בקוליטיס כיבית פעילה בינונית עד חמורה בחולים מבוגרים שלא הגיבו כראוי לטיפול קונבנציונאלי, כולל סטרואידים ו -6 מרקפטופורין (6 MP) או אזתיופרין (AZA), או שאינם סובלים או שיש להם התווית נגד רפואית לטיפולים אלה.
04.2 מינון ושיטת הניהול
יש להתחיל ולפקח על טיפול סימפוני על ידי רופאים מומחים המנוסים באבחון וטיפול בדלקת מפרקים שגרונית, דלקת מפרקים אידיופטית לנוער רב-מפרקית, דלקת מפרקים פסוריאטית, ספונדיליטיס אנקלוזינג, ספונדילוארתריטיס צירית לא רדיוגרפית או קוליטיס כיבית. כַּרְטִיס.
מִנוּן
דלקת מפרקים שגרונית
סימפוני 50 מ"ג ניתנת פעם בחודש, באותו היום בכל חודש.
יש לנהל סימפוני במקביל ל- MTX.
דלקת מפרקים פסוריאטית, ספונדיליטיס ankylosing או spondyloarthritis צירית לא רדיוגרפית
סימפוני 50 מ"ג ניתנת פעם בחודש, באותו היום בכל חודש.
לגבי כל האינדיקציות לעיל, הנתונים הזמינים מצביעים על כך שתגובה קלינית מושגת בדרך כלל תוך 12-14 שבועות מתחילת הטיפול (לאחר 3-4 מנות). יש לשקול המשך טיפול בחולים שאינם מראים עדות לתועלת טיפולית. במסגרת הזמן הזו.
חולים במשקל גוף העולה על 100 ק"ג
עבור כל האינדיקציות הנ"ל, בחולים עם RA, AP, SA או Axial SpA nr במשקל של יותר מ -100 ק"ג, שאינם משיגים תגובה קלינית מספקת לאחר 3 או 4 מנות, עלייה במינון golimumab עד 100 מ"ג. אחת לחודש, בהתחשב בסיכון המוגבר לתגובות שליליות חמורות של תרופות במינון של 100 מ"ג בהשוואה למינון של 50 מ"ג (ראה סעיף 4.8). יש לשקול המשך טיפול בחולים שאינם מראים עדות לתועלת טיפולית לאחר קבלת 3- 4 מנות משלימות של 100 מ"ג.
קוליטיס כיבית
חולים עם משקל גוף של פחות מ 80 ק"ג
סימפוני ניתן במינון התחלתי של 200 מ"ג, ואחריו 100 מ"ג בשבוע 2, ולאחר מכן 50 מ"ג כל 4 שבועות לאחר מכן (ראה סעיף 5.1).
חולים עם משקל גוף גדול או שווה ל -80 ק"ג
סימפוני ניתן במינון התחלתי של 200 מ"ג, ואחריו 100 מ"ג בשבוע 2, ולאחר מכן 100 מ"ג כל 4 שבועות לאחר מכן (ראה סעיף 5.1).
במהלך טיפול תחזוקה ניתן להפחית בהדרגה את סטרואידים בהתאם להנחיות הפרקטיקה הקלינית.
נתונים זמינים מצביעים על כך שתגובה קלינית מושגת בדרך כלל תוך 12-14 שבועות מהטיפול (לאחר 4 מנות). יש לשקול המשך טיפול בחולים שאינם מראים עדויות לתועלת טיפולית בתוך פרק זמן זה.
מינון חסר
אם מטופל שוכח להזריק סימפוני ביום המתוכנן, יש להזריק את המינון החסר ברגע שהחולה זוכר. יש להנחות את המטופלים שלא להזריק מנה כפולה כדי לפצות על מנה שנשכחה.
יש לתת את המנה הבאה על פי המדריך הבא:
• אם המינון המתעכב הוא פחות משבועיים, המטופל צריך להזריק את המינון החמיץ ולהמשיך לעקוב אחר לוח הזמנים המקורי שלו.
• אם העיכוב במינון הוא יותר משבועיים, על המטופל להזריק את המינון החמיץ ויהיה צורך להגדיר לוח מינון חדש ממועד הזריקה.
אוכלוסיות מיוחדות
קשיש (≥ 65 שנים)
אין צורך בהתאמת מינון אצל קשישים.
ליקוי כלייתי וכבד
סימפוני לא נחקר באוכלוסיות חולים אלו. לא ניתן להמליץ על מינון.
אוכלוסיית ילדים
הבטיחות והיעילות של סימפוני בחולים מתחת לגיל 18 לאינדיקציות שאינן pIA לא נקבעו.
דלקת מפרקים אידיופטית לנוער רב -מפרקית
סימפוני 50 מ"ג ניתנת פעם בחודש, באותו יום בכל חודש, לילדים עם משקל גוף של 40 ק"ג לפחות.
נתונים זמינים מצביעים על כך שתגובה קלינית מושגת בדרך כלל תוך 12-14 שבועות מהטיפול (לאחר 3-4 מנות). יש לשקול מחדש את המשך הטיפול בילדים שאינם מראים עדות לתועלת טיפולית בתוך פרק זמן זה.
שיטת ניהול
סימפוני מיועד לשימוש תת עורי. לאחר הכשרה נאותה בטכניקת ההזרקה התת עורית, יוכלו המטופלים להזריק לעצמו סימפוני אם הרופא שלהם קובע שהם מסוגלים, תוך השגחה רפואית מתאימה במידת הצורך. יש להנחות את המטופלים להזריק את מלוא כמות סימפוני בהתאם להוראות הניהול המלאות המופיעות בעלון. אם יש צורך בזריקות מרובות, יש לבצע את הזריקות באתרי גוף שונים.
להוראות ניהול, ראה סעיף 6.6.
04.3 התוויות נגד
רגישות יתר לחומר הפעיל או לכל אחד מהחומרים המצוינים בסעיף 6.1.
שחפת פעילה (שחפת) או זיהומים חמורים אחרים כגון אלח דם וזיהומים אופורטוניסטיים (ראה סעיף 4.4).
חולים עם אי ספיקת לב בינונית עד חמורה (NYHA Class III / IV - New York Heart Association) (ראה סעיף 4.4).
04.4 אזהרות מיוחדות ואמצעי זהירות מתאימים לשימוש
זיהומים
לפני, במהלך ואחרי הטיפול בסימפוני, יש לעקוב מקרוב אחר המטופלים לאיתור זיהומים כולל שחפת. מאחר שחיסול golimumab עשוי להימשך עד 5 חודשים, יש להמשיך במעקב במהלך תקופה זו. אין לתת טיפול נוסף בסימפוני אם מטופל מפתח זיהומים חמורים או אלח דם (ראה סעיף 4.3).
אסור להשתמש ב- Simponi בחולים עם זיהום פעיל, משמעותי מבחינה קלינית. יש להיזהר כאשר בוחנים את השימוש ב- Simponi בחולים עם זיהום כרוני או היסטוריה של זיהומים חוזרים. יש ליידע את המטופלים כראוי על הצורך להימנע מחשיפה לגורמי סיכון פוטנציאליים לזיהומים.
חולים הנוטלים תרופות חוסמות TNF נוטים יותר לזיהומים חמורים.
בחולים שטופלו ב- Simponi דווחו זיהומים חיידקיים (כולל אלח דם ודלקת ריאות), מיקובקטריאלי (כולל שחפת), זיהומים פטרייתיים פולשניים וזיהומים אופורטוניסטיים, כולל אלה עם תוצאה קטלנית. חלק מהזיהומים החמורים הללו התפתחו בחולים המטופלים בטיפול מקביל, אשר בנוסף למחלתם הבסיסית, עלולים לגרום להם לזיהומים. מטופלים המפתחים זיהום חדש בזמן הטיפול בסימפוני צריכים להיות במעקב קפדני ולעבור "הערכה אבחנתית קפדנית. יש להפסיק את הטיפול במתן סימפוני אם מטופל יפתח זיהום חמור חדש או אלח דם וטיפול" התחלתי ". מיקרוביאלית או אנטי פטרייתית עד להדבקה. למטופלים שגרו באזורים בהם נסעו או נסעו לאזורים שבהם זיהומים פטרייתיים פולשניים כגון היסטופלזמה, coccidioidomycosis או blastomycosis הם אנדמיים, יש לשקול היטב את היתרונות והסיכונים של טיפול סימפוני. לפני תחילת הטיפול ב- Simponi. בחולים בסיכון גבוה המטופלים עם סימפוני, יש לחשוד בזיהום פטרייתי פולשני אם הם מפתחים מחלה מערכתית קשה. במידת האפשר, האבחון והטיפול של טיפול אנטי פטרייתי אמפירי בחולים אלה צריכים להיעשות בהתייעצות עם רופא המנוסה בטיפול בחולים עם זיהומים פטרייתיים פולשניים.
שַׁחֶפֶת
מקרים של שחפת דווחו בחולים שטופלו ב- Simponi. יש לציין כי ברוב המקרים הללו מדובר בשחפת חוץ -ריאתית, מקומית ומפוזרת כאחד.
לפני תחילת הטיפול בסימפוני, יש להעריך את כל החולים הן לשחפת פעילה והן לא פעילה ("סמויה"). הערכה זו צריכה לכלול היסטוריה רפואית מפורטת הכוללת היסטוריה אישית של שחפת או מגע קודם אפשרי עם מקור לזיהום בשחפת וטיפול קודם ו / או מקביל. יש לבצע בדיקות אבחון מתאימות כגון עור שחפת או בדיקות דם וצילומי חזה בכל המטופלים (הנחיות מקומיות עשויות לחול). מומלץ לדווח על בדיקות אלו בכרטיס התראת המטופל. מרשמים נזכרים בסיכון לתוצאות בדיקת עור שחפת שלילית כוזבת, במיוחד בחולים חולים או חסרי פגיעה.
אם מאובחנת שחפת פעילה, אין להתחיל טיפול סימפוני (ראה סעיף 4.3).
אם יש חשד לשחפת סמויה, יש לפנות לרופא המנוסה בטיפול בשחפת. בכל המצבים המתוארים להלן, יש לשקול היטב את איזון התועלת / סיכון של טיפול סימפוני.
אם מאובחנת שחפת לא פעילה ("סמויה"), יש להתחיל בטיפול באנטי -שחפת לשחפת סמויה לפני תחילת הטיפול בסימפוני, בהתאם להנחיות המקומיות.
בחולים הסובלים מגורמי סיכון רבים או משמעותיים לשחפת ובעלי בדיקה שלילית לשחפת סמויה, יש לשקול טיפול נגד שחפת לפני תחילת סימפוני. יש לשקול גם שימוש בטיפול בשחפת לפני תחילת הטיפול בסימפוני ב. חולים עם היסטוריה קודמת של שחפת סמויה או פעילה שלא ניתן לאשר להם מהלך טיפול הולם.
מקרים של שחפת פעילה התרחשו בחולים שטופלו ב- Simponi במהלך הטיפול ואחריו לשחפת סמויה. יש לעקוב מקרוב אחר מטופלים המטופלים בסימפוני לאיתור סימנים ותסמינים של שחפת פעילה, כולל חולים שבדקו שלילי לגבי שחפת סמויה, מטופלים המטופלים בשחפת סמויה או חולים שטופלו בעבר בשחפת סמויה. "שחפת.
יש לייעץ לכל המטופלים לפנות לייעוץ רפואי אם מופיעים סימנים / תסמינים המעידים על שחפת (למשל שיעול מתמשך, בזבוז / ירידה במשקל, חום נמוך) במהלך או לאחר הטיפול בסימפוני.
הפעלה מחדש של וירוס הפטיטיס B
הפעלה מחדש של הפטיטיס B נצפתה בחולים שטופלו ב- TNF-antagonist, כולל סימפוני, ואשר היו נשאים כרוניים של וירוס זה (כלומר חיוביים לאנטיגן משטח). במקרים מסוימים התרחשו תוצאות קטלניות.
יש להעריך את המטופלים לגבי זיהום HBV לפני תחילת הטיפול ב- Simponi. לחולים הבודקים חיוביים לזיהום HBV, מומלץ להתייעץ עם רופא המנוסה בטיפול בהפטיטיס B.
יש לעקוב מקרוב אחר נשאי נגיף הפטיטיס B הדורש טיפול ב- Simponi לאיתור סימנים ותסמינים של זיהום וירוס הפטיטיס B במשך כל הטיפול ובמשך מספר חודשים לאחר סיום הטיפול. קיימים נתונים מספקים על חולים עם וירוס הפטיטיס B שטופלו בנגיף ויראלי. טיפול בשילוב עם טיפול אנטגוניסטי מסוג TNF למניעת הפעלה מחדש של נגיף הפטיטיס B. בחולים המפתחים הפעלה מחדש של וירוס הפטיטיס B יש להפסיק את הטיפול בסימפוני ולהתחיל בטיפול אנטי ויראלי יעיל עם טיפול תומך מתאים.
גידולים ממאירים ומחלות לימפופרוליפרטיביות
התפקיד הפוטנציאלי של טיפול במעכבי TNF בהתפתחות ממאירות אינו ידוע. בהתבסס על הידע הנוכחי, לא ניתן לשלול את הסיכון האפשרי להתפתחות לימפומה, לוקמיה או ממאירות אחרות בחולים שטופלו באנטגוניסט TNF. יש להיזהר כאשר בוחנים טיפול במעכבי TNF בחולים עם היסטוריה של ממאירות או בבחינת המשך טיפול בחולים המפתחים ממאירות.
גידולים ממאירים ילדים
מניסיון לאחר השיווק דווחו ממאירות, חלקן קטלניות, בקרב ילדים, מתבגרים וצעירים (עד גיל 22) שטופלו בחומרים חוסמי TNF (תחילת טיפול ≤ 18 שנים. כמחצית מהמקרים היו מקרים אחרים יוצגו על ידי מגוון ממאירים שונים וכללו ממאירות נדירות הקשורות בדרך כלל לדיכוי חיסוני. לא ניתן לשלול סיכון להתפתחות ניאופלזמות ממאירות אצל ילדים ובני נוער שטופלו במעכבי TNF.
לימפומה ולוקמיה
בשלבים מבוקרים של ניסויים קליניים עם כל התרופות מעכבות TNF, כולל סימפוני, נצפו מקרים נוספים של לימפומה בקרב מטופלים שקיבלו טיפול אנטי-TNF בהשוואה לחולי ביקורת. במהלך הניסויים הקליניים שלב IIb ו- III של סימוני ב- RA, AP ו- SA, שכיחות הלימפומה בחולים שטופלו ב- Simponi הייתה גבוהה מהצפוי באוכלוסייה הכללית. דווח על מקרים של לוקמיה בחולים שטופלו ב- Simponi. סיכון רקע מוגבר ללימפומה ולוקמיה בחולי דלקת מפרקים שגרונית הסובלים ממחלה דלקתית ותיקה מאוד, מה שמסבך את הערכת הסיכון.
מקרים נדירים של לימפומה של תאי T hepatosplenic (HSTCL) דווחו לאחר השיווק בחולים שטופלו בחומרים אחרים חוסמי TNF (ראה סעיף 4.8) .צורה נדירה זו של לימפומה של תאי T יש מהלך אגרסיבי במיוחד ותוצאה בדרך כלל קטלנית. רוב המקרים התרחשו בקרב גברים מתבגרים וצעירים כמעט כולם שקיבלו טיפול במקביל לאזתיופרין (AZA) או 6-מרקפטופורין (6 מגה-פיקסל) למחלות מעי דלקתיות. יש לבחון היטב את הסיכון הפוטנציאלי של השילוב של AZA או 6-MP ו- Simponi.
גידולים ממאירים מלבד לימפומה
בשלבים מבוקרים של ניסויים קליניים שלב IIb ו- III שנערכו עם סימפוני ב- RA, AP, SA ו- CU, שכיחות ממאירות אחרות מלבד לימפומה (לא כולל סרטן העור שאינו מלנומה) הייתה דומה בין קבוצת הטיפול עם סימפוני לבין קבוצת הביקורת. .
דיספלסיה של המעי הגס / קרצינומה
לא ידוע אם טיפול golimumab משפיע על הסיכון לפתח דיספלסיה או סרטן המעי הגס. כל החולים עם קוליטיס כיבית שיש להם סיכון מוגבר לפתח דיספלסיה של המעי הגס או קרצינומה (למשל, חולים עם קוליטיס כיבית ארוכת טווח או דלקת מפרקים ראשונית) או שיש להם היסטוריה רפואית של דיספלסיה או סרטן המעי הגס, צריכים להיבדק לגבי דיספלסיה זו ב מרווחים קבועים לפני תחילת הטיפול ובמהלך המחלה. הערכה זו צריכה לכלול קולונוסקופיה וביופסיות בהתאם להמלצות מקומיות. בחולים עם דיספלסיה שאובחנו לאחרונה המטופלים ב- Simponi, יש לשקול היטב את יחס התועלת / סיכון אצל המטופל הבודד והאם יש להמשיך את הטיפול.
בניסוי קליני חקירתי שהעריך את השימוש ב- Simponi בחולים עם אסתמה מתמשכת קשה, דווח על יותר מקרים של ממאירות בחולים שטופלו ב- Simponi מאשר בחולי ביקורת (ראה סעיף 4.8). המשמעות של ממצאים אלה אינה ידועה.
במחקר קליני חקירתי שהעריך את השימוש בסוכן אחר נגד TNF, אינפליקסימאב, בחולים עם מחלת ריאות חסימתית כרונית בינונית עד חמורה (COPD), דווח על מקרים נוספים של ממאירות., בעיקר המשפיעים על הריאות או הראש והצוואר, באינפליקסמאב. חולים שטופלו בהשוואה לחולים בקבוצת הביקורת. כל החולים היו מעשנים כבדים במשך זמן רב. לכן יש לנקוט משנה זהירות בהערכת השימוש באנטגוניסט TNF בחולי COPD, כמו גם בחולים עם סיכון גבוה יותר לממאירות. כמעשנים כבדים.
גידולי עור
מלנומה וקרצינומה של תאי מרקל דווחו בחולים שטופלו בחומרים מעכבי TNF, כולל סימפוני (ראה סעיף 4.8). מומלץ לבצע בדיקת עור תקופתית, במיוחד לחולים עם גורמי סיכון לסרטן העור.
אי ספיקת לב (CHF)
היו דיווחים על החמרה באי ספיקת לב (CHF) ובמקרים חדשים של CHF עם אנטגוניסטים מסוג TNF, כולל סימפוני. בחלק מהמקרים הייתה תוצאה קטלנית. במחקר קליני עם אנטגוניסט אחר של TNF, נצפתה החמרה באי ספיקת לב ותמותה מוגברת עקב CHF. סימפוני לא נחקר בחולים עם CHF. יש להשתמש בזהירות בחולי סימפוני בחולים עם אי ספיקה. לב קל (NYHA בכיתה I / II) יש לעקוב מקרוב אחר המטופלים ולהפסיק את הטיפול ב- Simponi בחולים עם תסמינים חדשים או מחמירים של אי ספיקת לב (ראה סעיף 4.3).
השפעות על מערכת העצבים
השימוש בתרופות חוסמות TNF, כולל סימפוני, נקשר למקרים חדשים או מחמירים של סימפטומים קליניים ו / או עדויות רדיוגרפיות להפרעות דמיאלינציה של מערכת העצבים המרכזית, כולל טרשת נפוצה והפרעות דמיאלינציה היקפיות. הפרעות, יש לשקול היטב את היתרונות והסיכונים של טיפול אנטי-TNF לפני תחילת הטיפול בסימפוני.
יש לשקול הפסקת הטיפול בסימפוני אם מצבים אלה מתפתחים (ראה סעיף 4.8).
התערבויות כירורגיות
הניסיון עם בטיחות הטיפול ב- Simponi בחולים שעברו ניתוח, כולל ארתרופלסטיקה, מוגבל. יש לקחת בחשבון את מחצית החיים של החיסול הארוך בעת תכנון הניתוח. יש לעקוב מקרוב אחר מטופל הזקוק לניתוח במהלך הטיפול ב- Simponi לסיכון מוגבר לזיהומים ולשקול אמצעים מתאימים.
דיכוי חיסוני
האפשרות קיימת כי תרופות אנטי-TNF, כולל סימפוני, משפיעות על הגנות המארח מפני זיהומים וממאירים, מכיוון ש- TNF מתווך דלקת ומווסת את תגובות החיסון התאיות.
תגובות אוטואימוניות
המחסור היחסי ב- TNF? הנגרמת כתוצאה מטיפול אנטי-TNF, עלולה להוביל לתחילת תהליך אוטואימוני. אם מטופל מפגין סימפטומים המנבאים תסמונת דמויית זאבת לאחר טיפול ב- Simponi והוא חיובי לנוגדני DNA כפולים, יש להפסיק את הטיפול ב- Simponi ( ראה סעיף 4.8).
תגובות המטולוגיות
מקרים לאחר השיווק של פנקיטופניה, לוקופניה, נויטרופניה, אנמיה אפלסטית וטרומבוציטופניה דווחו בחולים שטופלו בתרופות נגד TNF. ציטופניות, כולל פנקיטופניה, לא דווחו לעתים קרובות בניסויים קליניים עם סימפוני. יש לייעץ לכל המטופלים לפנות לטיפול רפואי מיידי אם הם מפתחים סימנים או תסמינים תואמים של הפרעות דם (למשל חום מתמשך, חבורות, דימומים וחיוורון). יש לשקול הפסקת הטיפול ב- Simponi בחולים עם הפרעות המטולוגיות המשמעותיות.
מתן טיפול מקביל של אנטגוניסטים מסוג TNF ואנאקינרה
זיהומים חמורים ונויטרופניה התרחשו בניסויים קליניים משולבים של anakinra ומעכב TNF אחר, etanercept, ללא תועלת קלינית נוספת. בהתחשב באופי תופעות הלוואי שנצפו עם טיפול משולב זה, רעילות דומה עשויה להתרחש בשילוב של אנאקינרה ומעכבי TNF אחרים. אין צורך בשילוב סימפוני ואנאקינרה.
מתן טיפול מקביל של אנטגוניסטים מסוג TNF ו- abatacept
במחקרים קליניים, השימוש המשולב של TNF-antagonists ו- abatacept היה קשור לסיכון מוגבר לזיהומים, כולל זיהומים חמורים, בהשוואה ל- TNF-antagonists בשימוש לבד, ללא עלייה בתועלת הקלינית. Simponi ו- abatacept לא מומלץ.
מתן טיפול במקביל לטיפולים ביולוגיים אחרים
אין מספיק מידע בנוגע לשימוש במקביל בסימפוני עם טיפולים ביולוגיים אחרים המשמשים לטיפול באותם מצבים כמו סימפוני.שימוש במקביל בסימפוני עם תרופות ביולוגיות אלה אינו מומלץ בשל האפשרות לסיכון מוגבר לזיהום, ואינטראקציות אפשריות אחרות של תרופות.
תחליף בין DMARD ביולוגי
יש לנקוט משנה זהירות ולהמשיך לפקח על המטופלים בעת מעבר מביולוגיה אחת לאחרת, שכן פעילות ביולוגית חופפת עלולה להגביר עוד יותר את הסיכון לאירועים שליליים, כולל זיהום.
חיסונים / חומרים טיפוליים זיהומיים
חולים המטופלים בסימפוני עשויים לקבל חיסונים במקביל, למעט חיסונים חיים (ראה סעיפים 4.5 ו -4.6). בחולים שטופלו בטיפול אנטי-TNF, קיימים נתונים מוגבלים על התגובה לחיסון, עם חיסונים חיים או על העברת זיהום משני עם מתן חיסונים חיים. שימוש בחיסונים חיים עלול להוביל לזיהומים קליניים, כולל זיהומים המופצים .
שימושים אחרים של חומרים טיפוליים זיהומיים כגון חיידקים מוחלשים חיים (למשל, הזרקות תוך -וסקאליות עם BCG לטיפול בסרטן) עלולים לגרום לזיהומים קליניים, כולל זיהומים מופצים. מומלץ לא לתת תרופות זיהומיות טיפוליות יחד עם סימפוני.
תגובות אלרגיות
מניסיון שלאחר השיווק דווחו תגובות רגישות מערכתיות חמורות (כולל תגובה אנפילקטית) לאחר מתן סימפוני. חלק מהתגובות הללו התרחשו לאחר הניהול הראשון של סימפוני. במקרה של תגובות אנפילקטיות או תגובות אלרגיות לחמורות, יש לתת מתן סימפוני. הופסק באופן מיידי והטיפול המתאים יזם.
רגישות לטקס
מכסה המחט על העט הממולא או המזרק המורכב עשוי לטקס המכיל גומי טבעי מיובש ועלול לגרום לתגובות אלרגיות אצל אנשים רגישים לטקס.
אוכלוסיות מיוחדות
קשישים (≥ 65 שנים)
במחקרי שלב III RA, AP, SA ו- CU לא נצפו הבדלים כלליים בתופעות הלוואי (AE), תופעות לוואי חמורות (EAG) וזיהומים חמורים בחולים בגיל 65 ומעלה שקיבלו טיפול. עם סימפוני, בהשוואה. למטופלים צעירים יותר. עם זאת, יש לנקוט משנה זהירות בטיפול בקשישים ולשים לב במיוחד להתרחשות של זיהומים.במחקר ה- Axial SpA מס 'לא היו מטופלים בני 45 ומעלה.
ליקוי כלייתי וכבד
לא נערכו מחקרים ספציפיים עם סימפוני בחולים עם ליקוי בכליות או בכבד. יש להשתמש בזהירות סימפוני בנבדקים עם תפקוד כבד לקוי (ראה סעיף 4.2).
אוכלוסיית ילדים
חיסונים
במידת האפשר, מומלץ כי חולי ילדים יהיו במצב טוב עם כל החיסונים בהתאם להנחיות החיסון הנוכחיות לפני תחילת הטיפול ב- Simponi.
חומרים עזר
סימפוני מכיל סורביטול (E420). חולים עם בעיות תורשתיות נדירות של אי סבילות לפרוקטוז לא צריכים לקחת סימפוני.
פוטנציאל לטעויות טיפול
סימפוני רשום בעוצמות של 50 מ"ג ו -100 מ"ג למתן תת עורי. חשוב להשתמש במינון הנכון לניהול המינון הנכון כפי שמצוין בפוסולוגיה (ראה סעיף 4.2). יש להקפיד על מתן המינון הנכון על מנת להבטיח כי המטופלים אינם מקבלים מנת יתר או מנת יתר.
04.5 אינטראקציות עם מוצרי תרופות אחרים וצורות אינטראקציה אחרות
לא בוצעו מחקרי אינטראקציה.
שימוש במקביל עם טיפולים ביולוגיים אחרים
השילוב של סימפוני עם טיפולים ביולוגיים אחרים המשמשים לטיפול באותם מצבים כמו סימפוני, כולל אנאקינרה ואבטאצפט אינו מומלץ (ראה סעיף 4.4).
חיסונים חיים / סוכנים טיפוליים זיהומיים
אין לתת חיסונים חיים במקביל ל- Simponi (ראה סעיפים 4.4 ו -4.6).
אין לתת תרופות טיפוליות זיהומיות במקביל ל- Simponi (ראה סעיף 4.4).
מתוטרקסט
למרות ששימוש במקביל במתוטרקסאט (MTX) מביא לעלייה בריכוזי סימפוני במצב יציב בחולים עם RA, AP או AS, הנתונים אינם מצביעים על הצורך בהתאמת מינון Simponi או MTX (ראה סעיף 5.2).
04.6 הריון והנקה
נשים בעלות יכולת ללדת
נשים בעלות הפריון חייבות להשתמש באמצעי מניעה נאות למניעת הריון ולהמשיך בשימוש לפחות 6 חודשים לאחר הטיפול האחרון ב- golimumab.
הֵרָיוֹן
אין נתונים מספקים על השימוש בגלימומאב בנשים בהריון. בשל עיכובו ב- TNF, מתן גולימומאב במהלך ההריון עשוי להשפיע על התגובות החיסוניות התקינות של הילוד. מחקרים בבעלי חיים אינם מצביעים על השפעות ישירות או מזיקות. השפעות עקיפות על ההיריון. , התפתחות עוברית / עוברית, לידה או התפתחות לאחר הלידה (ראה סעיף 5.3) השימוש בגולימומאב אינו מומלץ לנשים בהריון; יש לתת golimumab לנשים בהריון רק כאשר יש צורך בבירור.
Golimumab חוצה את השליה. לאחר טיפול בנוגדן חד שבטי מעכב TNF במהלך ההריון, הנוגדן נמצא עד 6 חודשים בסרום של תינוקות שנולדו לנשים מטופלות. כתוצאה מכך, תינוקות אלה עלולים להיות בעלי סיכון מוגבר לזיהום.
מתן חיסונים חיים בתינוקות חשופים ברחם golimumab אינו מומלץ למשך 6 חודשים לאחר הזרקת golimumab האחרונה של האם במהלך ההריון (ראה סעיפים 4.4 ו- 4.5).
הנקה
לא ידוע אם גולימומאב מופרש בחלב אם או נספג באופן מערכתי לאחר בליעה. הוכח כי גולימומאב עובר לחלב של קופים, ומכיוון שהאימונוגלובולינים אנושיים מופרשים בחלב, נשים לא צריכות להניק במהלך הטיפול ולפחות 6 חודשים. לאחר טיפול golimumab.
פוריות
מחקרי פוריות עם golimumab לא נערכו בבעלי חיים. מחקר פוריות בעכברים שהשתמשו בנוגדן דומה המעכב באופן סלקטיבי את הפעילות התפקודית של TNF עכברי לא הראו השפעות רלוונטיות על הפוריות (ראו סעיף 5.3).
04.7 השפעות על יכולת הנהיגה וההתנהלות במכונות
סימפוני עלול לפגוע מעט ביכולת הנהיגה וההתנהלות במכונות. סחרחורת עלולה להתרחש לאחר מתן סימפוני (ראה סעיף 4.8).
04.8 תופעות לא רצויות
סיכום פרופיל הבטיחות
בתקופת הביקורת של מחקרי RA, AP, SA, Axial SpA nr ו- CU המרכזיים, זיהום בדרכי הנשימה העליונות הייתה התגובה השלילית של התרופה השלילית (ADR) הנפוצה ביותר שדווחה ב -12.6% מהחולים שטופלו ב- golimumab. לעומת 11.0% מהחולים לשלוט בחולים. תופעות הלוואי החמורות ביותר שדווחו עבור golimumab כוללות זיהומים חמורים (כולל אלח דם, דלקת ריאות, שחפת, זיהומים פטרייתיים פולשניים וזיהומים אופורטוניסטיים), מחלות demyelinating, הפעלה מחדש של HBV, CHF, תהליכים אוטואימוניים (תסמונת דמויית זאבת), תגובות המטולוגיות, רגישות יתר מערכתית ( כולל תגובה אנפילקטית), דלקת כלי הדם, לימפומה ולוקמיה (ראה סעיף 4.4).
טבלה עם רשימת תופעות הלוואי
תופעות הלוואי שנצפו בניסויים קליניים ודווחו בעקבות שימוש עולמי שלאחר השיווק בגולימומב מופיעות בטבלה 1. בתוך מחלקת איברי המערכת, תגובות התרופות השליליות מופיעות לפי תדירות באמצעות הקטגוריות הבאות: שכיחות מאוד (≥ 1/10); נפוץ (≥ 1/100,
שולחן 1
טבלה עם רשימת ADR
*: נצפה עם סוכני חסימת TNF אחרים.
בחלק זה, משך הממוצע החציוני (כ -4 שנים) מוצג בדרך כלל לכל השימושים של golimumab. כאשר מתואר השימוש בגלימומאב לפי מינון, משך הממוצע החציוני משתנה (כשנתיים למינון של 50 מ"ג, כשלוש שנים למינון של 100 מ"ג) מכיוון שניתן היה להחליף מטופלים בין מינונים.
תיאור תגובות שליליות של תרופות
זיהומים
בתקופת הבקרה של המחקרים המרכזיים, דלקת בדרכי הנשימה העליונות הייתה התגובה השלילית השכיחה ביותר שדווחה בקרב 12.6% מהחולים שטופלו ב- golimumab (שכיחות ל -100 שנות נושא: 60.8, 95% CI: 55.0, 67.1) לעומת 11.0% של חולי הביקורת (שכיחות ל -100 נבדקים בשנה: 54.5, 95% CI: 46.1, 64.0). בשלבים מבוקרים ובלתי מבוקרים של המחקרים עם מעקב חציוני של כ -4 שנים, השכיחות לכל 100 שנות נושא של דלקות בדרכי הנשימה העליונות הייתה 34.9 אירועים; 95% CI: 33.8, 36.0 לחולים שטופלו ב- golimumab.
בתקופת הבקרה של המחקרים המרכזיים, נצפו זיהומים ב -23.0% מהחולים שטופלו בגלימומאב (שכיחות ל -100 שנות נושא: 132.0; 95% CI: 123.3, 141.1) לעומת 20, 2% מחולי הביקורת (שכיחות לכל 100 שנות נושא: 122.3; 95% CI: 109.5, 136.2). בשלבים מבוקרים ובלתי מבוקרים של המחקרים עם מעקב חציוני של כ -4 שנים, השכיחות לכל 100 שנות נושא של זיהומים הייתה 81.1 אירועים; 95% CI: 79.5, 82.8 לחולים שטופלו ב- golimumab.
בתקופת הביקורת של מחקרי RA, AP, SA ו- Axial SpA nr, נצפו זיהומים חמורים ב -1.2% מהחולים שטופלו ב- golimumab וב -1.2% מחולי הביקורת. שכיחות הזיהומים החמורים לכל 100 שנות נושא במהלך המעקב בתקופת הבקרה של מחקרי RA, AP, SA ו- nr-Axial SpA הייתה 7.3; 95% CI: 4.6, 11, 1 עבור קבוצת 100 מ"ג golimumab, של 2.9; 95% CI: 1.2, 6.0 לקבוצת golimumab 50 מ"ג ו- 3.6; 95% CI: 1, 5, 7.0 עבור קבוצת הפלסבו. בתקופת הבקרה של מחקרי UC אינדוקציה של golimumab, נצפו זיהומים חמורים ב- 0.8 % מהחולים שטופלו ב- golimumab לעומת 1.5% מחולי הביקורת. זיהומים חמורים שנראו בחולים שטופלו ב- golimumab כללו שחפת, זיהומים חיידקיים כולל אלח דם ודלקת ריאות, זיהומים פטרייתיים פולשניים וזיהומים אופורטוניסטיים אחרים. חלק מהזיהומים הללו היו קטלניים. בחלקים המבוקרים והבלתי מבוקרים של המחקרים המרכזיים עם מעקב חציוני של עד 3 שנים, הייתה שכיחות גבוהה יותר של זיהומים חמורים, כולל זיהומים אופורטוניסטיים ושחפת בחולים שטופלו ב- golimumab 100 מ"ג בהשוואה למטופלים שטופלו ב- golimumab. 50 מ"ג. השכיחות לכל 100 שנות נושא של כל הזיהומים החמורים הייתה 4.1; 95% CI: 3.6, 4.5, לחולים שטופלו ב- golimumab 100 מ"ג ו -2.5; 95% CI: 2.0, 3.1, לחולים שטופלו ב- golimumab 50 מ"ג.
גידולים ממאירים
לימפומה
שכיחות הלימפומה בחולים שטופלו ב- golimumab במהלך המחקרים המרכזיים הייתה גבוהה מהצפוי באוכלוסייה הכללית. בחלקים מבוקרים ולא מבוקרים של מחקרים אלו עם מעקב חציוני של עד 3 שנים, נצפתה שכיחות גבוהה יותר של לימפומה. בחולים שטופלו ב- golimumab 100 מ"ג בהשוואה לחולים שטופלו ב- golimumab 50 מ"ג. לימפומה אובחנה ב -11 נבדקים (1 בקבוצות הטיפול ב- golimumab 50 מ"ג ו -10 בקבוצות הטיפול ב- golimumab 100 מ"ג) עם שכיחות (95% CI) לכל 100 שנות נושא של מעקב אחר 0.03 ו 0.13 אירועים עבור golimumab 50 מ"ג ו- golimumab 100 מ"ג, בהתאמה, ו 0.00 אירועים עבור פלסבו. רוב הלימפומות התרחשו במחקר GO-AFTER בו נרשמו מטופלים שנחשפו בעבר לתרופות אנטי-TNF ועם משך מחלה ארוך יותר עקשן יותר (ראה סעיף 4.4).
גידולים ממאירים מלבד לימפומה
בתקופות הבקרה של המחקרים המרכזיים ובמשך כ -4 שנים של מעקב, שכיחות ממאירות אחרות מלבד לימפומה (לא כולל סרטן עור שאינו מלנומה) הייתה דומה בין הגלימומאב לקבוצות הביקורת. כ -4 שנים של מעקב, שכיחות ממאירות לא לימפומה (למעט סרטן עור שאינו מלנומה) הייתה דומה לזו באוכלוסייה הכללית.
בתקופות מבוקרות ובלתי מבוקרות של המחקרים המרכזיים עם חציון מעקב עד 3 שנים, אובחן סרטן עור שאינו מלנומה אצל 5 נבדקים שטופלו בפלסבו, 10 טופלו ב- golimumab 50 מ"ג ו -31 שטופלו ב- golimumab 100 מ"ג עם שכיחות (95% CI) לכל 100 שנות נושא של מעקב של 0.36 עבור golimumab משולב ו- 0.87 עבור פלסבו.
בתקופות מבוקרות ובלתי מבוקרות של המחקרים המרכזיים עם חציון מעקב עד 3 שנים, אובחנו ממאירות בנוסף למלנומה, סרטן עור שאינו מלנומה ולימפומה אצל 5 נבדקים שטופלו בפלסבו, מתוך 21 שטופלו ב- golimumab 50 מ"ג וב -34 שטופלו ב- golimumab 100 מ"ג עם שכיחות (95% CI) לכל 100 שנות מעקב של 0.48 עבור golimumab משולב ו- 0.87 עבור פלסבו (ראה סעיף 4.4).
מקרים שדווחו בניסויים קליניים בנוכחות אסתמה
במחקר קליני חוקר, מטופלים הסובלים מאסתמה חמורה קיבלו מינון טעינה של golimumab (150% ממינון הטיפול שהוקצה) תת עורית בשבוע 0, ואחריו golimumab 200 מ"ג, golimumab 100 מ"ג או golimumab 50 מ"ג כל אחד. 4 שבועות תת עורית דרך שבוע 52. שמונה ממאירים בקבוצת הטיפול המשולב בגלימומאב (n = 230) ואף אחד בקבוצת הטיפול בפלסבו (n = 79) דווחו. לימפומה דווחה אצל חולה אחד, סרטן עור שאינו מלנומה בשני חולים וממאירים אחרים ב -5 חולים. לא היה מיזוג ספציפי של כל סוג ממאיר.
בשלב מבוקר הפלצבו של המחקר, השכיחות (95% CI) של כל הממאירות ל -100 שנות מעקב של מעקב הייתה 3.19 בקבוצת הטיפול ב- golimumab. שכיחות (95% CI) ל -100 שנות מעקב אחר מעקב. -חולים בחולים שטופלו ב- golimumab היו 0.40 ללימפומה, 0.79 לסרטן עור שאינו מלנומה, ו -1.99 עבור ממאירות אחרות. עבור נבדקים שטופלו בפלסבו, השכיחות (95% CI) של ממאירות אלו לכל 100 נבדקים / שנת מעקב הייתה 0.00. המשמעות של ממצאים אלה אינה ידועה.
אירועים נוירולוגיים
בתקופות המבוקרות והלא מבוקרות של המחקרים המרכזיים עם מעקב חציוני של עד 3 שנים, נצפתה שכיחות גבוהה יותר של דמיאלינציה בחולים שטופלו ב- golimumab 100 מ"ג בהשוואה לחולים שטופלו ב- golimumab 50 מ"ג (ראה סעיף 4.4). .
עלייה באנזימי הכבד
בתקופות הבקרה של מחקרי RA ו- AP מרכזיים, עליות קלות ב- ALT (> 1 ו- 1 ו-
בתקופת הביקורת של מחקרי RA ו- AS המרכזיים, עליות ALT פי 5 ULN היו נדירות ונצפו במספר גדול יותר של מטופלים שטופלו ב- golimumab (0.4%עד 0, 9%) בהשוואה לחולי ביקורת (0.0%). מגמה זו לא נצפתה באוכלוסיית AP. בתקופות מבוקרות ובלתי מבוקרות של מחקרי RA, AP ו- SA המרכזיים עם מעקב חציוני של 5 שנים, שכיחות העלאות ALT ≥ 5 פעמים ULN הייתה דומה הן לחולי golimumab והן לחולי ביקורת. באופן כללי, העלאות הללו היו אסימפטומטיות והחריגות פחתו או נפתרו עם המשך או הפסקת גלימומאב או שינוי תרופות נלוות. לא דווחו מקרים בתקופות מבוקרות ובלתי מבוקרות של מחקר Axial SpA. (עד שנה) בתקופות הבקרה. ממחקרי האינדוקציה החשובים של CU עם golimumab, נצפו עליות ב- ALAT ≥ 5 x ULN בשיעורים דומים בקרב מטופלים שטופלו ב- golimumab ופלסבו (0, 3% עד 1.0%).בתקופות מבוקרות ובלתי מבוקרות של מחקרי UC מרכזיים עם מעקב חציוני של כשנתיים, שיעור החולים עם העלאות ALT ≥ 5 x ULN היה 0.8% בחולים שקיבלו golimumab במהלך הטיפול במחקר UC.
במחקרים מרכזיים של RA, AP, SA ו- Axial SpA, חולה במחקר RA עם הפרעות בכבד קיימות ותרופות גורם מבלבל שטופלו ב- golimumab פיתחו הפטיטיס קטלנית שאינה מדבקת עם צהבת. לא ניתן לשלול את תפקידו של golimumab כגורם תורם או מחמיר.
תגובות באתר ההזרקה
בתקופות הבקרה של המחקרים המרכזיים, נצפו תגובות באתר ההזרקה אצל 5.4% מהחולים שטופלו ב- golimumab, לעומת 2.0% מחולי הביקורת. הימצאות נוגדנים ל- golimumab עשויה להגביר את הסיכון לתגובות באתר ההזרקה. רוב התגובות באתר ההזרקה היו קלות ובינוניות והתופעות השכיחות ביותר היו אריתמה באתר ההזרקה. תגובות באתר ההזרקה בדרך כלל אינן דורשות הפסקת הטיפול בתרופה.
במחקרי שלב IIb ו / או III מבוקרים ב- RA, AP, SA, Axial nr SpA, אסתמה מתמשכת קשה ובמחקרי שלב II / III UC, אף חולה שטופל ב- golimumab לא פיתח תגובות אנפילקטיות.
נוגדנים אוטואימוניים
בתקופות המבוקרות והלא מבוקרות של המחקרים המרכזיים עם שנה אחת של מעקב, 3.5% מהחולים שטופלו ב- golimumab ו -2.3% מחולי הביקורת סבלו מ- ANA חיובי לאחרונה (טיטרציות של 1: 160 ומעלה). התדירות של נוגדנים נגד dsDNA בשנה אחת של מעקב בחולים שליליים נגד dsDNA בתחילת המחקר הייתה 1.1%.
אוכלוסיית ילדים
דלקת מפרקים אידיופטית לנוער רב -מפרקית
הבטיחות של golimumab נחקרה במחקר שלב III שנערך בקרב 173 חולים עם pJIA מגיל שנתיים עד 17 שנים. המעקב הממוצע היה כשנתיים. במחקר זה, סוג ותדירות תופעות הלוואי המדווחות היו בדרך כלל דומות לאלה שנראו במחקרים במבוגרים עם RA.
דיווח על חשדות לתגובות שליליות
הדיווח על תגובות שליליות החשודות המתרחשות לאחר אישור התרופה חשוב, שכן הוא מאפשר מעקב רציף אחר יחס התועלת / סיכון של התרופה. אנשי מקצוע בתחום הבריאות מתבקשים לדווח על כל חשד לתגובות שליליות באמצעות סוכנות התרופות האיטלקית, אתר האינטרנט: http://www.agenziafarmaco.gov.it/it/responsabili.
04.9 מנת יתר
במנות קליניות ניתנו מינונים בודדים של עד 10 מ"ג / ק"ג תוך ורידי ללא כל רעילות מגבילה. במקרה של מנת יתר, מומלץ לעקוב אחר המטופל לאיתור סימנים ותסמינים של תופעות לוואי וטיפול סימפטומטי מתאים ייפתח מיידית.
05.0 נכסים פרמקולוגיים
05.1 תכונות פרמקודינמיות
קבוצה פרמקותרפית: מעכבי חיסון, מעכב גורם נמק בגידול אלפא (TNF-?), קוד ATC: L04AB06
מנגנון הפעולה
Golimumab הוא נוגדן חד-שבטי אנושי היוצר מתחמים יציבים בעלי זיקה גבוהה הן לצורות הטרנס ממברנה המסיסות והן הביו-אקטיביות של TNF-? אנושי, מונע את קישור TNF-? לקולטנים שלו.
השפעות פרמקודינמיות
הוכח כי קישור גולימומאב ל- TNF אנושי מעכב ביטוי של פני התא של מולקולות הדבקה ב- TNF-?, Selectin E, מולקולת הדבקה של תאי כלי דם מסוג 1 (VCAM) ומולקולת הדבקה תאיים מסוג 1 (ICAM) על ידי תאי אנדותל אנושיים. בַּמַבחֵנָה, הפרשה הנגרמת על ידי TNF על ידי אינטרלוקין (IL) -6, IL-8 וגרנולוציטים וגורם מגרה מושבה מקרופאג (GM-CSF) על ידי תאי האנדותל האנושיים, נבלמה גם היא על ידי golimumab.
נצפה שיפור ברמות החלבון C-reactive (CRP) בהשוואה לקבוצות הפלסבו, וטיפול סימפוני הביא לירידה משמעותית ברמות הסרום מהתחלה של IL-6, ICAM-1, מטריקס מטלופרוטאינאז. 3 (MMP) ואנדותל וסקולרי. גורם הגדילה (VEGF), בהשוואה לטיפול הבקרה. יתר על כן, בחולי RA ו- AS, רמות TNF-? ירידה ורמות IL-8 ירדו בחולים עם AP. שינויים אלה נצפו בהערכה הראשונה (שבוע 4) לאחר מתן סימפוני הראשוני ובדרך כלל נמשכו עד שבוע 24.
יעילות קלינית
דלקת מפרקים שגרונית
היעילות של סימפוני הודגמה בשלושה ניסויים קליניים רב-מרכזיים, אקראיים, כפול-סמיות, מבוקרי פלסבו, שנערכו ביותר מ- 1500 חולים בגילאי 18 ומעלה עם RA פעיל בינוני עד חמור שאובחן על פי הקריטריונים של American College of Rheumatology (ACR). לתקופה של 3 חודשים לפחות לפני ההקרנה. לחולים היו צריכים להיות לפחות 4 מפרקים נפוחים וארבעיים. סימפוני או פלצבו ניתנו תת עורית כל 4 שבועות.
GO-FORWARD העריך 444 חולים עם RA פעיל למרות מינון יציב של לפחות 15 מ"ג לשבוע של MTX ואשר לא טופלו בעבר בתרופות אנטי-TNF כלשהן. החולים חולקו באקראי לפלצבו + MTX, סימפוני 50 מ"ג + MTX, סימפוני 100 מ"ג + MTX או סימפוני 100 מ"ג + פלצבו. לחולים שקיבלו פלצבו + MTX, לאחר שבוע 24, הוקצו סימפוני 50 מ"ג + MTX. בשבוע 52, המטופלים נכנסו למחקר הרחבה ארוך טווח בעל תווית פתוחה.
GO-AFTER העריך 445 מטופלים שטופלו בעבר בתרופה אחת או יותר נגד TNF, אדלימומאב, etanercept או אינפליקסימאב. החולים חולקו באקראי לפלסבו, סימפוני 50 מ"ג או סימפוני 100 מ"ג. במהלך המחקר, החולים הצליחו להמשיך בטיפול DMARD במקביל עם MTX, sulfasalazine (SSZ) ו / או הידרוקסיכלורוקין (HCQ). הסיבות שניתנו להפסקת טיפולים קודמים נגד TNF היו חוסר יעילות (58%), חוסר סובלנות (13%) ו / או סיבות אחרות מלבד בטיחות או יעילות (29%, בעיקר מסיבות כלכליות).
GO-BEFORE העריך 637 חולים עם RA פעיל, נאיבי MTX ולא טופלו בעבר בתרופה נגד TNF. החולים חולקו באקראי לקבלת פלסבו + MTX, סימפוני 50 מ"ג + MTX, סימפוני 100 מ"ג + MTX או סימפוני 100 מ"ג + פלצבו. בשבוע 52, המטופלים נכנסו למחקר הרחבה ארוך טווח, שבו מטופלים שקיבלו פלסבו + MTX והיו להם לפחות מפרק אחד כואב או נפוח הועברו לטיפול Simponi 50 מ"ג + MTX.
ב- GO-FORWARD, נקודות הקצה העיקריות (co) היו שיעור החולים שהשיגו תגובה ACR 20 בשבוע 14 ושיפור בשאלון הערכת הבריאות (HAQ) בשבוע 24 מתחילת המחקר. היה שיעור החולים שהשיגו תגובה ACR 20. בשבוע 14. ב- GO-BEFORE, נקודות הסיום השיתופיות העיקריות היו שיעור החולים שהשיגו תגובת ACR 50 בשבוע 24 ושינוי מהבסיס בניקוד Sharp שהשתנה על ידי ואן דר היידה (vdH-S) בשבוע 52. בנוסף לנקודות הסיום העיקריות, נערכו הערכות נוספות של ההשפעה של טיפול סימפוני על סימנים ותסמינים של דלקת פרקים, תגובה רדיוגרפית, תפקוד גופני ואיכות חיים הקשורה למצב. של בריאות.
באופן כללי, לא נצפו הבדלים משמעותיים מבחינה קלינית בהערכות היעילות בין Simponi 50 מ"ג ל- 100 מ"ג בשילוב עם משטרי מינון MTX עד שבוע 104 ב- GO-FORWARD ו- GO-BEFORE ועד שבוע 24. ב- GO-AFTER. ב כל אחד ממחקרי RA בהתאם לתכנון המחקר, ניתן היה להעביר חולים בהארכה ארוכת טווח בין 50 מ"ג ל- 100 מ"ג מינונים לפי שיקול דעתו של רופא המחקר.
סימנים וסימפטומים
תוצאות קריטריוני ACR המרכזיים למינון 50 מ"ג סימפוני בשבועות 14, 24 ו -52 עבור GO-FORWARD, GO-AFTER ו- GO-BEFORE מוצגים בטבלה 2 ומתוארים להלן. תגובות נצפו בהערכה הראשונה (שבוע 4) לאחר הניהול הראשוני של סימפוני.
במחקר GO-FORWARD, מתוך 89 הנבדקים שאקראו ל- Simponi 50 מ"ג + MTX, 48 עדיין היו בטיפול בשבוע 104. בין אלה, 40, 33 ו -24 חולים קיבלו תגובה ACR 20/50/70 בשבוע 104, בקרב מטופלים שנשארו במחקר וטיפלו ב- Simponi, נצפו שיעורי תגובה דומים ל- ACR 20/50/70 משבוע 104 עד שבוע 256.
במחקר GO-AFTER, אחוז החולים שהשיגו תגובה ACR 20 היה גבוה יותר בקרב מטופלים שטופלו ב- Simponi בהשוואה לחולים שטופלו בפלסבו, ללא קשר לסיבה המדווחת להפסקת טיפול אנטי דלקתי אחד או יותר. -TNF.
שולחן 2
תוצאות יעילות מרכזיות מהחלקים המבוקרים במחקרי GO-FORWARD, GO-AFTER ו- GO-BEFORE
a מתאים לחולים אקראיים; מספר החולים בפועל שניתן להעריך עבור כל נקודת קצה עשוי להשתנות לפי נקודת זמן.
* p ≤ 0.001
NA: לא ישים
במחקר GO-BEFORE, הניתוח העיקרי בחולים עם דלקת מפרקים שגרונית בינונית עד חמורה (סימפוני 50 ו -100 מ"ג + קבוצות שילוב MTX לעומת MTX בלבד ל- ACR 50) לא היה מובהק סטטיסטית בשבוע 24 (p = 0.053 בשבוע 52 האוכלוסייה, שיעור החולים בקבוצת Simponi 50 מ"ג + MTX שהשיגו תגובה ACR היה בדרך כלל גבוה יותר אך לא שונה באופן משמעותי בהשוואה ל- MTX בלבד (ראה טבלה 2). ניתוחי תת -קבוצה נוספים המייצגים את האוכלוסייה המצוין של חולים עם , RA פעיל ומתקדם הוכח השפעה מעולה באופן כללי עם סימפוני 50 מ"ג + MTX לעומת MTX בלבד באוכלוסייה המצוינת בהשוואה לאוכלוסייה הכוללת.
במחקרי GO-FORWARD ו- GO-AFTER נצפו תגובות מובהקות סטטיסטית וקלינית בסולם הפעילות של המחלות (DAS28) בכל שלב שצוין מראש, בשבוע 14 ובשבוע 24 (p ≤ 0.001). בקרב מטופלים שנשארו בטיפול סימפוני, אקראית בתחילת המחקר, תגובות DAS28 נשמרו עד שבוע 104. בקרב מטופלים שנשארו במחקר וטיפלו בסימפוני, תגובות DAS28 היו דומות משבוע 104 עד שבוע 256.
במחקר GO-BEFORE הוערכה תגובה קלינית מרכזית שהוגדרה כשמירה על תגובה ACR 70 לאורך 6 חודשים רצופים. בשבוע 52, 15% מהחולים בקבוצת Simponi 50 מ"ג + MTX השיגו תגובה קלינית מעולה בהשוואה ל -7% מהחולים בקבוצת הפלסבו + MTX (p = 0.018). מתוך 159 הנבדקים שאקראו ל- Simponi 50 מ"ג + MTX, 96 עדיין היו בטיפול בשבוע 104. מבין 85, 66 ו -53 חולים קיבלו תגובה ACR 20/50/70 בשבוע 104, בהתאמה. וטופלו ב- Simponi, דומה שיעורי התגובה של ACR 20/50/70 נצפו משבוע 104 עד שבוע 256.
תגובה רדיוגרפית:
במחקר GO-BEFORE, שינויים מהבסיס בציון vdH-S, ציון נזק מבני מורכב המודד באופן רדיוגרפי את מספר וגודל שחיקות המפרקים ומידת הפחתת שטח המפרק בידיים / פרקי הידיים והרגליים, שימשו להערכת מידת הנזק המבני. תוצאות מפתח עבור סימפוני ב -50 מ"ג בשבוע 52 מוצגות בטבלה 3.
מספר החולים ללא שחיקה חדשה או שינוי מהבסיס בציון ה- vdH-S הכולל ≤ 0 היה גבוה משמעותית בקבוצת סימפוני מאשר בקבוצת הביקורת (p = 0.003). ההשפעות הרדיוגרפיות שנצפו בשבוע 52 נשמרו עד שבוע 104. בקרב מטופלים שנשארו במחקר וטיפלו בסימפוני, ההשפעות הרדיוגרפיות היו דומות משבוע 104 עד שבוע 256.
שולחן 3
ממוצע (SD) של שינויים רדיוגרפיים מהבסיס לשבוע 52 בציון ה- vdH-S הכולל בקרב אוכלוסיית המחקר GO-BEFORE
a מתאים לחולים אקראיים
* p = 0.015
** p = 0.044
תפקוד גופני ואיכות חיים הקשורה לבריאות
התפקוד הגופני והנכות הוערכו כנקודות קצה נפרדות במחקרי GO-FORWARD ו- GO-AFTER, תוך שימוש במדד הנכות של HAQ DI. במחקרים אלה, בשבוע 24, סימפוני הראה שיפור מובהק קלינית וסטטיסטית ב- HAQ DI מהתחלה בהשוואה לקבוצת הביקורת. בקרב מטופלים שנשארו בטיפול סימפוני, אקראית בתחילת המחקר, השיפור ב- HAQ DI נשמר עד שבוע 104 בקרב מטופלים שנשארו במחקר וטיפלו ב- Simponi, השיפור ב- HAQ DI היה דומה משבוע 104 עד שבוע 256.
מחקר GO-FORWARD הראה שיפור משמעותי מבחינה קלינית וסטטיסטית באיכות החיים הקשורה לבריאות, כפי שנמדד לפי ציון המרכיבים הפיזיים של SF-36 בחולים שטופלו ב- Simponi לעומת פלסבו בשבוע 24. בקרב מטופלים שנשארו בטיפול Simponi, רנדומלית ב תחילת המחקר, השיפור ב- SF-36 נשמר עד שבוע 104. בקרב מטופלים שנשארו במחקר וטיפלו ב- Simponi, השיפור ברכיב הפיזי של SF-36 היה במצב דומה משבוע 104 עד שבוע 256. ב- GO -מחקרים FORWARD ו- GO-AFTER, נצפו שיפורים מובהקים סטטיסטית בעייפות, על פי סולם ההערכה התפקודית של טיפול במחלות כרוניות-עייפות (FACIT-F).
דלקת מפרקים פסוריאטית
היעילות והבטיחות של סימפוני הוערכו במחקר קליני רב-מרכזי, אקראי, כפול סמיות, מבוקר פלצבו (GO-REVEAL) שנערך בקרב 405 חולים מבוגרים עם PA פעיל (3 מפרקים נפוחים ו -3 מפרקים כואבים), למרות טיפול עם תרופות נוגדות דלקת לא סטרואידיות (NSAIDs) או DMARDs. לחולים במחקר זה אובחנו AP למשך 6 חודשים לפחות ולפחות פסוריאזיס קלה. גושים (43%), דלקת מפרקים היקפית אסימטרית (30%), דלקת מפרקים אינטרפלנגלית דיסטאלית (DIP) (15%), דלקת ספונדיליטיס עם דלקת פרקים היקפית (11%) ודלקת מפרקים מושחתת (1%). ללא טיפול קודם עם אנטי-TNF סימפוני או פלסבו ניתנו תת עורית כל 4 שבועות. החולים חולקו באקראי לפלצבו, סימפוני 50 מ"ג או ל- S להטיל 100 מ"ג. לחולים שקיבלו פלסבו, לאחר שבוע 24, הוקצו סימפוני 50 מ"ג. בשבוע 52, חולים נכנסו למחקר הרחבה ארוך טווח.
כ -48% מהחולים המשיכו במינונים יציבים של מתוטרקסט (≤ 25 מ"ג לשבוע). נקודות הקצה השיתופיות הראשונות היו שיעור החולים שהשיגו תגובה ACR 20 בשבוע 14 והשינוי מהבסיס בניקוד הכולל של AP vdH-S שהשתנה בשבוע 24.
באופן כללי, לא נצפו הבדלים קליניים משמעותיים במדדי יעילות בין שיעורי המינון של 50 מ"ג ל- 100 מ"ג עד שבוע 104. על פי תכנון המחקר, חולים בהארכה ארוכת טווח יכולים לעבור מעבר בין סימפוני 50 מ"ג ל -100. מנות מ"ג לפי שיקול דעתו של רופא המחקר.
סימנים וסימפטומים
תוצאות מפתח למינון 50 מ"ג בשבועות 14 ו -24 מוצגות בטבלה 4 ומתוארות להלן.
טבלה 4
תוצאות יעילות מרכזיות ממחקר GO-REVEAL
* עמ '
a מתאים לחולים אקראיים; מספר החולים בפועל שניתן להעריך עבור כל נקודת קצה עשוי להשתנות לפי נקודת זמן
ב מדד אזור פסוריאזיס וחומרת חומרה
c בהתבסס על תת -קבוצת החולים עם מעורבות שטח הגוף (BSA) ≥ 3%בתחילת המחקר, 79 חולים (69.9%) בקבוצת הטיפול בפלסבו ו -109 (74.3%) ב- Simponi 50 מ"ג.
תגובות נצפו בהערכה הראשונה (שבוע 4) לאחר הניהול הראשוני של סימפוני. תגובות ACR 20 דומות נצפו בשבוע 14 בחולים עם דלקת מפרקים רב -מפרקית בהיעדר גושים שגרוניים ותת -סוגים AP, דלקת מפרקים היקפית א -סימטרית. מספר החולים עם תת -סוגים אחרים של הרשות הפלסטינית היה קטן מכדי לאפשר הערכה משמעותית.התגובות שנצפו בקבוצות הטיפול ב- Simponi היו דומות בחולים שטופלו או לא עם MTX במקביל. מתוך 146 החולים שאקראו ל- Simponi 50 מ"ג, 70 עדיין היו בטיפול בשבוע 104. מבין 70 החולים הללו, 64, 46 ו -31 חולים קיבלו תגובה ACR 20/50/70 בהתאמה. בקרב מטופלים שנשארו במחקר וטיפלו ב- Simponi, נצפו שיעורי תגובה דומים ל- ACR 20/50/70 משבוע 104 עד שבוע 256.
תגובות מובהקות סטטיסטית נצפו גם ב- DAS28 בשבועות 14 ו -24 (עמ '
בשבוע 24 נצפו שיפורים בפרמטרי הפעילות ההיקפית האופייניים לדלקת פרקים פסוריאטית (למשל מספר מפרקים נפוחים, מספר מפרקים רכים, דקטיליטיס ודלקות) בחולים שטופלו ב- Simponi. הטיפול ב- Simponi הביא לשיפור משמעותי בתפקוד הגופני כפי שהוערך על ידי HAQ DI ושיפור משמעותי באיכות החיים הקשורה לבריאות בהתבסס על ציוני סיכום של המרכיבים הפיזיים והנפשיים של ה- SF-36. על טיפול Simponi, שאליו הם חולקו באקראי. בתחילת המחקר, תגובות DAS28 ו- HAQ DI נשמרו עד שבוע 104. בקרב מטופלים שנשארו במחקר וטיפלו ב- Simponi, תגובות DAS28 ו- HAQ DI היו דומות. שבוע 104 עד שבוע 256.
תגובה רדיוגרפית:
הנזק המבני לכפות הידיים והרגליים הוערך באופן רדיולוגי על ידי השינוי מהנקודה הבסיסית בציון vdH-S, שהשתנה עבור ה- AP בתוספת המפרקים הבין דיסטאלנגאליים הדיסטליים (DIP) של היד.
טיפול Simponi 50 מ"ג מפחית את קצב התקדמות הנזק למפרקים היקפיים בהשוואה לטיפול פלסבו בשבוע 24, נמדד כשינוי מההתחלה בציון ה- vdH -S הכולל שהשתנה (ממוצע ± SD ציון היה 0.27 ± 1, 3 בקבוצת הפלסבו בהשוואה ל- - 0.16 ± 1.3 בקבוצת סימפוני; p = 0.011). מתוך 146 המטופלים שהוקצו באקראי ל- Simponi 50 מ"ג, נתוני רנטגן בשבוע 52 היו זמינים עבור 126 חולים, מתוכם 77% לא הראו התקדמות מתחילת המחקר. בשבוע 104, נתוני רנטגן היו זמינים עבור 114 חולים ו -77% לא הראו התקדמות מהתחלה. בקרב מטופלים שנשארו במחקר וטיפלו ב- Simponi, חלקים דומים של מטופלים לא הראו התקדמות מהתחלה משבוע 104 עד שבוע 256.
ספונדילוארתריטיס צירית
ספונדיליטיס אנקילוזינג
היעילות והבטיחות של סימפוני הוערכו במחקר קליני רב-מרכזי, כפול סמיות, אקראי, מבוקר פלסבו (GO-RAISE) שנערך בקרב 356 חולים מבוגרים עם ספונדיליטיס אקלילית פעילה (המוגדרת כפעילות הפתולוגית של מדד באת 'של ספונדיליטיס אנקילוזינג (BASDAI) ) ≥ 4 ו- VAS לכאבי גב מוחלטים ≥ 4 בסולם של 0 עד 10 ס"מ). לחולים שנרשמו למחקר זה הייתה המחלה בשלב פעיל, למרות הטיפול הנוכחי או הקודם בתרופות NSAID או DMARD ולא טופלו בעבר בתרופות אנטי-TNF כלשהן. סימפוני או פלצבו ניתנו תת עורית כל 4 שבועות. החולים חולקו באקראי לפלצבו, סימפוני 50 מ"ג או סימפוני 100 מ"ג והצליחו להמשיך בטיפול DMARD במקביל (MTX, SSZ ו / או HCQ). נקודת הסיום העיקרית הייתה אחוז החולים עם תגובת קבוצת המחקר Ankylosing Spondylitis Assessment Group (ASAS 20) בשבוע 14. נתוני יעילות מבוקרי פלסבו נאספו ונותחו עד שבוע 24.
תוצאות המפתח למינון 50 מ"ג מוצגות בטבלה 5 ומתוארות להלן. באופן כללי, לא נצפו הבדלים קליניים משמעותיים במדדי יעילות בין משטרי המינון של 50 מ"ג ל- 100 מ"ג עד שבוע 24. על פי תכנון המחקר, חולים בהארכה ארוכת טווח יכולים לעבור מעבר בין סימפוני 50 מ"ג ל -100 מ"ג. מינונים לפי שיקול דעתו של רופא המחקר.
טבלה 5
תוצאות יעילות מרכזיות ממחקר GO-RAISE
* p ≤ 0.001 לכל ההשוואות
a מתאים לחולים אקראיים; מספר החולים בפועל שניתן להעריך עבור כל נקודת קצה עשוי להשתנות לפי נקודת זמן
בקרב מטופלים שנשארו במחקר וטיפלו ב- Simponi, שיעור החולים עם תגובה ASAS 20 ו- ASAS 40 היה דומה משבוע 24 עד שבוע 256.
תגובות מובהקות סטטיסטית נצפו גם ב- BASDAI 50, 70 ו- 90 (p ≤ 0.017) בשבועות 14 ו -24. נמצאו שיפורים במדידות מפתח של פעילות מחלות בהערכה הראשונה (שבוע 4) לאחר מתן סימפוני הראשוני שנשמר עד שבוע. 24. בקרב מטופלים שנשארו במחקר וטיפלו ב- Simponi, שיעורים דומים של שינוי מהבסיס נצפו ב- BASDAI משבוע 24 עד שבוע 256. יעילות עקבית נצפתה בחולים ללא קשר לשימוש ב- DMARD (MTX, sulfasalazine ו / או הידרוקסיכלורוקין), נוכחות של האנטיגן HLA-B27 או רמות CRP בסיסיות המבוססות על הערכת תגובות ASAS 20 בשבוע 14.
הטיפול ב- Simponi הוביל לשיפור משמעותי בתפקוד הגופני כפי שהוערך על ידי שינויים מהבסיס במדד פונקציונלי של ספונדיטיס באנקילוזינג (BASFI) בשבועות 14 ו -24. השתפר בשבועות 14 ו- 24. בקרב מטופלים שנשארו במחקר וטיפלו ב- Simponi, שיפורים בתפקוד הגופני ובאיכות החיים הקשורה לבריאות היו דומים משבוע 24 עד שבוע 256.
ספונדילוארתריטיס צירית לא רדיוגרפית
הבטיחות והיעילות של סימפוני הוערכו במחקר רב-מרכזי, אקראי, כפול סמיות, מבוקר פלצבו (GO-AHEAD) שנערך ב -197 חולים מבוגרים עם SpA מספר ציני חמור בשלב פעיל (מוגדר כמטופלים שעמדו בסיווג ASAS. קריטריונים לאבחון של spondyloarthritis צירית אך לא עמדו בקריטריונים שהשתנו בניו יורק לאבחון AS.) לחולים שנרשמו למחקר זה הייתה מחלה פעילה (המוגדרת על ידי BASDAI ≥ 4 וסולם אנלוגי חזותי (VAS) לכאבי גב כלליים. ≥ 4, כל אחד בסולם של 0 עד 10 ס"מ) למרות טיפול מתמשך או קודם ב- NSAID ולא טופל בעבר בכל גורם ביולוגי כולל אנטי TNF. החולים חולקו באקראי לפלסבו או ל- Simponi 50 מ"ג הניתנים תת עורית כל 4 שבועות. בשבוע 16, נכנסו מטופלים תקופת טיפול פתוחה בה קיבלו כולם Simponi 50 מ"ג במתן תת עורית כל 4 שבועות עד שבוע 48 עם הערכות יעילות שבוצעו עד שבוע 52 ומעקב בטיחותי עד שבוע 60. כ -93% מהחולים שקיבלו סימפוני בתחילת הארכת התווית הפתוחה (שבוע 16) נותרה בטיפול עד סוף המחקר (שבוע 52). הניתוחים בוצעו הן על כלל האוכלוסייה שטופלה (AT, N = 197) והן על האוכלוסייה עם סימנים אובייקטיביים של דלקת (OSI, N = 158, כפי שמעידים על ידי רמות גבוהות של CRP ו / או על ידי "עדויות של sacroiliitis ב- MRI נתוני יעילות מבוקרי פלסבו נאספו ונותחו עד שבוע 16. נקודת הסיום העיקרית הייתה שיעור החולים שהשיגו תגובה ASAS 20 בשבוע 16. תוצאות מפתח מוצגות בטבלה 6 ומתוארות להלן.
טבלה 6
תוצאות יעילות מרכזיות ממחקר GO-AHEAD בשבוע 16
a מתאים לחולים אקראיים ומטופלים
b ציון פעילות של מחלת חלבון אנקילוזינג C-תגובתי (AT-Placebo, N = 90; AT-Simponi 50 mg, N = 88; OSI-Placebo, N = 71; OSI-Simponi 50 mg, N = 71)
c n תואם למספר החולים עם נתוני MRI בסיסי ושבוע 16
d SPARCC (קונסורציום המחקר Spondyloarthritis של קנדה)
** p לעומת פלצבו
* p לעומת פלצבו
שיפור מובהק סטטיסטית בסימנים ובסימפטומים של שלב פעיל חמור מספר אקסיאלי חמור הוכח בחולים שטופלו ב- Simponi 50 מ"ג בהשוואה לפלסבו בשבוע 16 (טבלה 6). השיפור נצפה בהערכה הראשונה (שבוע 4) לאחר הניהול הראשוני של סימפוני. ציון ה- MRI של SPARCC הראה ירידה מובהקת סטטיסטית בדלקת במפרק ה- SI בשבוע 16 בחולים שטופלו ב- Simponi 50 מ"ג בהשוואה לפלסבו (טבלה 6). כאבים שהוערכו על ידי כאבי גב כלליים בכאבי גב וכאבי גב לילית ופעילות מחלות כפי שנמדדו על ידי ASDAS-C הראו גם שיפור מובהק סטטיסטית מההתחלה לשבוע 16 בחולים שטופלו ב- Simponi 50 מ"ג בהשוואה לפלסבו (p
שיפור מובהק סטטיסטית בניידות עמוד השדרה כפי שהוערך על ידי BASMI (Bath Ankylosing Spondylitis Metrology Index) ובתפקוד הגופני כפי שהוערך על ידי BASFI הודגמו בחולים שטופלו ב- Simponi 50 מ"ג בהשוואה לחולים שטופלו בפלסבו (p
עבור כל נקודות הקצה המתוארות לעיל, הוכחו תוצאות מובהקות סטטיסטית גם באוכלוסיית OSI בשבוע 16.
הן באוכלוסיות AT והן ב- OSI, השיפורים בסימנים והתסמינים, ניידות עמוד השדרה, תפקוד גופני, איכות חיים ופרודוקטיביות שנצפו בשבוע 16 בקרב מטופלים שטופלו ב- Simponi 50 מ"ג נמשכו באותם חולים שנותרו במחקר. בשבוע 52.
קוליטיס כיבית
היעילות של סימפוני הוערכה בשני ניסויים קליניים אקראיים, כפולים סמיות, מבוקרי פלסבו, בחולים מבוגרים.
מחקר האינדוקציה (PURSUIT-Induction) העריך מטופלים עם קוליטיס כיבית פעילה בינונית עד חמורה (מאו ציון 6 עד 12; תת-ציון אנדוסקופי ≥ 2) אשר היו בעלי תגובה לא מספקת או שלא סבלו טיפולים קונבנציונליים או שהם תלויים בקורטיקוסטרואידים. בחלק אישור המינון של המחקר, 761 חולים חולקו באקראי לקבלת Simponi SC 400 מ"ג בשבוע 0 ו -200 מ"ג בשבוע 2, סימפוני SC 200 מ"ג בשבוע 0 ו -100 מ"ג בשבוע 2 או פלסבו SC בשבוע 0 ו- 2. ניתן מנות במקביל של מינונים יציבים של aminosalicylates אוראלי, קורטיקוסטרואידים ו / או תרופות אימונומודולטוריות. היעילות של סימפוני עד שבוע 6 הוערכה במחקר זה.
תוצאות מחקר התחזוקה (PURSUIT-Maintenance) התבססו על הערכה של 456 מטופלים שהשיגו תגובה קלינית באינדוקציה הקודמת של סימפוני. החולים חולקו באקראי לקבלת סימפוני 50 מ"ג, סימפוני 100 מ"ג או פלסבו הניתנים תת עורית כל 4 שבועות. ניתן מניה במקביל של מינונים יציבים של aminosalicylates אוראלי ו / או סוכני חיסון. הקורטיקוסטרואידים היו מופחתים בהדרגה בתחילת מחקר התחזוקה. היעילות של סימפוני הוערכה עד שבוע 54 במחקר זה. חולים שסיימו את מחקר התחזוקה עד שבוע 54 המשיכו את הטיפול במחקר אחד. הארכה, עם הערכת היעילות. עד שבוע 216. הערכת היעילות במחקר ההרחבה התבססה על שינויים בשימוש בקורטיקוסטרואידים, הערכה גלובלית של הרופא (PGA) של פעילות המחלה ושיפור באיכות החיים כפי שנמדד על ידי שאלון מחלות המעי הדלקתיות (IBDQ).
טבלה 7
תוצאות יעילות מרכזיות ממחקרי PURSUIT - אינדוקציה ו- PURSUIT - תחזוקה
N = מספר החולים
** p ≤ 0.001
* p ≤ 0.01
a מוגדר כירידה מהנקודה הבסיסית בציון מאיו של 30% ו -3 נקודות ≥, מלווה בירידה בשיעור דימום רקטאלי ≥ 1 או בתת דימום רקטלי של 0 או 1.
ב מוגדר כציון מאיו ≤ 2 נקודות, ללא ציוני משנה בודדים> 1
c מוגדר כ- 0 או 1 בתת-הציון האנדוסקופי של ציון מאיו.
ד אינדוקציה עם סימפוני בלבד.
המטופלים הוערכו לפעילות CU עם הציון החלקי של Mayo כל 4 שבועות (אובדן תגובה אושר עם אנדוסקופיה). לכן, מטופל אחד ששמר על תגובה היה במצב תגובה קלינית רציפה בכל הערכה קלינית עד שבוע 54.
f חולה היה צריך להיות בהפוגה בשבועות 30 ו -54 (לא מראה אובדן תגובה בכל נקודת זמן עד שבוע 54) כדי להשיג הפוגה מתמשכת.
g בחולים שמשקלם פחות מ -80 ק"ג, שיעור גבוה יותר של החולים שקיבלו טיפול תחזוקה של 50 מ"ג הפגין הפוגה קלינית מתמשכת מאלו שקיבלו פלסבו.
חולים נוספים שטופלו ב- Simponi הראו ריפוי מתמשך של הרירית (מטופלים עם ריפוי רירי בשבועות 30 ו -54) בקבוצת 50 מ"ג (42%, נומינלי p
בקרב 54% מהחולים (247/456) שקיבלו טיפול קורטיקוסטרואידים במקביל בתחילת ה- PURSUIT-Maintenance, שיעור החולים ששמרו על תגובה קלינית עד שבוע 54 ולא קיבלו טיפול קורטיקוסטרואידי במקביל בתחילת הטיפול ב- PURSUIT שבוע 54 היה גדול יותר בקבוצת 50 מ"ג (38%, 30/78) ובקבוצה 100 מ"ג (30%, 25/82) בהשוואה לקבוצת הפלסבו (21%, 18/87). שיעור החולים שחיסלו סטרואידים בשבוע 54 היו גדולים יותר בקבוצת 50 מ"ג (41%, 32/78) ובקבוצה 100 מ"ג (33%, 27/82) בהשוואה לקבוצת הפלסבו (22%, 19/87). כשנכנסו למחקר ההרחבה, שיעור הנבדקים שנותרו ללא קורטיקוסטרואידים נשמר בדרך כלל עד שבוע 216.
בשבוע 6, סימפוני שיפר משמעותית את איכות החיים כפי שנמדד על ידי שינוי מהבסיס במדד ספציפי למחלה, IBDQ (שאלון מחלות מעי דלקתיות). בקרב מטופלים שקיבלו טיפול תחזוקה עם סימפוני, השיפור באיכות החיים כפי שנמדד על ידי IBDQ. נשמר עד שבוע 54.
כ -63% מהחולים שקיבלו סימפוני בתחילת מחקר ההרחבה (שבוע 56) נותרו בטיפול עד תום המחקר (מתן הגלימומאב האחרון בשבוע 212).
אימונוגניות
במחקרי Phase III RA, AP ו- SA עד שבוע 52, נוגדנים לגולימומב התגלו עם האנזים אימונו-אסיאה (EIA) ב -5% (105/2062) מהחולים שטופלו בגלימומאב והיכן שנבדקו, כמעט כולם היו נוגדנים מנטרלים. בַּמַבחֵנָה. אחוזים דומים הודגשו בהתוויות הראומטולוגיות. ניהול משותף של MTX הביא לאחוז נמוך יותר של חולים עם נוגדנים לגולימומאב מאשר מטופלים שקיבלו golimumab ללא MTX (כ -3% [41/1235] לעומת 8% [64/827], בהתאמה).
ב- AxA SpA nr, נוגדנים ל- golimumab התגלו בקרב 7% (14/193) מהחולים שטופלו ב- golimumab עד שבוע 52 עם מבחן ה- EIA.
במחקרי UC II שלב II ו- III עד שבוע 54, התגלו נוגדנים ל- golimumab עם מבחן ה- EIA ב -3% (26/946) מהחולים שטופלו ב- golimumab. לשישים ושמונה אחוזים (21/31) מהחולים החיוביים לנוגדן היו נוגדנים מנטרלים בַּמַבחֵנָה. טיפול במקביל עם אימונומודולטורים (azathioprine, 6-mercaptopurine ו- MTX) הביא לאחוז נמוך יותר של חולים עם נוגדנים ל- golimumab מאשר בחולים שקיבלו golimumab ללא immunomodulators (1% (4/308) לעומת 3% (22), בהתאמה. / 638)). בקרב מטופלים שהמשיכו במחקר ההרחבה והיו להם דגימות הניתנות להערכה עד שבוע 228, זוהו נוגדנים לגולימומאב ב -4% (23/604) מהחולים שטופלו בגלימומאב. לשמונים ושניים אחוזים (18/22) מהחולים החיוביים לנוגדן היו נוגדנים מנטרלים בַּמַבחֵנָה.
במחקר pJIA נעשה שימוש במבחן EIA סובלני לסמים לאיתור נוגדנים כנגד golimumab.לאור הרגישות המוגברת ושיפור הסובלנות לתרופות, צפויה להתגלות שכיחות גבוהה יותר של נוגדנים כנגד golimumab עם מבחן ה- EIA סובלני התרופות בהשוואה למבחן ה- EIA. בניסוי שלב III ב- pIA עד שבוע 48 התגלו נוגדנים לגולימומאב עם מבחן ה- EIA סובלני סמים ב -40% (69/172) מהילדים שטופלו בגלימומאב, מתוכם לרוב היה כותרת פחות מ -1: 1,000. השפעה על ריכוזי הסרום של golimumab נצפתה ב titers> 1: 100, ואילו לא נמצאה השפעה על היעילות עד titers> 1: 1,000, אם כי מספר הילדים עם titers> 1: 1,000 היה נמוך (N = 8). ילדים שבדקו חיוביים לגבי נוגדנים כנגד golimumab, ל -39% (25/65) היו נוגדנים מנטרלים. לשכיחות גבוהה יותר של נוגדנים עם מבחן ה- EIA סובלני תרופות, בהתחשב בעובדה שהם בעיקר נוגדנים לטיטר נמוך, לא השפיעה באופן ברור על רמות התרופות, יעילות ובטיחות ולכן אינו מייצג אותות בטיחות חדשים.
הימצאות נוגדנים ל- golimumab עשויה להגביר את הסיכון לתגובות באתר ההזרקה (ראה סעיף 4.4). מספר המטופלים החיוביים של נוגדני golimumab מגביל את היכולת להסיק מסקנות נחרצות בנוגע לקשר בין נוגדנים אנטי-golimumab לבין יעילות קלינית או אמצעי בטיחות.
מכיוון שמבחני אימונוגניות הם ספציפיים למוצר ולמבחן, השוואה של אחוזי נוגדנים לאלה של מוצרים אחרים אינה מתאימה.
אוכלוסיית ילדים
דלקת מפרקים אידיופטית לנוער רב -מפרקית
הבטיחות והיעילות של סימפוני הוערכו במחקר אקראי, כפול סמיות מבוקר פלסבו (GO-KIDS) בקרב 173 ילדים (גילאי 2 עד 17) עם pJIA פעיל עם לפחות 5 מפרקים פעילים. תגובה ל- MTX. ילדים עם JIA קורס רב -מפרקי (פוליארתריטיס גורם ראומטי -חיובי או שלילי, אוליגוארתריטיס נרחבת, דלקת מפרקים פסוריאטית לנוער או JIA מערכתית ללא תסמינים סיסטמיים מתמשכים) נכללו במחקר. המספר החציוני של המפרקים הפעילים בתחילת המחקר היה 12 והחציון CRP החציוני היה 0.17 מ"ג / ד"ל.
חלק 1 של המחקר כלל שלב בן 16 שבועות פתוח שבו 173 הילדים הרשומים קיבלו סימפוני 30 מ"ג / מ"ר (מקסימום 50 מ"ג) תת עורית כל 4 שבועות ו- MTX. 154 הילדים שהשיגו תגובת ACR Ped 30 בשבוע 16 נכנסו לחלק 2 של המחקר, שלב הגמילה האקראי, וקיבלו סימפוני 30 מ"ג / מ"ר (מקסימום 50 מ"ג) + MTX או פלסבו + MTX כל 4 שבועות. לאחר התלקחות המחלה, ילדים קיבלו סימפוני 30 מ"ג / מ"ר (מקסימום 50 מ"ג) + MTX. בשבוע 48 נכנסו התינוקות לשלב הארכה ארוך טווח.
הילדים במחקר זה הראו תגובות ACR Ped 30, 50, 70 ו- 90 כבר בשבוע 4.
בשבוע 16, 87% מהילדים היו מגיבים ל- ACR Ped 30 ו- 79%, 66%, ו -36% מהילדים היו מגיבים ל- ACR Ped 50, ACR Ped 70 ו- ACR Ped 90, בהתאמה. בשבוע 16, ה -34 % מהילדים סבלו ממחלה לא פעילה המוגדרת בנוכחות כל אלה: היעדר מפרקים עם דלקת פרקים פעילה; היעדר חום, פריחה, סרוזיטיס, splenomegaly, hepatomegaly או לימפדנופתיה כללית המיוחסת ל- JIA; היעדר דלקת יובשנית פעילה;
בשבוע 16 כל רכיבי ה- ACR Ped הראו שיפור רלוונטי מבחינה קלינית מההתחלה (ראה טבלה 8).
טבלה 8
שיפורים מהבסיס ברכיבי ACR Ped בשבוע 16
בתחילת המחקר = שבוע 0
b "n" משקף מטופלים שנרשמו
c VAS: קנה מידה אנלוגי חזותי
d CHAQ: שאלת הערכת בריאות הילד
ו- ESR (מ"מ / שעה): קצב שקיעת אריתרוציטים (מילימטרים לשעה)
נקודת הסיום העיקרית של המחקר, אחוז הילדים שהיו מגיבים ל- ACR Ped 30 בשבוע 16 ואשר לא חוו החמרה בין שבוע 16 לשבוע 48, לא התקיים. לרוב הילדים לא הייתה החמרה. החמרה בין שבוע 16 ושבוע 48 (59% בקבוצת Simponi + MTX ו -53% בקבוצת פלסבו + MTX, בהתאמה; p = 0.41).
ניתוח תת-קבוצה שצוין מראש של נקודת הסיום העיקרית בהתבסס על ערכי CRP בסיסיים (≥ 1 מ"ג / ד"ל לעומת
בשבוע 48, 53% ו -55% מהילדים מקבוצת Simponi + MTX וקבוצת הפלסבו + MTX, בהתאמה, היו מגיבי ACR Ped 30, ו -40% ו -28% מהילדים מקבוצת Simponi + MTX ובפלסבו + MTX, בהתאמה, השיגה מחלה לא פעילה.
סוכנות התרופות האירופית דחתה את החובה למסור את תוצאות המחקרים עם סימפוני באוכלוסיית הילדים בדלקת קוליטיס כיבית (ראו סעיף 4.2 למידע על שימוש בילדים).
05.2 תכונות פרמקוקינטיות
קְלִיטָה
לאחר מתן יחיד של "גלימומאב תת עורית" לנבדקים בריאים או לחולי RA, הזמן הממוצע להגיע לריכוז מקסימלי בסרום (Tmax) נע בין 2 ל -6 ימים. הזרקת golimumab תת -עורית של 50 מ"ג בנבדקים בריאים הביאה ליצירת ריכוז מקסימלי בסרום. (Cmax) ± סטיית תקן של 3.1 ± 1.4 mcg / mL.
לאחר זריקה תת עורית אחת של 100 מ"ג, ספיגת golimumab הייתה דומה בזרוע, בבטן ובירך, עם ממוצע של זמינות ביולוגית מוחלטת של 51%. תת עורית, הזמינות הביולוגית המוחלטת של 50 מ"ג או 200 מ"ג Golimumab צפויה להיות דומה.
הפצה
לאחר מתן IV יחיד, נפח ההפצה הממוצע היה 115 ± 19 מ"ל / ק"ג.
חיסול
ההערכה המערכתית של golimumab הייתה 6.9 ± 2.0 מ"ל / יום / ק"ג. מחצית החיים הסופנית הוערכה כ -12 ± 3 ימים בנבדקים בריאים והיתה להם ערכים דומים בחולים עם RA, AP, SA או CU.
כאשר מנה של 50 מ גולימומאב ניתנה תת עורית לחולים עם RA, AP או AS כל 4 שבועות, ריכוזי הסרום הגיעו למצב יציב בשבוע 12. עם שימוש מקביל ב- MTX, טיפול ב- 50 מ"ג golimumab תת עורית כל 4 שבועות הניב ממוצע. (± סטיית תקן) ריכוז בסרום במצב יציב של כ -0.6 ± 0.4 מיקרוגרם / מ"ל בחולים עם RA פעיל למרות טיפול ב- MTX, כ -0.5 ± 0.4 מיקרוגרם / מ"ל בחולים עם AP פעיל וכ -0.8 ± 0.4 מיקרוגרם / מ"ל ב- חולים עם AS. Golimumab ממוצעים בריכוז נמוך בסרום של מצב חולה בחולים עם Axial SpA nr היו דומים לאלה שנצפו בחולי AS לאחר מתן תת עורית של 50 מ"ג golimumab כל 4 שבועות.
לחולים עם RA, AP או SA שלא קיבלו MTX בשילוב עם ריכוז נמוך של golimumab במצב יציב נמוך בכ -30% מזה של מטופלים שקיבלו golimumab עם MTX. במספר מצומצם של חולי RA שטופלו ב- golimumab תת עורית למשך יותר מ -6 חודשים, ניהול משותף של MTX הפחית את הסליקה לכאורה של golimumab בכ -36%. עם זאת, ניתוחים פרמקוקינטיים לאוכלוסייה מצביעים על כך ששימוש במקביל בתרופות NSAID, סטרואידים דרך הפה או sulfasalazine לא השפיע על הסליקה לכאורה של golimumab.
לאחר מינוני אינדוקציה של 200 מ"ג ו -100 מ"ג גולימומאב בשבוע 0 ו -2, בהתאמה, ולאחר מכן מנות תחזוקה של 50 מ"ג או 100 מ"ג גולימומאב תת עורית כל 4 שבועות בחולי UC, ריכוזי הסרום של גולימומאב הגיעו למצב יציב כ -14 שבועות לאחר תחילת הטיפול. טיפול עם golimumab 50 מ"ג או 100 מ"ג תת עורית כל 4 שבועות במהלך תחזוקה הביא לריכוז ממוצע של רמת סרום של רמת סרום של 0., 9 ± 0.5 מק"ג / מ"ל ו -1.8 ± 1.1 מק"ג / מ"ל, בהתאמה.
בחולי UC שטופלו ב- golimumab 50 מ"ג או 100 מ"ג תת עורית כל 4 שבועות, לשימוש בו זמני במודולי חיסון לא הייתה השפעה מהותית על רמות השוקת של מצב הגלימומאב.
למטופלים שפיתחו נוגדנים אנטי-גולימומאב היו ריכוז נמוך של סרום במצב יציב בסרום של גולימומאב (ראה סעיף 5.1).
לינאריות
Golimumab, בחולי RA, הציגה פרמטרים פרמקוקינטיים פרופורציונליים בערך במינון בטווח המינונים של 0.1 - 10.0 מ"ג / ק"ג לאחר מנה אחת תוך ורידית. לאחר מינון SC יחיד בנבדקים בריאים נצפו גם פרמטרים פרמקוקינטיים פרופורציונליים במינון בטווח המינון של 50 מ"ג עד 400 מ"ג.
השפעת המשקל על הפרמקוקינטיקה
קיימת מגמה לקראת פינוי לכאורה גבוה יותר של golimumab עם עלייה במשקל (ראה סעיף 4.2).
אוכלוסיית ילדים
פרמקוקינטיקה של Golimumab נקבעה ב -173 ילדים עם pJIA בגילאי 2 עד 17 שנים. במחקר pJIA, לילדים שטופלו בגולימומאב 30 מ"ג / מ"ר (מקסימום 50 מ"ג) תת עורית כל ארבעה שבועות היו ריכוזים נמוכים של חציון גלימומאב במצב גופני שהיו דומים בין קבוצות גיל ושהם גם דומים או מעט גבוהים מאלה שנראו ב RA מטופלים שטופלו ב- golimumab 50 מ"ג כל 4 שבועות.
מודלים פרמקוקינטיים / פרמקודינמיים וסימולציות בילדים עם pJIA אישרו את הקשר בין חשיפות בסרום של golimumab לבין יעילות קלינית ותמיכה כי משטר המינון של golimumab 50 מ"ג כל 4 שבועות לילדים עם pJIA במשקל של 40 ק"ג לפחות מאפשר לו להשיג חשיפות דומות לאלה אשר הוכח כיעיל במבוגרים.
05.3 נתוני בטיחות פרה -קליניים
נתונים לא קליניים לא חושפים שום סכנה מיוחדת לבני אדם על סמך מחקרים קונבנציונאליים בנושא פרמקולוגיה בטיחותית, רעילות של מינון חוזר, רעילות והתפתחותיות.
מוטגניות, פוריות בעלי חיים או מחקרים קרצינוגניים לטווח ארוך לא נערכו עם golimumab.
במחקר פוריות עכברים ותפקוד רבייה כללי באמצעות נוגדן דומה המעכב באופן סלקטיבי את הפעילות התפקודית של TNF עכברי?, מספר העכברים ההרות הופחת. לא ידוע אם תוצאות אלו נבעו מההשפעות. אצל גברים ו / או במחקר על רעילות אבולוציונית שנערכה בעכברים לאחר מתן אותו נוגדן אנלוגי ובקופי צינומולגוס באמצעות golimumab, לא היה כל אינדיקציה לרעילות אימהית, עוברי רעילות או טרטוגניות.
06.0 מידע פרמצבטי
06.1 מרכיבים
סורביטול (E420)
L-histidine
L-histidine מונוהידרוכלוריד מונוהידראט
פוליסורבט 80
מים להזרקות.
06.2 חוסר התאמה
בהיעדר מחקרי תאימות, אסור לערבב תרופה זו עם מוצרים אחרים.
06.3 תקופת תוקף
22 חודשים
06.4 אמצעי זהירות מיוחדים לאחסון
שומרים במקרר (2 ° C - 8 ° C).
אל תקפא.
שמור את העט הממולא או המזרק המצורף בקרטון החיצוני כדי להגן מפני אור.
06.5 אופי האריזה המיידית ותכולת האריזה
פתרון סימפוני 50 מ"ג להזרקה בעט מלא מראש
0.5 מ"ל של תמיסה במזרק מלא (זכוכית מסוג 1) עם מחט קבועה (נירוסטה) ומכסה מחט (גומי המכיל לטקס), עט מלא מראש. סימפוני זמין באריזות המכילות 1 מילוי מראש. עט ומרבדים המכילים 3 (3 אריזות של 1) עטים מלאים מראש.
פתרון סימפוני 50 מ"ג להזרקה במזרק מלא
0.5 מ"ל של תמיסה במזרק מלא (זכוכית מסוג 1) עם מחט קבועה (נירוסטה) ומכסה מחט (גומי המכיל לטקס). ניתן להשיג את סימפוני באריזות המכילות מזרק אחד ומרובה חבילות המכילות 3 (3 אריזות של 1) מזרקים מלאים מראש.
לא כל גודל האריזה עשוי להיות משווק.
06.6 הוראות שימוש וטיפול
סימפוני מסופק בעט מלא חד פעמי בשם SmartJect או במזרק מלא לשימוש חד פעמי. כל חבילת סימפוני מגיעה עם הוראות שימוש המתארות באופן מלא את השימוש בעט או במזרק. לאחר שהעט או המזרק הממולא הוצא מהמקרר, יש לאפשר לו להגיע לטמפרטורת החדר על ידי המתנה של 30 דקות לפני הזרקת סימפוני. אין לנער את העט או את המזרק.
הפתרון ברור עד מעט סמיך, חסר צבע עד צהוב בהיר ויכול להכיל חלקיקי חלבון קטנים שקופים או לבנים. זה לא יוצא דופן עבור פתרונות המכילים חלבונים.
אסור להשתמש ב- Simponi אם הפתרון שינה את צבעו, עכור או מכיל חלקיקים זרים גלויים.
הוראות מלאות להכנה וניהול סימפוני בעט מלא או במזרק מלא ניתנות בעלון האריזה.
יש להיפטר מתרופות שאינן בשימוש ופסולת המופקת מתרופה זו בהתאם לתקנות המקומיות.
מחזיק רשות השיווק 07.0
Janssen Biologics B.V.
איינשטייןווג 101
2333 CB ליידן
הולנד
08.0 מספר אישור השיווק
EU/1/09/546/001 1 עט מלא מראש
EU/1/09/546/002 3 עטים מלאים מראש
האיחוד האירופי/1/09/546/003 1 מזרק מלא מראש
EU/1/09/546/004 3 מזרקים מלאים מראש
039541014
039541026
039541038
039541040
09.0 תאריך האישור הראשון או חידוש האישור
תאריך האישור הראשון: 1 באוקטובר 2009
תאריך החידוש האחרון: 19 ביוני 2014
10.0 תאריך עיון הטקסט
02 בפברואר 2017
11.0 לתרופות רדיו, נתונים מלאים על מינון הקרינה הפנימי
12.0 לתרופות רדיו, הוראות מפורטות נוספות בנושא הכנה זמנית ובקרת איכות.
























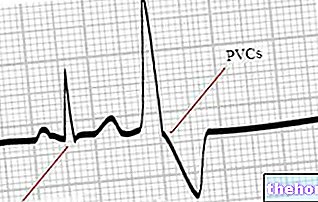

-e-bpco.jpg)

