ניתן לנהל כמה תכונות של הנטינגטון באמצעות:
- טיפול בדיבור, פסיכותרפיה ושיקום קוגניטיבי יכולים לשפר את התסמינים הפיזיים והפסיכולוגיים של המחלה. בפרט, טיפולים אלה מועילים לסיוע בתקשורת ולביצוע האוטונומי של פעילויות יומיומיות. הבנה טובה יותר של הפרעות התנהגותיות וקוגניטיביות יכולה לסייע גם בפיתוח אסטרטגיות להתאמה לשינויים הנגרמים על ידי התקדמות מחלת הנטינגטון;
- פיזיותרפיה ופעילות גופנית סדירה: תורמים לשמירה על תיאום התנועה. בשלבים המוקדמים של המחלה, מומלץ לבצע פעילות גופנית עדינה (שחייה, הליכה וכו ');
- שימוש בעזרים ספציפיים כדי לסייע לחולי מחלת הנטינגטון, החווים קשיי תיאום, ללכת באופן עצמאי;
- תרופות: הן מצוינות כאשר מתרחשים תסמינים חשובים. לדוגמה, ניתן לדכא חלקית את התפקוד ואת התסיסה עם תרופות החוסמות או מרוקנות קולטני דופמין. עם זאת, תרופות רבות יכולות לגרום לתופעות לוואי, כמו גם להשפעות שונות אצל מטופלים שונים. לכן יש לקבוע את האיזון האידיאלי של הטיפול התרופתי. כל מקרה לגופו של הרופא המומחה, על סמך סימפטומים ותגובה פרטנית לטיפולים.
, בטיפול במחלת הנטינגטון. השלב הקליני הוא תובעני מאוד, בעיקר מכיוון שלמחלה יש התקדמות איטית ו"הטרוגניות קלינית רחבה. ישנם סדרי הערכה של מחלת הנטינגטון והם כמעט זהים בכל המרפאות. חדירת המחלה המלאה וזמינותה של בדיקות. גנטיקה מנבאת, היא מציעה את ההזדמנות לנסות טיפול במהלך השלבים הראשונים של המחלה. נכון לעכשיו, המחקרים מכוונים לחיפוש אחר סמני ביור רגישים ויציבים של שינוי, על מנת להתערב בביטויים הראשונים של המחלה.
נכון לעכשיו, טכניקות הדמיה עצבית הציעו את הסמנים הביולוגיים הטובים ביותר במהלך השלב הפרודרומי (שקדם לסימפטומים הקליניים של המחלה); יתר על כן, הם מספקים מתאם בין הטיפולים שנעשו על מודלים של בעלי חיים ועל בני אדם.
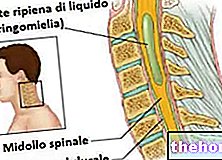
כאמור, ניוון הסטריאטום מוקדם ומתקדם במהלך המחלה.הוכח כי אזורים אחרים במוח כגון מבני החומר הלבן תת -קליפת המוח וקורטיקלית מושפעים גם בתקופה הפרודרומית.
באמצעות הדמיה תפקודית היא יכולה גם לזהות הפרעות מסוימות באנשים במהלך התקופה הפרודרומלית.טכניקה זו עשויה גם להיות רגישה מספיק כדי לזהות אי סדרים במבנה או שינויים בהתנהגות.
לבסוף, הזיהוי של סמנים ביולוגיים מולקולריים, כגון לקטט או מוצרי לחץ תאיים אחרים, יתאפשר הודות לטכניקות ספקטרוסקופיה של תהודה מגנטית.
הניוון הסלקטיבי של נוירונים במחלת הנטינגטון טרם הובהר במלואו; לכן, יש צורך לחקור אסטרטגיות טיפוליות חדשות אפשריות. בפרט, נמצא כי במחלת הנטינגטון יש אובדן סלקטיבי של קולטני קנבינואידים מסוג CB1 בגרעיני הבסיס, המייצגים את אחד השינויים הנוירוכימיים המוקדמים ביותר. מסיבה זו, מחקרי מחקר חוקרים כיום את התפקיד הנוירו -הגנתי של הקנבינואידים במחלת הנטינגטון.
למידע נוסף: קולטנים קנבינואידיםמחלת הנטינגטון: קולטני CB1
מעורבותה של מעורבות המערכת האנדוקנבינואידית, במיוחד קולטני CB1, במחלת הנטינגטון. אכן, הוכח כי אחד השינויים הראשונים הניכרים באנשים שנפגעו מהמחלה הוא אובדן סלקטיבי של קולטני CB1 בגרעיני הבסיס. נצפה שינוי הן בביטוי קולטן CB1 והן ברמות האנדוקנבינואידים. עדויות אלה הובילו להשערה כי חוסר ויסות של המערכת האנדוקנבינואידית יכול לייצג יעד לפיתוח אסטרטגיות טיפוליות חדשות.
במחקרים שנעשו לאחרונה הוכח כי מחיקת קולטני CB1 במודלים טרנסגניים למחלת הנטינגטון גרמה להחמרה של הפנוטיפ המוטורי, ל"ניוון סטריאטום והצטברות של חלבון האנטין, בעוד טיפול כרוני באגוניסט קנאביס. , tetrahydrocannibol (Δ9-THC), היה מועיל.
לבסוף, קולטני CB1 מתבטאים מאוד בנוירונים GABAergic, המהווים 90-95% מהנוירונים בסטריאטום, אזור המוח שנפגע במחלת הנטינגטון, כפי שהוסבר בפסקאות הקודמות.
גירוי קולטני CB1 מוביל לירידה בשחרורו של המוליך הנוירוטרנסמיטר המעכב GABA. הפחתה זו עלולה להזיק לחולים שנפגעו ממחלת הנטינגטון, בהתחשב בכך שעל ידי הפחתת הטון המעכב המופעל על ידי GABA, תהיה עלייה מופרזת בטון המעורר, הנקבע על ידי גלוטמט, וכתוצאה מכך לתופעה של אקסיטוטוקסיות. סבורים כי אקסיטוטוקסיות תורמת למוות של נוירונים הקרנה בסטריאטום. עם זאת, קולטני CB1 ממוקמים גם בנוירונים של גלוטמט, אם כי במידה פחותה. ההשערה היא שגירוי של קולטנים אלה יוביל גם לשחרור נמוך יותר של גלוטמט. העובדה שטיפול כרוני ב- Δ9-THC היה מועיל עולה כי התרומה של קולטני CB1 בתיווך התגובה לאגוניסטים של קנבינואידים בנוירונים ספציפיים עשויה להשתנות בהתקדמות המחלה.
סיכויי עתיד
נכון לעכשיו, החיפוש אחר תרופה למחלת הנטינגטון פעיל וכמה ניסויים קליניים מתבצעים להערכת יעילותם של גורמים פרמקולוגיים שונים ו / או גישות לא תרופתיות (למשל טיפול גנטי, השתלת תאי גזע) המסוגלות להפחית את ייצור האנטין. או לשפר את הישרדות העצבים, למנוע או להאט את התקדמות המחלה.
לדוגמה, השתקת גנים באמצעות הפרעות RNA (RNAi) או oligonucleotides antisense (ASO). ה- ASO נקשרים, בפרט, ל"- RNA שליח הנושא מידע "מהגן המוטה, חוסם את התרגום שלו וממריץ את התדרדרותו כך שחלבון האנטינגטין לא ייוצר. טיפול בתאי גזע, לעומת זאת, מורכב מהחלפת נוירונים פגועים, הודות להשתלת תאי גזע, באזורים המוחים של המוח. ניסויים במודלים של בעלי חיים ובניסויים קליניים מקדימים הניבו תוצאות סותרות עם טכניקה זו, ולכן יש צורך בראיות נוספות כדי לבסס את יעילותה.
בִּיבּלִיוֹגְרָפִיָה
- Caron, N.S., רייט, G.E.B. והיידן, מ.ר. מחלת הנטינגטון. GeneReviews ((R)) מחלת הנטינגטון. סיאטל (וושינגטון), 2018.
- נוירוביול דיס. 2012 מרץ; 45: 983-91. doi: 10.1016 / j.nbd.2011.12.017. Epub 23. דצמבר 23. חוסר איזון של קולטני CB1 המתבטאים בנוירונים GABAergic וגלוטמטרגיים במודל עכבר מהונדס של מחלת הנטינגטון. Chiodi V, Uchigashima M, Beggiato S, Ferrante A, Armida M, Martire A, Potenza RL, Ferraro L, Tanganelli S, Watanabe M, Domenici MR, Popoli P.