מרכיבים פעילים: בורטזומיב
אבקת VELCADE 3.5 מ"ג לתמיסה להזרקה.
אינדיקציות מדוע משתמשים ב- Velcade? לשם מה זה?
VELCADE מכיל את החומר הפעיל בורטזומיב, מה שמכונה "מעכב פרוטאזום". הפרוטאזומים ממלאים תפקיד חשוב בשליטה על תפקוד התא וצמיחתו. על ידי הפרעה לתפקודם, בורטזומיב יכול להרוג תאים סרטניים.
VELCADE משמש לטיפול במיאלומה נפוצה (סוג של ממאירות של מח עצם) בחולים מעל גיל 18:
- לבד או יחד עם התרופות הדוקסורוביצין או דקסמתזון, ליפוזומלי, לחולים הסובלים ממחלה מחמירה (מתקדמת) לאחר שקיבלו טיפול אחד לפחות או שהשתלת תאי גזע בדם נכשלה או שאינה אפשרית.
- בשילוב עם התרופות מלפלן ופרדניזון לחולים עם מחלה שטרם טופלה אשר אינם יכולים לקבל כימותרפיה במינון גבוה עם השתלת תאי גזע בדם.
- בשילוב עם דקסמתזון או דקסמתזון יחד עם תלידומיד, לחולים עם מחלה שטרם טופלה ולפני קבלת כימותרפיה במינון גבוה עם השתלת תאי גזע בדם (טיפול אינדוקציה)
VELCADE משמש לטיפול בלימפומה של תאי מעטה (סוג ממאיר המשפיע על בלוטות הלימפה) בחולים בגילאי 18 ומעלה. במקרה זה, VELCADE משמשת בשילוב עם התרופות rituximab, cyclophosphamide, doxorubicin ו- prednisone, לחולים עם מחלה שטרם טופלה ועבורם השתלת תאי גזע בדם אינה אפשרית.
התוויות נגד כאשר אין להשתמש ב- Velcade
אין להשתמש ב- VELCADE
- אם אתה אלרגי לבורטזומיב, בורון או כל אחד ממרכיבי התרופה האחרים (מופיע בסעיף 6)
- אם יש לך בעיות ריאה או לב חמורות.
אמצעי זהירות לשימוש מה שאתה צריך לדעת לפני נטילת Velcade
ספר לרופא אם יש לך:
- מספר נמוך של תאי דם אדומים או תאי דם לבנים
- בעיות דימום ו / או ספירת טסיות דם נמוכה
- שלשולים, עצירות, בחילות או הקאות
- חוויות קודמות של התעלפות, סחרחורת או סחרחורת
- בעיות כליה
- בעיות בכבד בינוניות עד חמורות
- תלונות קודמות כגון קהות, עקצוצים או כאבים בידיים או ברגליים (נוירופתיה)
- הפרעת לב או לחץ דם
- קוצר נשימה או שיעול
- עוויתות
- שלבקת חוגרת (ממוקמת גם סביב העיניים או מתפשטת לשאר הגוף)
- תסמינים של תסמונת תמוגה של גידולים כגון למשל התכווצויות שרירים, חולשת שרירים, בלבול, הפרעה בראייה או אובדן ראייה וקוצר נשימה
- אובדן זיכרון, קשיי חשיבה, קשיי הליכה או אובדן ראייה. אלה יכולים להיות סימנים לזיהום חמור במוח, והרופא שלך עשוי להצביע על בדיקות ובדיקות נוספות.
יהיה עליך לבצע בדיקות דם באופן קבוע לפני ובמהלך הטיפול ב- VELCADE כדי לבדוק כל הזמן את ערכי תאי הדם שלך.
אם יש לך לימפומה של תאי מעטפת ונותנת לך ריטוקסימאב יחד עם VELCADE עליך לספר לרופא:
- אם אתה חושב שיש לך הפטיטיס או שחלת בעבר. במקרים מסוימים, חולים שסבלו מהפטיטיס B עלולים להתקף התקף חדש של הפטיטיס שעלול להיות קטלני. אם הייתה לך דלקת הפטיטיס B בעבר, הרופא יצטרך לעקוב אחריך אחר סימנים ותסמינים של הפטיטיס פעילה. ב.
קרא את עלוני החבילות של כל התרופות שאתה לוקח בשילוב עם VELCADE למידע על תרופות אלו לפני תחילת הטיפול ב- VELCADE.
כאשר VELCADE ניתנת יחד עם התרופה thalidomide, יש לשים לב במיוחד לייעוץ בנושא בדיקות הריון והתוכנית למניעת הריון (ראה "הריון והנקה" בסעיף זה).
ילדים ומתבגרים
אין להשתמש ב- VELCADE לילדים ובני נוער מכיוון שלא ידוע כיצד פועלת התרופה באנשים אלה.
אינטראקציות אילו תרופות או מזונות יכולים לשנות את השפעת הוולקייד
ספר לרופא או לרוקח אם אתה נוטל או נטלת לאחרונה תרופות אחרות.
בפרט, ספר לרופא אם אתה משתמש בתרופות המכילות את כל החומרים הפעילים הבאים:
- קטוקונזול, המשמש לטיפול בזיהומים פטרייתיים
- ריטונוויר, המשמש לטיפול בזיהום HIV - ריפמפיצין, אנטיביוטיקה המשמשת לטיפול בזיהומים חיידקיים
- carbamazepine, phenytoin או phenobarbital, המשמשים לטיפול באפילפסיה
- ג 'ון סנט (Hypericum perforatum), המשמש לטיפול בדיכאון או במצבים אחרים
- תרופות נוגדות סוכרת דרך הפה.
אזהרות חשוב לדעת כי:
הריון והנקה
אין להשתמש ב- VELCADE אם הינך בהריון, אלא אם כן יש צורך בכך בבירור.
גברים ונשים בטיפול VELCADE צריכים להשתמש באמצעי מניעה יעילים במהלך ועד 3 חודשים לאחר הטיפול. אם, למרות אמצעי זהירות אלה, אתה נכנס להריון, דווח לרופא מיד.
אסור להניק בזמן נטילת VELCADE. שוחח עם הרופא שלך על הזמן הטוב ביותר להתחיל להניק שוב לאחר סיום הטיפול.
התרופה thalidomide גורמת למומים מולדים ולמוות העובר. כאשר VELCADE ניתנת בשיתוף עם תאלידומיד, עליך לעקוב אחר התוכנית למניעת הריון תלידומיד (ראה עלון תכלידומיד).
נהיגה ושימוש במכונות
VELCADE יכול לגרום לעייפות, סחרחורת, התעלפות או ראייה מטושטשת. אין לנהוג במכוניות או להשתמש במכונות אם אתה נתקל באחד מהתסמינים הללו. שימו לב גם אם תופעות אלה אינן מתרחשות.
מינון, אופן וזמן הניהול אופן השימוש בוולקייד: מינון
הרופא שלך יחשב את המינון של VELCADE ביחס לגובה ולמשקל שלך. המינון ההתחלתי הסטנדרטי של VELCADE הוא 1.3 מ"ג / מ"ר שטח גוף פעמיים בשבוע. הרופא שלך עשוי לשנות את המינון ואת המספר הכולל של קורסי הטיפול בהתאם לתגובתך לטיפול, הופעת תופעות לוואי מסוימות ומצבי הבריאות הכלליים שלך (למשל בעיות בכבד).
מיאלומה נפוצה בהתקדמות
כאשר VELCADE ניתנת לבד, תקבל 4 מנות של VELCADE תוך ורידי או תת עורית בימים 1, 4, 8 ו 11. לאחר מכן תקופת "כבוי" של 10 ימים ללא טיפול.
תקופה זו של 21 ימים (3 שבועות) מתאימה לקורס טיפול אחד.
אתה יכול לקבל עד 8 מחזורים (24 שבועות). אתה עשוי גם לקבל VELCADE יחד עם תרופות דוקסורובצין ליפוזומליות או דקסמתזון.
כאשר ניתנת VELCADE יחד עם דוקסורוביצין ליפוזומלי מפוגל, תקבל קורס של 21 יום של VELCADE תוך ורידי או תת עורית ו -30 מ"ג / מ"ר של דוקסורובצין ליגוזומלי מוגדר יינתן ביום 4 למחזור הטיפול בן 21 הימים של VELCADE כעירוי. תוך ורידי לאחר הזרקת VELCADE.
אתה יכול לקבל עד 8 מחזורים (24 שבועות של טיפול).
כאשר VELCADE ניתנת בשיתוף עם דקסמתזון, תקבל קורס של 21 יום עם VELCADE תוך ורידי או תת עורי ודקסמתזון אוראלי במינון של 20 מ"ג בימים 1, 2, 4, 5, 8, 9, 11 ו -12, של מהלך הטיפול בן 21 הימים ב- VELCADE.
אתה יכול לקבל עד 8 מחזורים (24 שבועות של טיפול).
מיאלומה נפוצה שלא טופלה בעבר
אם מעולם לא טופלת בעבר במיאלומה נפוצה ואינך מועמד להשתלת תאי גזע בדם, תקבל VELCADE יחד עם שתי תרופות נוספות: מלפלן ופרדניזון.
במקרה זה, משך הטיפול הוא 42 ימים (6 שבועות). הוא יקבל 9 מחזורים (54 שבועות).
- במחזורים 1-4, VELCADE ניתנת פעמיים בשבוע בימים 1, 4, 8, 11, 22, 25, 29 ו -32.
- במחזורים 5-9, VELCADE ניתנת פעם בשבוע בימים 1, 8, 22 ו -29.
מלפלן (9 מ"ג / מ"ר) ופרדניזון (60 מ"ג / מ"ר) ניתנים על ידי הפה בימים 1, 2, 3 ו -4 בשבוע הראשון של כל מחזור.
אם מעולם לא טופלת בעבר במיאלומה נפוצה ואתה מועמד להשתלת תאי גזע בדם, תקבל VELCADE תוך ורידי או תת עורי יחד עם התרופות: דקסמתזון, או דקסמתזון ותלידומיד, כטיפול אינדוקציה.
כאשר VELCADE ניתנת בשיתוף עם דקסמתזון, תקבל קורס טיפול בן 21 יום עם VELCADE תוך ורידי או תת עורי ו -40 מ"ג דרך הפה בימים 1, 2, 3, 4, 8, 9, 10 ו -11 של המחזור. -טיפול VELCADE ביום.
תקבל 4 מחזורים (12 שבועות של טיפול).
כאשר VELCADE ניתנת יחד עם תאלידומיד ודקסמתזון, משך קורס הטיפול הוא 28 ימים (4 שבועות).
Dexamethasone 40 מ"ג ניתנת דרך הפה בימים 1, 2, 3, 4, 8, 9, 10 ו -11 של מחזור הטיפול של 28 ימים עם VELCADE ותאלידומיד ניתנת דרך הפה במינון של 50 מ"ג ליום עד יום 14 הראשון של המחזור הראשון מחזור, ואם הוא נסבל, מינון התאלידומיד מוגדל ל -100 מ"ג בימים 15-28 ולאחר מכן ניתן להגדיל אותו עד 200 מ"ג ליום מהמחזור השני ואילך. אתה יכול לקבל עד 6 מחזורים (24 שבועות של טיפול).
לימפומה של תאי מעטפת שלא טופלה בעבר
אם מעולם לא קיבלת טיפול ספציפי בלימפומה של תאי מעטפת בעבר, תקבל VELCADE תוך ורידי או תת עורי יחד עם התרופות rituximab, cyclophosphamide, doxorubicin ו- prednisone.
VELCADE ניתנת תוך ורידי או תת עורית בימים 1, 4, 8 ו -11, ואחריה תקופת "מנוחה" ללא טיפול. משך הקורס הטיפולי הוא 21 ימים (3 שבועות).
תוכל לקבל עד 8 קורסי טיפול (24 שבועות).
התרופות הבאות ניתנות ביום 1 של כל מחזור טיפול של 21 ימים של VELCADE כעירוי תוך ורידי: ריטוקסימב 375 מ"ג / מ"ר, ציקלופוספמיד 750 מ"ג / מ"ר ודוקסורוביצין 50 מ"ג / מ"ר.
פרדניזון ניתנת דרך הפה במינון של 100 מ"ג / מ"ר בימים 1, 2, 3, 4 ו -5 של מחזור הטיפול ב- VELCADE.
כיצד ניתן VELCADE
תרופה זו מיועדת לווריד או תת עורית. VELCADE תינתן על ידי רופא בעל ניסיון עם שימוש בתרופות ציטוטוקסיות. אבקת ה- VELCADE חייבת להיות מומסת לפני הניהול. הדבר ייעשה על ידי רופא. לאחר מכן מוזרק את הפתרון המתקבל במהירות לווריד או תת עורית. הזרקת L "לווריד היא מהירה, על פני תקופה של 3 עד 5 שניות. הזריקה תת עורית יכולה להתבצע בירך או בבטן.
מנת יתר מה לעשות אם נטלת יותר מדי וולקייד
מכיוון שתרופה זו ניתנת על ידי הרופא או האחות שלך לא סביר שתיקח יותר ממה שאתה צריך. במקרה לא סביר של מנת יתר, הרופא יעקוב אחר תופעות לוואי.
תופעות לוואי מהן תופעות הלוואי של הוולקייד
כמו כל התרופות, תרופה זו עלולה לגרום לתופעות לוואי, אם כי לא כולם מקבלים אותן. חלק מההשפעות הללו עלולות להיות חמורות.
אם ניתנת לך VELCADE עבור מיאלומה נפוצה או לימפומה של תאי מעטפת, דווח לרופא מיד אם אתה מבחין באחד מהתסמינים הבאים:
- התכווצויות שרירים, חולשת שרירים
- בלבול, אובדן מופרע או ראייתי, עיוורון, התקפים, כאבי ראש
- קוצר נשימה, נפיחות בכפות הרגליים או שינויים בקצב הלב, לחץ דם גבוה, עייפות, התעלפות
- שיעול וקשיי נשימה או לחץ בחזה.
טיפול ב- VELCADE יכול בדרך כלל לגרום לירידה במספר כדוריות הדם האדומות והלבנות וטסיות הדם. לכן, תצטרך לבצע בדיקות דם באופן קבוע לפני ובמהלך הטיפול ב- VELCADE, כדי לבדוק את ספירת תאי הדם שלך באופן קבוע. אתה עשוי לחוות הפחתה במספר:
- טסיות הדם עלולות לגרום לך להיות חשוף יותר לחבורות או לדימומים ללא פגיעה ניכרת (למשל דימום במעיים, בקיבה, בפה ובחניכיים או בדימום במוח או בכבד)
- תאי דם אדומים שיכולים לגרום לאנמיה, עם תסמינים כגון עייפות וחיוורון
- תאי דם לבנים שיכולים לגרום לך להיות רגישים יותר לזיהומים או לתסמינים דמויי שפעת.
אם ניתנת לך VELCADE לטיפול במיאלומה נפוצה, תופעות הלוואי שעלולות להתרחש מפורטות להלן.
תופעות לוואי שכיחות מאוד (עשויות להשפיע על יותר מ -1 מתוך 10 אנשים)
- רגישות, קהות, תחושת עקצוץ או צריבה של העור, או כאבים בידיים או ברגליים, עקב נזק עצבי.
- הפחתה במספר כדוריות הדם האדומות ו / או הלבנות (ראו לעיל).
- חום.
- תחושת בחילה או הקאות, חוסר תיאבון.
- עצירות עם או בלי עודף גז (יכולה להיות חמורה).
- שלשולים: אם זה קורה חשוב שתשתו הרבה יותר מים מהרגיל. הרופא שלך עשוי לרשום תרופות לשליטה על שלשול.
- עייפות (עייפות), תחושת חולשה.
- כאבי שרירים, כאבי עצמות.
תופעות לוואי שכיחות (עשויות להשפיע על עד 1 מתוך 10 אנשים)
- לחץ דם נמוך, ירידה פתאומית בלחץ הדם בעמידה שעלולה להוביל לעילפון.
- לחץ דם מוגבר.
- תפקוד מופחת של הכליות.
- כְּאֵב רֹאשׁ.
- תחושה כללית לא טובה, כאב, סחרחורת, סחרחורת, תחושת חולשה או אובדן הכרה.
- צְמַרמוֹרֶת.
- זיהומים, כולל דלקת ריאות, דלקות בדרכי הנשימה, ברונכיטיס, זיהום פטרייתי, שיעול עם ליחה, מחלה דמוית שפעת.
- זיהום הרפס זוסטר (מקומי, כולל סביב העיניים, או התפשט על הגוף).
- כאבים בחזה או קשיי נשימה במהלך פעילות גופנית.
- סוגים שונים של פריחה בעור (פריחה).
- עור מגרד, גושים בעור או עור יבש.
- אדמומיות בפנים או שבירות קטנות בנימים.
- אדמומיות העור.
- התייבשות.
- צרבת, נפיחות, גיהוקים, גזים, כאבי בטן, דימום במעי או בקיבה.
- שינוי תפקוד הכבד.
- גירוי בפה או בשפתיים, יובש בפה, כיבים בפה או כאב גרון.
- ירידה במשקל, ירידה בטעם.
- התכווצויות שרירים, התכווצויות שרירים, חולשת שרירים, כאבים בזרועות וברגליים.
- ראייה מטושטשת.
- זיהום השכבה החיצונית ביותר של העיניים והמשטח הפנימי של העפעפיים (דלקת הלחמית).
- דימום באף (דימום).
- הפרעות שינה או בעיות, הזעה, חרדה, שינויים במצב הרוח, מצב רוח מדוכא, אי שקט או תסיסה, שינויים במצב הנפשי, חוסר התמצאות.
- נפיחות בגוף, כולל נפיחות סביב העיניים וחלקים אחרים של הגוף.
תופעות לוואי לא שכיחות (עשויות לפגוע בעד אחד מכל 100 אנשים)
- אי ספיקת לב, התקף לב, כאבים בחזה, אי נוחות בחזה, עלייה או ירידה בקצב הלב.
- אי ספיקת כליות.
- דלקת בווריד, קרישי דם בוורידים ובריאות.
- בעיות קרישת דם.
- כשל במחזור הדם.
- דלקת הקרום המקיפה את הלב או נוכחות נוזלים סביב הלב.
- זיהומים הכוללים דלקות בדרכי השתן, שפעת, דלקות נגיף הרפס, דלקות אוזניים וצלוליטיס.
- דם בצואה, או דימום של הריריות כגון הפה, הנרתיק.
- הפרעות מוחיות.
- שיתוק, עוויתות, נפילה, הפרעות בתנועה, רגישות חריגה, שונה או מופחתת (תחושה, שמיעה, טעימה, ריח), הפרעת קשב, רעד, עוויתות.
- דלקת פרקים, כולל דלקת במפרקי האצבעות, בהונות ולסת.
- הפרעות המשפיעות על הריאות, ומונעות מגופך לקבל מספיק חמצן. חלק מאלה כוללים קשיי נשימה, קוצר נשימה, צפצופים גם ללא פעילות גופנית, קושי בנשימה רדודה או צורך להפסיק, צפצופים.
- שיהוקים, הפרעות בדיבור.
- ייצור שתן מוגבר או מופחת (נזק לכליות), שתן כואבת או דם / חלבון בשתן, אגירת נוזלים.
- רמות תודעה, בלבול, פגיעה בזיכרון או אובדן.
- רגישות יתר.
- אובדן שמיעה, חירשות או צלצולים באוזניים, אי נוחות באוזן.
- שינויים הורמונליים שיכולים להשפיע על ספיגה חוזרת של מלחים ומים.
- היפראקטיביות של בלוטת התריס.
- חוסר יכולת לייצר מספיק אינסולין או עמידות לרמות אינסולין תקינות.
- עיניים כואבות או דלקתיות, עיניים רטובות מדי, כאבי עיניים, עיניים יבשות, דלקות עיניים, הפרשות עיניים, הפרעות בראייה, דימום בעיניים.
- בלוטות לימפה מוגדלות.
- נוקשות מפרקים או שרירים, תחושת כבדות, כאבי מפשעה.
- נשירת שיער או מרקם שיער לא תקין.
- תגובות אלרגיות.
- אדמומיות או כאבים באתר ההזרקה.
- כאב בפה.
- זיהום או דלקת בפה, כיבים בפה, הוושט, הקיבה והמעיים הקשורים לעיתים בכאבים או בדימומים, פגיעה בתנועתיות המעיים (כולל חסימת מעיים), אי נוחות בבטן או בוושט, קשיי בליעה, הקאות דם.
- זיהומים בעור.
- זיהומים חיידקיים ויראליים.
- זיהום בשיניים.
- דלקת בלבלב, חסימה של צינורות המרה.
- כאבים באברי המין, בעיות זקפה.
- עלייה במשקל.
- מרגיש צמא.
- דַלֶקֶת הַכָּבֵד.
- הפרעות באתר ההזרקה או באתר הקטטר.
- תגובות עור או הפרעות (שיכולות להיות חמורות ומסכנות חיים), כיבים בעור.
- חבלות, נפילות ופציעות.
- דלקת או דימום של כלי דם אשר עשויים להתבטא כנקודות אדומות או סגולות קטנות (בדרך כלל על הרגליים) אשר עלולות להפוך לדומות לחבלות גדולות בעור או ברקמה.
- ציסטות שפירות.
- מצב חמור והפיך של המוח הכולל התקפים, לחץ דם גבוה, כאבי ראש, עייפות, בלבול, עיוורון או בעיות ראייה אחרות.
תופעות לוואי נדירות (עשויות להופיע עד 1 מתוך 1,000 אנשים)
- בעיות לב כולל התקף לב, אנגינה.
- שוטפים.
- שינוי צבע הוורידים.
- דלקת בעצב השדרה.
- בעיות אוזניים, דימום מהאוזן.
- פעילות מופחתת של בלוטת התריס.
- תסמונת באד-צ'יארי (סימנים קליניים נגרמים כתוצאה מחסימה של ורידי הכבד).
- שינוי או תפקוד מעיים לא תקין.
- דימום מוחי (דימום).
- שינוי צבע צהוב של העיניים והעור (צהבת).
- סימנים של תגובה אלרגית חמורה (הלם אנפילקטי) כוללים קשיי נשימה, כאבים בחזה או לחץ בחזה ו / או תחושת סחרחורת / חולשה, עור מגרד חמור או גושים בעור, נפיחות בפנים, בשפתיים, בלשון ו / או בגרון שעלולות לגרום קושי בבליעה, התמוטטות.
- הפרעות בחזה.
- הפרשות מהנרתיק.
- נפיחות של איברי המין.
- חוסר יכולת לסבול צריכת אלכוהול.
- בזבוז או אובדן מסת גוף.
- תיאבון מוגבר.
- פיסטולות.
- נפיחות משותפת.
- ציסטה על הממברנה המכסה את המפרקים (ציסטות סינוביאליות).
- שברים.
- פירוק סיבי שריר המוביל לסיבוכים אחרים.
- כבד מוגדל, דימום בכבד.
- סרטן הכליות.
- מצב עור דומה לפסוריאזיס.
- סרטן העור.
- חיוורון של העור.
- עלייה בטסיות או בתאי פלזמה (סוג של כדוריות דם לבנות) בדם.
- תגובה חריגה לעירוי דם.
- אובדן ראייה חלקי או מוחלט.
- ירידה בחשק המיני.
- אובדן רוק.
- בליטת עיניים.
- פוטופוביה (רגישות מוגזמת של העין לאור).
- נשימה מהירה.
- כאבים בפי הטבעת.
- אבני מרה.
- בֶּקַע.
- פציעות.
- ציפורניים שבירות או חלשות.
- תצהיר חלבון לא תקין באיברים חיוניים.
- תרדמת.
- כיבים במעיים.
- פגיעה במספר איברים.
- מוות.
אם ניתנת לך VELCADE יחד עם תרופות אחרות לטיפול בלימפומה של תאי מעטפת, תופעות הלוואי שעלולות להתרחש מפורטות להלן.
תופעות לוואי שכיחות מאוד (עשויות להשפיע על יותר מ -1 מתוך 10 אנשים)
- דלקת ריאות.
- אובדן תיאבון.
- רגישות, קהות, תחושת עקצוץ או צריבה של העור, או כאבים בידיים או ברגליים, עקב נזק עצבי.
- בחילות והקאות.
- שִׁלשׁוּל.
- כיבים בפה.
- עצירות מעיים.
- כאבי שרירים, כאבי עצמות.
- נשירת שיער או מרקם שיער לא תקין.
- עייפות, תחושת חולשה.
- חום.
תופעות לוואי שכיחות (עשויות להשפיע על עד 1 מתוך 10 אנשים)
- זיהום הרפס זוסטר (מקומי, כולל סביב העיניים או התפשט על הגוף).
- זיהום בנגיף הרפס.
- זיהומים חיידקיים ויראליים.
- דלקות נשימה, ברונכיטיס, שיעול עם ליחה, מחלה דמוית שפעת.
- זיהומים פטרייתיים.
- רגישות יתר (תגובה אלרגית).
- חוסר יכולת לייצר מספיק אינסולין או עמידות לרמות אינסולין תקינות.
- החזקת מים.
- קשיים או בעיות שינה.
- אובדן ההכרה.
- רמות מודעות שונות, בלבול.
- סחרחורת.
- קצב לב מוגבר, לחץ דם גבוה, הזעה.
- הפרעות ראייה, ראייה מטושטשת.
- אי ספיקת לב, התקף לב, כאבים בחזה, אי נוחות בחזה, עלייה או ירידה בקצב הלב.
- לחץ דם גבוה או נמוך.
- ירידה פתאומית בלחץ הדם בעמידה שעלולה להוביל לעילפון.
- קוצר נשימה במהלך פעילות גופנית.
- לְהִשְׁתַעֵל.
- לְשַׁהֵק.
- צלצולים באוזניים, אי נוחות באוזן.
- דימום במעי או בקיבה.
- כאב בטן.
- כאבי בטן, נפיחות.
- קושי בבליעה.
- זיהום או דלקת בקיבה ובמעיים.
- כאב בטן.
- גירוי בפה או בשפתיים, כאב גרון.
- שינוי תפקוד הכבד.
- עור מגרד.
- אדמומיות העור.
- פריחה.
- התכווצות שרירים.
- דלקת בדרכי שתן.
- כאבים בגפיים.
- נפיחות בגוף, כולל נפיחות סביב העיניים וחלקים אחרים של הגוף.
- צְמַרמוֹרֶת.
- אדמומיות וכאבים באתר ההזרקה.
- תחושת חולשה כללית.
- ירידה במשקל הגוף.
- עלייה במשקל הגוף.
תופעות לוואי לא שכיחות (עשויות לפגוע בעד אחד מכל 100 אנשים)
- דַלֶקֶת הַכָּבֵד.
- תגובה אלרגית חמורה (תגובה אנפילקטית) אשר סימניה עשויים לכלול קשיי נשימה, כאבים בחזה או לחץ בחזה, ו / או תחושת סחרחורת / חולשה, עור מגרד או גושים בעור, נפיחות בפנים, בשפתיים, בלשון ו / או גרון שעלול לגרום לקושי בבליעה, קריסה.
- הפרעות בתנועה, שיתוק, התכווצויות.
- סְחַרחוֹרֶת.
- אובדן שמיעה, חירשות.
- הפרעות המשפיעות על הריאות, ומונעות מגופך לקבל מספיק חמצן. חלק מאלה כוללים קשיי נשימה, קוצר נשימה, צפצופים גם ללא פעילות גופנית, נשימה שהופכת רדודה, קשה או מפסיקה, צפצופים.
- קרישי דם בריאות.
- שינוי צבע צהוב של העיניים והעור (צהבת).
דיווח על תופעות לוואי
אם אתה נתקל בתופעות לוואי כלשהן, דבר עם הרופא או הרוקח שלך. זה כולל כל תופעות לוואי אפשריות שאינן מופיעות בעלון זה. תוכל גם לדווח על תופעות לוואי ישירות באמצעות מערכת הדיווח הלאומית הרשומה בנספח V. על ידי דיווח על תופעות לוואי תוכל לסייע לספק מידע נוסף אודות בטיחותה של תרופה זו.
תפוגה ושמירה
שמור את התרופה הרחק מעיני ילדים.
אין להשתמש בתרופה זו לאחר תאריך התפוגה המופיע על הבקבוקון והקרטון לאחר תאריך התפוגה.
יש לאחסן בטמפרטורה שלא תעלה על 30 מעלות צלזיוס. שמור את הבקבוקון בקרטון החיצוני כדי להגן על התרופה מפני אור.
יש להשתמש בפתרון המחודש מיד לאחר ההכנה. אם הפתרון המחודש אינו בשימוש מיידי, תנאי וזמני השימוש הם באחריות המכין. עם זאת, הפתרון המשוחזר יציב במשך 8 שעות בטמפרטורה של 25 מעלות צלזיוס לפני הניהול כאשר הוא מאוחסן בבקבוקון המקורי ו / או במזרק, עם זמן אחסון מרבי של התרופה המשוחזרת לא יעלה על 8 שעות.
VELCADE מיועד לשימוש חד פעמי בלבד. יש להיפטר ממוצר ופסולת שאינם בשימוש בהתאם לתקנות המקומיות בתוקף.
דדליין "> מידע אחר
מה מכיל VELCADE
- המרכיב הפעיל הוא בורטזומיב. כל בקבוקון מכיל 3.5 מ"ג בורטזומיב (כאסתר בורוני של מניטול). לאחר הכינון מחדש, 1 מ"ל של פתרון להזרקה מכיל 1 מ"ג של בורטזומיב.
- המרכיבים הנוספים הם מניטול (E421) וחנקן.
שחזור לשימוש תוך ורידי: לאחר היישוב מחדש, 1 מ"ל של תמיסה להזרקה תוך ורידית מכיל 1 מ"ג בורטזומיב.
שחזור לשימוש תת עורי: לאחר היישוב מחדש, 1 מ"ל של תמיסה להזרקה תת עורית מכיל 2.5 מ"ג בורטזומיב.
תיאור איך נראית VELCADE ותכולת האריזה
אבקת VELCADE לתמיסה להזרקה היא לבנה עד לבנה שמנת.
כל חבילה של VELCADE 3.5 מ"ג מכילה בקבוקון זכוכית אחד של 10 מ"ל עם פקק כחול, המכיל שלפוחית שקופה.
דדליין "> מידע לאנשי מקצוע בתחום הבריאות
המידע הבא מיועד לאנשי מקצוע בתחום הבריאות בלבד
שחזור לזריקה תוך -עירונית
הערה: VELCADE הוא חומר ציטוטוקסי. כתוצאה מכך, יש לנקוט משנה זהירות במהלך הטיפול וההכנה. מומלץ ללבוש כפפות ובגדי מגן אחרים, למניעת מגע עם העור.
בשל היעדרותם של כל מיני סוגים של חומרים משמרים, יש לעקוב אחר סטנדרטים טכניים אספקטיים במהלך הטיפול ב- VELCADE.
- הכנת הבקבוקון 3.5 מ"ג: הוסף 3.5 מ"ל תמיסת נתרן כלוריד סטרילית 9 מ"ג / מ"ל (0.9%) להזרקה לבקבוקון המכיל את אבקת VELCADE. האבקה המסועפת מתמוססת לחלוטין תוך פחות מ -2 דקות.
ריכוז הפתרון המתקבל שווה ל- 1 מ"ג / מ"ל. הפתרון יהיה צלול וחסר צבע עם pH סופי בין 4 ל 7. אין צורך לבדוק את ה- pH של התמיסה.
- יש לבדוק את התמיסה ויזואלית לפני הניהול כדי לבדוק אם יש חלקיקים או שינוי בצבע. בנוכחות חלקיקים או שינוי צבע, אין להשתמש בתמיסה ויש להשליך אותה.
אשר את הריכוז בבקבוקון כדי להבטיח שהמינון הנכון יינתן לווריד (1 מ"ג / מ"ל).
- הפתרון המחודש אינו מכיל חומרים משמרים ויש להשתמש בו מיד לאחר ההכנה תוך יציבות כימית ופיזית במשך 8 שעות ב -25 מעלות צלזיוס בבקבוקון המקורי ו / או במזרק עם 8 שעות לכל היותר במזרק. זמן האחסון הכולל של התרופה המשוחזרת לא יעלה על 8 שעות לפני הניהול. אם הפתרון המחודש אינו בשימוש מיד לאחר ההכנה, באחריות המשתמש לציית לתנאי האחסון והזמנים של המוצר לפני השימוש.
אין צורך להגן על התרופה המשוחזרת מפני אור.
מִנהָל
- לאחר המסה יש למשוך את הכמות המתאימה של הפתרון המשוחזר בהתאם למינון המחושב על בסיס שטח הגוף של המטופל.
- יש לאשר את המינון והריכוז במזרק לפני השימוש (בדקו שהמזרק מסומן למתן תוך ורידי).
- הזריק את התמיסה תוך ורידי כבולוס של 3-5 שניות, דרך קטטר תוך ורידי היקפי או מרכזי.
- שטפו את הקטטר תוך ורידי עם תמיסת זרקור נתרן כלוריד 9 מ"ג / מ"ל (0.9%) להזרקה.
אבקת VELCADE 3.5 מ"ג לתמיסה להזרקה מיועדת לשימוש תת -מידי או תוך -עירוני. אין לנהל במסלולים אחרים. ניהול תוך -פתולוגי גרם למקרי מוות.
רְשׁוּת
הבקבוקון מיועד לשימוש חד פעמי בלבד ויש להשליך את הפתרון הנותר.
יש להשליך תרופות שאינן בשימוש ופסולת מתרופה זו בהתאם לתקנות המקומיות.
המידע הבא מיועד לאנשי מקצוע בתחום הבריאות בלבד:
ניתן לתת את הבקבוקון של 3.5 מ"ג תת עורית כמתואר להלן.
שחזור לזריקה תת -מקומית
הערה: VELCADE הוא חומר ציטוטוקסי. כתוצאה מכך, יש לנקוט משנה זהירות במהלך הטיפול וההכנה. מומלץ ללבוש כפפות ובגדי מגן אחרים, למניעת מגע עם העור.
בשל היעדרותם של כל מיני סוגים של חומרים משמרים, יש לעקוב אחר סטנדרטים טכניים אספקטיים במהלך הטיפול ב- VELCADE.
- הכנת הבקבוקון 3.5 מ"ג: הוסף 1.4 מ"ל של תמיסת נתרן כלוריד סטרילית 9 מ"ג / מ"ל (0.9%) להזרקה לבקבוקון המכיל את אבקת VELCADE. האבקה המסועפת מתמוססת לחלוטין תוך פחות מ -2 דקות.
ריכוז הפתרון המתקבל שווה ל- 2.5 מ"ג / מ"ל. הפתרון יהיה צלול וחסר צבע עם pH סופי בין 4 ל 7. אין צורך לבדוק את ה- pH של התמיסה.
- יש לבדוק את התמיסה ויזואלית לפני הניהול כדי לבדוק אם יש חלקיקים או שינוי בצבע. בנוכחות חלקיקים או שינוי צבע, אין להשתמש בתמיסה ויש להשליך אותה.
אשר את הריכוז בבקבוקון כדי להבטיח שהמינון הנכון יינתן תת עורית (2.5 מ"ג / מ"ל).
- הפתרון המחודש אינו מכיל חומרים משמרים ויש להשתמש בו מיד לאחר ההכנה תוך יציבות כימית ופיזית במשך 8 שעות ב -25 מעלות צלזיוס בבקבוקון המקורי ו / או במזרק עם 8 שעות לכל היותר במזרק. זמן האחסון הכולל של התרופה המשוחזרת לא יעלה על 8 שעות לפני הניהול. אם הפתרון המחודש אינו בשימוש מיד לאחר ההכנה, באחריות המשתמש לציית לתנאי האחסון והזמנים של המוצר לפני השימוש.
אין צורך להגן על התרופה המשוחזרת מפני אור.
מִנהָל
- לאחר המסה יש למשוך את הכמות המתאימה של הפתרון המשוחזר בהתאם למינון המחושב על בסיס שטח הגוף של המטופל.
- יש לאשר את המינון והריכוז במזרק לפני השימוש (בדקו שהמזרק מסומן למתן תת עורית).
- הזריק את הפתרון תת עורית, בזווית של 45-90 מעלות
- הפתרון המחודש מנוהל תת עורית בירכיים (ימין או שמאל) או בבטן (ימין או שמאל)
- במנהלים הבאים יש צורך לשנות את מקום ההזרקה בסיבוב.
- אם מתרחשות תגובות מקומיות באתר ההזרקה לאחר הזרקה תת עורית של VELCADE, ניתן לתת ריכוז נמוך יותר של תמיסת VELCADE 3.5 מ"ג (1 מ"ג / מ"ל במקום 2.5 מ"ג / מ"ל) או מומלץ לעבור ל"זרקה לווריד ".
אבקת VELCADE 3.5 מ"ג לתמיסה להזרקה מיועדת לשימוש תת -מידי או תוך -עירוני. אין לנהל במסלולים אחרים. ניהול תוך -פתולוגי גרם למקרי מוות.
רְשׁוּת
הבקבוקון מיועד לשימוש חד פעמי בלבד ויש להשליך את הפתרון הנותר.
יש להשליך תרופות שאינן בשימוש ופסולת מתרופה זו בהתאם לתקנות המקומיות.
עלון המקור: AIFA (סוכנות התרופות האיטלקית). תוכן שפורסם בינואר 2016. ייתכן שהמידע הנוכחי אינו מעודכן.
כדי לקבל גישה לגרסה העדכנית ביותר, מומלץ לגשת לאתר AIFA (סוכנות התרופות האיטלקית). כתב ויתור ומידע שימושי.
01.0 שם התרופה -
אבקה של VELCADE 3,5 מג לתמיסה להזרקה
02.0 הרכב איכותי וכמותי -
כל בקבוקון מכיל 3.5 מ"ג בורטזומיב (כאסתר בורוני של מניטול).
לאחר השחזור, 1 מ"ל של פתרון להזרקה לשימוש תת עורי מכיל 2.5 מ"ג בורטזומיב.
לאחר השחזור, 1 מ"ל של פתרון להזרקה לשימוש תוך ורידי מכיל 1 מ"ג של בורטזומיב.
לרשימת החומרים המלאים, ראה סעיף 6.1.
03.0 טופס פרמצבטי -
אבקה לתמיסה להזרקה.
אבקה לבנה עד שמנת (אם דחוסה או לא).
מידע קליני 04.0 -
04.1 אינדיקציות טיפוליות -
VELCADE כטיפול יחיד או בשילוב עם דוקסורוביצין ליפוזומלי או דקסמתזון מסומנים לטיפול בחולים בוגרים עם מיאלומה פרוגרסיבית שכבר קיבלו לפחות טיפול אחד קודם ואשר כבר עברו או אינם זכאים להשתלת תאי גזע. .
VELCADE בשילוב עם מלפלן ופרדניזון מיועדים לטיפול בחולים מבוגרים עם מיאלומה נפוצה שטרם טופלו שאינם כשירים לכימותרפיה במינון גבוה עם השתלת תאי גזע המטופויאטיים.
VELCADE בשילוב עם dexamethasone או עם dexamethasone ו thalidomide מיועדת לטיפול אינדוקציה בחולים מבוגרים עם מיאלומה נפוצה שטרם טופלו, הזכאים לכימותרפיה במינון גבוה עם השתלת תאי גזע המטופויטיים.
VELCADE בשילוב עם ריטוקסימאב, ציקלופוספמיד, דוקסורוביצין ופרדניזון מיועדים לטיפול בחולים מבוגרים עם לימפומה של תאי מעטה שלא טופלו בעבר שאינם כשירים להשתלת תאי גזע המטופויאטיים.
04.2 מינון ואופן ניהול -
יש להתחיל את הטיפול ולנהל אותו תחת פיקוחו של רופא בעל הכשרה ומנוסה בשימוש בתרופות כימותרפיות.
מינון לטיפול במיאלומה נפוצה פרוגרסיבית (חולים שקיבלו לפחות קו טיפול אחד קודם)
מונוטרפיה
אבקת VELCADE 3.5 מ"ג לתמיסה להזרקה ניתנת תוך ורידי או תת עורית במינון המומלץ של 1.3 מ"ג / מ"ר שטח גוף פעמיים בשבוע למשך שבועיים בימים 1, 4, 8 ו -11 במחזור טיפול אחד בן 21 יום זה תקופה של 3 שבועות נחשב למחזור טיפול.
מומלץ כי המטופלים יקבלו 2 קורסים של VELCADE לאחר אישור שהושגה תגובה מלאה.
למטופלים המגיבים לטיפול אך אינם משיגים הפוגה מלאה, מומלץ לבצע סך של 8 קורסים של VELCADE.
אמורות לחלוף לפחות 72 שעות בין מתן שתי מנות רצופות של VELCADE.
התאמות המינון במהלך הטיפול והחידוש שלו כטיפול יחידני
יש להפסיק את הטיפול ב- VELCADE עם תחילת כל רעילות לא-המטולוגית בדרגה 3 או כל רעילות המטולוגית בדרגה 4, למעט נוירופתיה, כפי שצוין להלן (ראה גם סעיף 4.4). רעילות, ניתן להמשיך את הטיפול ב- VELCADE במינון נמוך יותר של 25% ( 1.3 מ"ג / מ"ר מופחת ל -1.0 מ"ג / מ"ר; 1.0 מ"ג / מ"ר מופחת ל -0.7 מ"ג / מ"ר). כאשר תסמיני הרעילות לא נפתרו, או אם הם חוזרים במינון מופחת, יש לשקול הפסקת טיפול ב- VELCADE, אלא אם כן היתרונות של הטיפול עולים בבירור על הסיכונים.
כאבים נוירופתיים ו / או נוירופתיה היקפית
יש לטפל בחולים הסובלים מכאב נוירופתי הקשור לבורטזומיב ו / או נוירופתיה היקפית בהתאם לטבלה 1 (ראה סעיף 4.4).
חולים עם נוירופתיה חמורה קיימת ניתן לטפל ב- VELCADE רק לאחר "הערכת סיכון / תועלת קפדנית".
טבלה 1: שינויים מומלצים במינון * במקרה של נוירופתיה הקשורה במתן בורטזומיב
טיפול משולב עם דוקסורוביצין ליפוזומלי מפוגל
אבקת VELCADE 3.5 מ"ג לתמיסה להזרקה ניתנת תוך ורידי או תת עורית במינון המומלץ של 1.3 מ"ג / מ"ר שטח גוף פעמיים בשבוע למשך שבועיים בימים 1, 4, 8 ו -11 במחזור טיפול אחד בן 21 יום זה תקופה של 3 שבועות נחשב למעגל טיפול לפחות 72 שעות אמורות לעבור בין מתן שתי מנות רצופות של VELCADE.
Doxorubicin ליפוזומלית מפוגלית ניתנת במינון של 30 מ"ג / מ"ר ביום 4 של מחזור הטיפול ב- VELCADE כעירוי תוך ורידי שנמשך שעה אחת לאחר הזרקת VELCADE.
ניתן לתת עד 8 מחזורים של טיפול משולב זה עד שהמטופלים יראו התקדמות וסובלים טיפול. חולים שמשיגים תגובה מלאה יכולים להמשיך בטיפול במשך 2 מחזורים לפחות לאחר הוכחה ראשונה לתגובה מלאה, גם אם הדבר דורש טיפול במשך יותר מ -8 מחזורים. חולים שרמות הפראפרוטאין שלהם ממשיכות לרדת לאחר 8 מחזורים יכולים להמשיך בטיפול כל עוד הטיפול נסבל ולהמשיך להראות תגובה.
למידע נוסף בנוגע לדוקסורוביצין ליפוזומלי מפוגל, עיין בסיכום המאפיינים של המוצר.
שילוב עם דקסמתזון
אבקת VELCADE 3.5 מ"ג לתמיסה להזרקה ניתנת תוך ורידי או תת עורי במינון המומלץ של 1.3 מ"ג / מ"ר שטח גוף פעמיים בשבוע למשך שבועיים בימים 1, 4, 8 ו -11 במחזור טיפול אחד בן 21 יום זה תקופה של 3 שבועות נחשב למחזור טיפול לפחות 72 שעות אמורות לעבור בין מתן שתי מנות רצופות של VELCADE.
Dexamethasone ניתנת דרך הפה במינון של 20 מ"ג בימים 1, 2, 4, 5, 8, 9, 11 ו -12 של מחזור הטיפול ב- VELCADE.
מטופלים שמשיגים תגובה או התייצבות למחלה לאחר 4 מחזורים של טיפול משולב זה יכולים להמשיך לקבל את אותו שילוב עד 4 מחזורים נוספים.
למידע נוסף אודות דקסמתזון, עיין בסיכום המאפיינים של המוצר.
התאמת מינון לטיפול משולב בחולים עם מיאלומה נפוצה פרוגרסיבית
להתאמות המינון של VELCADE בטיפול משולב יש לעקוב אחר ההמלצות לשינוי המינון המתוארות בסעיף המונוטרפיה לעיל.
מינון לטיפול במיאלומה נפוצה שטרם טופלה בחולים שאינם זכאים לכימותרפיה במינון גבוה עם השתלת תאי גזע המטופויטיים.
טיפול משולב עם מלפלן ופרדניזון
אבקת VELCADE 3.5 מ"ג לתמיסה להזרקה ניתנת תוך ורידי או תת עורית בשילוב עם מלפלן דרך הפה ופרדניזון דרך הפה כפי שמצוין בטבלה 2. פרק זמן של 6 שבועות נחשב כטיפול. במחזורים 1-4 VELCADE ניתנת פעמיים בשבוע בימים 1, 4, 8, 11, 22, 25, 29 ו -32. במחזורים 5-9 VELCADE ניתנת פעם בשבוע בימים 1, 8, 22 ו -29. אמורות לחלוף לפחות 72 שעות בין מתן שתי מנות רצופות של VELCADE.
מלפלאן ופרדניזון צריכים להינתן דרך הפה בימים 1, 2, 3 ו -4 בשבוע הראשון של כל מחזור טיפול VELCADE. 9 מחזורי טיפול של טיפול משולב זה ניתנים.
טבלה 2: לוח הזמנים של הפוסולוגיה המומלצת של VELCADE בשילוב עם מלפלן ופרדניזון
התאמות המינון במהלך הטיפול והחידוש שלו בשילוב עם מלפלן ופרדניזון
לפני תחילת קורס טיפול חדש:
• ספירת הטסיות צריכה להיות ≥ 70 x 109 / L וספירת נויטרופילים מוחלטת (ANC) ≥ 1.0 x 109 / L
• הרעילות הלא-המטולוגית בוודאי ירדה לדרגה 1 או לתחילת המחקר
טבלה 3: שינויים בפוסולוגיה במהלך הקורסים הבאים של טיפול VELCADE בשילוב עם מלפלן ופרדניזון
למידע נוסף אודות מלפלן ופרדניזון, עיין בסיכומי מאפייני המוצר שלהם.
מינון לטיפול במיאלומה נפוצה שטרם טופלה בחולים הזכאים להשתלת תאי גזע המטופויטיים (טיפול אינדוקציה).
טיפול משולב עם דקסמתזון
אבקת VELCADE 3.5 מ"ג לתמיסה להזרקה ניתנת תוך ורידי או תת עורי במינון המומלץ של 1.3 מ"ג / מ"ר שטח גוף פעמיים בשבוע למשך שבועיים בימים 1, 4, 8 ו -11 במחזור טיפול אחד בן 21 יום זה תקופה של 3 שבועות נחשב למעגל טיפול לפחות 72 שעות אמורות לעבור בין מתן שתי מנות רצופות של VELCADE.
Dexamethasone ניתנת דרך הפה במינון של 40 מ"ג בימים 1, 2, 3, 4, 8, 9, 10 ו -11 של מחזור הטיפול VELCADE.
ארבעה מחזורי טיפול של טיפול משולב זה ניתנים.
טיפול משולב עם תלידומיד ודקסמתזון
אבקת VELCADE 3.5 מ"ג לתמיסה להזרקה ניתנת תוך ורידי או תת עורית במינון המומלץ של 1.3 מ"ג / מ"ר שטח גוף פעמיים בשבוע במשך שבועיים בימים 1, 4, 8 ו -11 במחזור טיפול אחד בן 28 ימים. תקופה זו בת 4 שבועות נחשב למחזור טיפול.
אמורות לחלוף לפחות 72 שעות בין מתן שתי מנות רצופות של VELCADE.
Dexamethasone ניתנת דרך הפה במינון של 40 מ"ג בימים 1, 2, 3, 4, 8, 9, 10 ו -11 של מחזור הטיפול ב- VELCADE.
Thalidomide ניתנת דרך הפה במינון יומי של 50 מ"ג בימים 1-14; אם נסבול, המינון מוגדל ל -100 מ"ג בימים 15-28 ולאחר מכן ניתן להגדיל אותו עד 200 מ"ג ליום ממחזור 2 (ראה טבלה 4).
ארבעה מחזורי טיפול של טיפול משולב זה ניתנים.
למטופלים שמשיגים תגובה חלקית לפחות, מומלץ להוסיף 2 קורסי טיפול נוספים.
טבלה 4: מינון של טיפול משולב עם VELCADE לטיפול במיאלומה נפוצה שטרם טופלה בחולים הזכאים להשתלת תאי גזע המטופויאטיים.
התאמת מינון למועמדים להשתלה
להתאמת מינון VELCADE לנוירופתיה, עיין בטבלה 1.
בנוסף, כאשר VELCADE ניתנת בשילוב עם חומרים כימותרפיים אחרים, יש לשקול הפחתת מינון מתאים של תרופות רפואיות אלה במקרה של רעילות בהתאם להמלצות בסיכום הרלוונטי של מאפייני המוצר.
מינון לחולים עם לימפומה של תאי מעטה שטרם טופלו (MCL)
טיפול משולב עם ריטוקסימאב, ציקלופוספמיד, דוקסורוביצין ופרדניזון (VcR-CAP)
אבקת VELCADE 3.5 מ"ג לתמיסה להזרקה ניתנת תוך ורידי או תת עורי במינון המומלץ של 1.3 מ"ג / מ"ר שטח גוף פעמיים בשבוע למשך שבועיים בימים 1, 4, 8 ו -11, ואחריו תקופת מנוחה של 10 ימים בימים 12 עד 21. תקופה זו של 3 שבועות נחשבת למהלך של טיפול. לפחות 72 שעות אמורות לעבור בין מתן שתי מנות רצופות של VELCADE.
מומלץ 6 מחזורי טיפול עם טיפול משולב זה. למטופלים עם תגובה ראשונה מתועדת למחזור 6 ניתן לקבל 2 קורסי טיפול נוספים.
התרופות הבאות ניתנות כחליטה תוך ורידית ביום 1 של כל 3 שבועות טיפול עם VELCADE: ריטוקסימב במינון של 375 מ"ג / מ"ר, ציקלופוספמיד במינון של 750 מ"ג / מ"ר ודוקסורוביצין במינון של 50 מ"ג. / מ"ר.
פרדניזון ניתנת דרך הפה במינון של 100 מ"ג / מ"ר בימים 1, 2, 3, 4 ו -5 מכל מחזור טיפול עם VELCADE.
התאמת המינון במהלך הטיפול בחולים עם MCL שטרם טופל
לפני תחילת קורס טיפול חדש:
• ספירת הטסיות חייבת להיות ≥ 100,000 תאים / מק"ל וספירת הנויטרופילים המוחלטת (ANC) חייבת להיות ≥ 1,500 תאים / מק"ל
• ספירת הטסיות צריכה להיות ≥ 75,000 תאים / מק”ל בחולים עם חדירת מח עצם או התכווצות טחול
• ההמוגלובין חייב להיות ≥ 8 גרם / ד"ל
• יש להפחית את הרעילות הלא-המטולוגית לדרגה 1 או לתחילת המחקר.
יש להפסיק את הטיפול ב- VELCADE עם תחילת כל רעילות שאינה המטולוגית הקשורה ל VELCADE בדרגה 3 (למעט נוירופתיה) או רעילות המטולוגית בדרגה 3 (ראה גם סעיף 4.4). להתאמת המינון, ראה טבלה 5 להלן.
במקרה של רעילות המטולוגית, ניתן לנהל גורמי גדילה של גרנולוציטים בהתאם לפרקטיקה הסטנדרטית המקומית. יש לשקול שימוש מונע בגורמי גדילה של גרנולוציטים במקרה של עיכובים חוזרים ונשנים במתן קורסי טיפול.כאשר הדבר מתאים מבחינה קלינית, יש לשקול עירוי של טסיות דם לטיפול בטרומבוציטופניה.
טבלה 5: התאמת המינון במהלך הטיפול בחולים עם MCL שטרם טופל
בנוסף, כאשר VELCADE ניתנת בשילוב עם תרופות כימותרפיות אחרות, יש לשקול "הפחתת מינון מתאימה של תרופות אלו במקרה של רעילות, בהתאם להמלצות הכלולות בסיכום מאפייני המוצר".
אוכלוסיות מיוחדות
מטופלים מבוגרים
אין עדות קלינית המצביעה על צורך בהתאמת המינון בחולים מעל גיל 65 עם מיאלומה נפוצה או לימפומה של תאי מעטפת.
אין מחקרים על השימוש ב- VELCADE בחולים קשישים עם מיאלומה נפוצה שטרם טופלו המועמדים לכימותרפיה במינון גבוה עם השתלת תאי גזע המטופויאטיים.
לכן, לא ניתן להמליץ על אוכלוסייה זו.
במחקר שנערך בקרב חולי לימפומה של תאי מעטפת שלא טופלו בעבר, 42.9% ו -10.4% מהחולים שנחשפו ל- VELCADE היו בטווח של 65-74 שנים וגיל 75 ≥ בהתאמה. בחולים בני 75 ומעלה, שני המשטרים, VELCADE בשילוב עם ריטוקסימאב, ציקלופוספמיד, דוקסורוביצין ופרדניזון (VcR-CAP) וריטוקסימאב, ציקלופוספמיד, דוקסורוביצין, וינסריסטין ופרדניזון (R-CHOP), נסבלו פחות (ראה סעיף 4.8 ).
תפקוד לקוי של הכבד
חולים עם ליקוי כבד קל אינם דורשים התאמת מינון ויש לטפל בהם במינון המומלץ.חולים עם ליקוי בכבד בינוני או חמור צריכים להתחיל בטיפול ב- VELCADE במינון מופחת של 0.7 מ"ג / מ"ר לזריקה במהלך מחזור הטיפול הראשון, ועלייה נוספת במינון ל -1.0 מ"ג / מ"ר או הפחתה נוספת של מינון ל -0.5 מ"ג / מ"ר עלולה להתרחש. להיחשב על סמך סובלנות המטופל (ראה טבלה 6 וסעיפים 4.4 ו -5.2).
טבלה 6: שינויים מומלצים במינון ההתחלתי של VELCADE לחולים עם ליקוי בכבד
תפקוד לקוי של הכליות
הפרמקוקינטיקה של בורטזומיב אינה מושפעת בחולים עם ליקוי כלייתי קל עד בינוני (פינוי קריאטינין [CrCL]> 20 מ"ל / דקה / 1.73 מ"ר); לכן אין צורך בהתאמת מינון בחולים אלה. לא ידוע אם הפרמקוקינטיקה של בורטזומיב משתנה בחולים עם ליקוי כלייתי חמור שאינם בדיאליזה (CrCL
אוכלוסיית ילדים
הבטיחות והיעילות של VELCADE בחולים מתחת לגיל 18 לא נקבעו (ראו סעיפים 5.1 ו -5.2). אין נתונים זמינים.
שיטת ניהול
אבקת VELCADE 3.5 מ"ג לתמיסה להזרקה מיועדת לניהול תוך ורידי או תת עורי.
אבקת VELCADE 1 מ"ג לתמיסה להזרקה מיועדת לניהול תוך ורידי בלבד.
אסור לנהל את VELCADE בנתיבים אחרים. ניהול תוך -פתולוגי גרם למוות.
זריקה תוך ורידית
הפתרון המחודש של VELCADE 3.5 מ"ג ניתנת תוך ורידי כבולוס של 3-5 שניות, באמצעות קטטר תוך ורידי היקפי או מרכזי, ולאחר מכן שטיפה עם נתרן כלורי 9 מ"ג / מ"ל (0, 9%). אמורות להיות לפחות 72 שעות בין שתי מנות רצופות של VELCADE.
זריקה תת עורית
התמיסה המחודשת של VELCADE 3.5 מ"ג ניתנת תת עורית בירכיים (ימין או שמאל) או בבטן (ימין או שמאל). יש להזריק את הפתרון תת עורית בזווית של 45-90 מעלות.
יש לשנות את אתרי ההזרקה בסיבוב לזריקות הבאות.
אם מתרחשות תגובות באתר ההזרקה לאחר מתן תת עורית של VELCADE, ניתן לתת תמיסה פחות מרוכזת של VELCADE (3.5 מ"ג מחדש של VELCADE במינון של 1 מ"ג / מ"ל במקום 2.5 מ"ג / מ"ל) או לעבור למינון תוך ורידי.
כאשר VELCADE ניתנת בשילוב עם תרופות מרפא אחרות, עיין בסיכום מאפייני המוצר של תרופות אלו להנחיות לגבי הניהול.
04.3 התוויות נגד -
רגישות יתר לחומר הפעיל, לבורון או לכל אחד מהחומרים המצוינים בסעיף 6.1.
מחלת ריאות חדירה דיפוטית חריפה ופריקרדיופתיה.
כאשר VELCADE ניתנת בשילוב עם תרופות רפואיות אחרות, עיין בסיכום מאפייני המוצר הרלוונטי לקבלת התוויות נגד נוספות.
04.4 אזהרות מיוחדות ואמצעי זהירות מתאימים לשימוש -
כאשר VELCADE מנוהל בשילוב עם תרופות אחרות, יש להתייעץ עם סיכום מאפייני המוצר הרלוונטי לפני תחילת הטיפול ב- VELCADE. יש להקדיש תשומת לב מיוחדת לבדיקות הריון ולתקנות מניעת הריון בעת מתן תאלידומיד. ראה סעיף 4.6).
מתן תוך -פתולוגי
היו מקרים של מוות לאחר מתן אינטראקלי תוך -כווני של VELCADE. אבקת VELCADE 1 מ"ג לתמיסה להזרקה מיועדת לשימוש תוך ורידי בלבד, ואילו אבקת VELCADE 3.5 מ"ג לתמיסה להזרקה מיועדת לשימוש תוך ורידי או תת עורי. אין לתת VELCADE באופן אינטראקטי.
רעילות במערכת העיכול
תופעות רעילות במערכת העיכול, כולל בחילות, שלשולים, הקאות ועצירות, שכיחות מאוד במהלך הטיפול ב- VELCADE. מקרים של ileus paralytic דווחו באופן נדיר (ראה סעיף 4.8). לכן, חולים הסובלים מעצירות צריכים להיות במעקב צמוד.
רעילות המטולוגית
טיפול ב- VELCADE קשור לעיתים קרובות להשפעות רעילות המטולוגיות (טרומבוציטופניה, נויטרופניה ואנמיה). במחקרים שנערכו בחולים עם מיאלומה נפוצה חוזרת שטופלה ב- VELCADE ובמטופלים עם MCL שטרם טופל ב- VELCADE בשילוב עם ריטוקסימאב, ציקלופוספמיד, דוקסורוביצין ופרדניזון (VcR-CAP), אחת הרעילות ההמטולוגיות הנפוצות ביותר הייתה טרומבוציטופניה חולפת. הטסיות היו ברמה הנמוכה ביותר שלהן ביום 11 של כל מחזור טיפול VELCADE וחזרו לרמות הבסיס בדרך כלל במחזור הבא. לא נמצאה עדות לטרומבוציטופניה מצטברת. ממוצע הערך הטסיות של הטסיות היה כ -40% מערך הבסיס במחקרי מיאלומה נפוצה כאשר VELCADE שימש כטיפול יחיד ו -50% במחקר MCL. בחולים עם מיאלומה מתקדמת חומרת הטרומבוציטופניה הייתה קשורה לערכי טסיות לפני הטיפול: לערכי טסיות בתחילת 75,000 / mcl רק 14% מתוך 309 חולים סבלו ממספר טסיות ≤ 25,000 / mcl במהלך המחקר.
בחולים עם MCL (מחקר LYM-3002), הייתה שכיחות גבוהה יותר (56.7% נגד 5.8%) טרומבוציטופניה בדרגה ≥ 3 בקבוצת הטיפול ב- VELCADE (VcR-CAP) לעומת קבוצת הלא-VELCADE (ריטוקסימאב, ציקלופוספמיד, דוקסורוביצין, וינסריסטין ופרדניזון [R-CHOP]). שתי קבוצות הטיפול היו דומות הן בשכיחות הכוללת של אירועי דימום מכל הציונים (6.3% בקבוצת VcR-CAP ו -5.0% בקבוצת R-CHOP) ובדרגה 3 ובדימום גדול (VcR-CAP: 4 מטופלים [ 1.7%]; R-CHOP: 3 חולים [1.2%]). בקבוצת VcR-CAP, 22.5% מהחולים קיבלו עירוי טסיות לעומת 2.9% מהחולים בקבוצת R-CHOP.
דיווחו על דימום במערכת העיכול והבין -מוחית בשילוב עם טיפול ב- VELCADE. לכן יש לעקוב אחר רמות הטסיות לפני מתן כל מנה של VELCADE. יש להפסיק את הטיפול ב- VELCADE כאשר מספר הטסיות מגיע לערכים
יש לעקוב באופן תדיר אחר ספירת דם מלאה, עם ספירת הפרשים וכוללת ספירת טסיות במהלך הטיפול ב- VELCADE. כאשר הדבר מתאים מבחינה קלינית, יש לשקול עירוי טסיות (ראה סעיף 4.2).
בחולי MCL ללא עדות לניוטרופניה מצטברת, נויטרופניה הפיכה חולפת נצפתה בין קורסי הטיפול. נויטרופילים היו ברמה הנמוכה ביותר ביום 11 של כל מחזור טיפול ב- VELCADE ובדרך כלל חזרו לקו הבסיס במחזור הבא. במחקר LYM-3002, תמיכה בגורמי גדילה הופעלה אצל 78% מהחולים בזרוע VcR-CAP ו -61% מהחולים בזרוע R-CHOP. מכיוון שחולים עם נויטרופניה נמצאים בסיכון מוגבר לזיהומים, יש לפקח עליהם על סימנים ותסמינים של זיהום ולטפל בהם מיד. ניתן לתת גורמי גדילה של גרנולוציטים לטיפול ברעילות המטולוגית בהתאם לפרקטיקה הסטנדרטית המקומית. במקרה של עיכובים חוזרים ונשנים במתן קורסי הטיפול, יש לשקול שימוש מונע בגורמי גדילה של גרנולוציטים (ראה סעיף 4.2).
הפעלה מחדש של וירוס הרפס זוסטר
מתן טיפול מונע אנטי -ויראלי מומלץ בחולים המקבלים VELCADE. במחקר שלב III שנערך בחולים עם מיאלומה נפוצה שטרם טופלה, השכיחות הכוללת של הפעלה מחדש של הרפס זוסטר הייתה שכיחה יותר בחולים שטופלו ב- VELCADE + מלפלן + פרדניזון מאשר בחולים שטופלו במלפלן + פרדניזון (בהתאמה 14 % לעומת 4 %).
בחולים עם MCL (מחקר LYM-3002), שכיחות זיהום הרפס זוסטר הייתה 6.7% בזרוע VcR-CAP ו -1.2% בזרוע R-CHOP (ראה סעיף 4.8).
הפעלה מחדש וזיהום בנגיף הפטיטיס B (HBV)
כאשר משתמשים בריטוקסימב בשילוב עם VELCADE, תמיד יש לבצע בדיקת HBV לפני תחילת הטיפול בחולים בסיכון לזיהום HBV. יש לעקוב מקרוב אחר נשאי הפטיטיס B וחולים עם היסטוריה של הפטיטיס B לאיתור סימנים קליניים ומעבדתיים לזיהום HBV פעיל במהלך הטיפול ואחריו בריטוקסימב בשילוב עם VELCADE. יש לשקול טיפול מונע אנטי ויראלי. למידע נוסף, עיין בסיכום מאפייני המוצר של rituximab.
לוקואנסצפלופתיה מולטיפוקלית מתקדמת (PML)
מקרים נדירים מאוד של זיהום בנגיף ג'ון קנינגהאם (JC) שגרם ל- PML ולמוות דווחו בחולים שטופלו ב- VELCADE, עם סיבתיות לא ידועה. חולים שאובחנו כסובלים מ- PML נטלו בעבר טיפול חיסוני או נטלו אותו במקביל. רוב מקרי PML אובחנו תוך 12 חודשים לאחר נטילת המנה הראשונה של VELCADE. יש לעקוב אחר המטופלים במרווחי זמן קבועים לאיתור סימפטומים או סימנים נוירולוגיים חדשים או המחמירים העשויים להצביע על PML בקרב האבחנות הדיפרנציאליות של בעיות במערכת העצבים המרכזית. אם יש חשד לאבחנה של PML, יש להפנות את המטופלים לרופא המתמחה בניהול PML ואמצעי אבחון מתאימים עבור PML המיושם. במקרה של אבחון PML מאושר, יש להפסיק את הטיפול ב- VELCADE.
נוירופתיה היקפית
טיפול ב- VELCADE קשור לרוב להופעת נוירופתיה פריפרית, בעיקר חושית, אולם עם זאת דווחו מקרים של נוירופתיה מוטורית קשה עם או בלי נוירופתיה חושית היקפית.
שכיחות הנוירופתיה ההיקפית עולה בתחילת הטיפול ומגיעה לשיא במחזור 5.
יש לעקוב מקרוב אחר המטופלים לגבי תסמינים של נוירופתיה כגון תחושת צריבה, היפרסטזיה, היפואתזיה, פאראסטזיה, חולשה, כאב נוירופתי או חולשה.
במחקר הקליני שלב III השוואת VELCADE הניתנת תוך ורידי למסלול התת -עורי, שכיחות אירועי נוירופתיה היקפיים מסוג 2 הייתה 24% בקבוצת הניהול התת עורית ו -41% בקבוצת ההזרקה תוך ורידית (p = 0.0124). נוירופתיה התרחשה ב -6% מהחולים בקבוצת הטיפול התת -עורי לעומת 16% בקבוצת הטיפול תוך ורידי (p = 0.0264). כל דרגות הנוירופתיה ההיקפית עם VELCADE שניתנו לווריד היו נמוכים יותר במחקרים קודמים בהם VELCADE ניתנה תוך ורידי מאשר במחקר MMY. -3021.
הערכה נוירולוגית מומלצת בחולים עם התפרצות או החמרה של נוירופתיה היקפית, שעבורם עשוי להידרש שינוי במינון או במשטר או שינוי דרך הניהול למסלול התת עורי (ראה סעיף 4.2). נוירופתיה טופלה באמצעות טיפולים תומכים או אחרים.
יש לשקול ניטור מוקדם וקבוע אחר סימפטומים של נוירופתיה הקשורה לטיפול עם הערכה נוירולוגית בחולים המקבלים VELCADE בשילוב עם תרופות ידועות כקשורות לנוירופתיה (למשל תלידומיד) ויש לקחת בחשבון הולם הפחתת המינון או הפסקת הטיפול .
בנוסף לנוירופתיה היקפית, נוירופתיה אוטונומית עשויה לתרום להופעתן של תופעות לוואי מסוימות, כגון לחץ דם יציב ועצירות קשה באילאוס. עדיין קיים מידע מוגבל על נוירופתיה אוטונומית ותרומתה לתופעות לוואי אלו.
עוויתות
התקפים דווחו באופן נדיר בחולים ללא היסטוריה של התקפים או אפילפסיה. טיפול מיוחד נדרש בעת טיפול בחולים בסיכון להתקפים.
לחץ דם גבוה
טיפול ב- VELCADE קשור בדרך כלל ליתר לחץ דם אורתוסטטי / יציב. רוב תגובות הלוואי הן בדרגת חומרה קלה עד בינונית והן נצפו במהלך הטיפול. לחולים שחוו לחץ דם אורתוסטטי עם VELCADE (מוזרק תוך ורידי) לא היו פרקים קודמים של לחץ דם אורתוסטטי לפני הטיפול. טיפול במרבית החולים היה נדרש לטיפול ביתר לחץ דם אורתוסטטי. מיעוט מהחולים עם לחץ דם אורתוסטטי חווה אפיזודות סינקופיות. לחץ דם אורתוסטטי / יציב לא היה קשור באופן חד לחליטת בולוס של VELCADE.
המנגנון של אירוע זה אינו ידוע, אם כי רכיב עשוי להיקבע על ידי נוירופתיה אוטונומית. נוירופתיה אוטונומית עשויה להיות קשורה לבורטזומיב, או שייתכן שהתרופה עלולה להחמיר מצב קיים, כגון נוירופתיה סוכרתית או עמילואידוטית. יש לנקוט בזהירות רבה בטיפול בחולים עם היסטוריה של סינקופה המטופלים בתרופות הידועות כקשורות ליתר לחץ דם, או בחולים המגלים התייבשות הנובעת משלשולים או הקאות חוזרות. תרופות נוגדות יתר לחץ דם, התייבשות או מתן מינרל קורטיקוסטרואידים ו / או תרופות סימפטוממימטיות. יש לייעץ למטופלים להתייעץ עם רופא במקרה של סחרחורת, סחרחורת או פרקים קצרים של התעלפות.
תסמונת אנצפלופתיה הפיכה אחורית (PRES)
דווחו דיווחים על PRES בחולים שקיבלו VELCADE. PRES היא צורה נוירולוגית נדירה המאופיינת באבולוציה מהירה, לעתים קרובות הפיכה, שיכולה להתבטא בהתקפים, יתר לחץ דם, כאבי ראש, עייפות, בלבול, עיוורון ושינויים חזותיים ונוירולוגיים אחרים. האבחנה מאושרת על ידי תמונות רדיולוגיות של מבני המוח, רצוי שהושגו באמצעות תהודה מגנטית גרעינית (MRI). בחולים המפתחים PRES, יש להפסיק את הטיפול ב- VELCADE.
אִי סְפִיקַת הַלֵב
הופעה חריפה או החמרה של אי ספיקת לב, ו / או התפתחות ירידה של שפיכת פליטת החדר השמאלי נצפתה במהלך הטיפול ב- bortezomib. שמירת נוזלים עשויה להיות גורם מוביל לסימנים ותסמינים של אי ספיקת לב. חולים עם אי ספיקת לב או עם גורמי סיכון. עבור אי ספיקת לב צריך להיות במעקב קפדני.
חקירות אלקטרוקרדיוגרפיות
מקרים בודדים של הארכת מרווח QT נצפו במחקרים קליניים, שסיבתם לא נקבעה.
שינויים ריאתיים
מקרים נדירים של מחלת ריאות חדירה מפושטת של אטיולוגיה לא ידועה, כגון דלקת ריאות, דלקת ריאות אינטרסטיציאלית, חדירת ריאות ותסמונת מצוקה נשימתית חריפה (ARDS), דווחו בחולים שקיבלו VELCADE (ראה סעיף 4.8). חלק מהפרקים הללו היו קטלניים. מומלץ לבצע צילום חזה לפני הטיפול כהפניה בסיסית לשינויים ריאתיים פוטנציאליים לאחר הטיפול.
במקרה של הופעה או החמרה של סימפטומים ריאתיים (למשל שיעול, קוצר נשימה), יש לבצע הערכה אבחנתית מהירה של המטופל וטיפול מתאים כתוצאה מכך. יש לשקול את איזון הסיכון / תועלת לפני שתמשיך בטיפול VELCADE.
במהלך מחקר קליני, שניים מתוך שני מטופלים שקיבלו ציטראבין במינון גבוה (2 גרם / מ"ר ליום) כחליטה מתמשכת של 24 שעות בשילוב עם daunorubicin ו- VELCADE לטיפול בלוקמיה מיאלואידית חריפה חוזרת מתו בשל ARDS. בשלב הראשוני של הטיפול, המחקר הופסק. לכן אין צורך במשטר טיפול משולב ספציפי זה עם ציטראבין במינון גבוה (2 גרם / מ"ר ליום) תוך עירוי רציף של 24 שעות.
תפקוד כלייתי לקוי
סיבוכים בכליות שכיחים בחולים עם מיאלומה נפוצה. יש לעקוב בקפידה אחר מטופלים עם אי ספיקת כליות (ראה סעיפים 4.2 ו -5.2).
תפקוד כבד לקוי
בורטזומיב עוברת חילוף חומרים על ידי אנזימי כבד. בחולים עם ליקוי בכבד בינוני או חמור, החשיפה לבורטזומיב מוגברת; יש לטפל בחולים כאלה במינון מופחת של VELCADE ויש לעקוב בקפידה אחר הופעת הרעילות (ראה סעיפים 4.2 ו- 5.2).
תגובות כבדות
מקרים נדירים של אי ספיקת כבד דווחו בחולים שקיבלו VELCADE וטיפולים תרופתיים במקביל ולוקים במחלות חמורות.דווחו תגובות כבד אחרות כגון אנזימי כבד מוגברים, היפרבילירובינמיה והפטיטיס. שינויים אלה עשויים להיות הפיכים לאחר הפסקת הטיפול ב- bortezomib (ראה סעיף 4.8).
תסמונת תמונת גידול
מכיוון שבורטזומיב הוא חומר ציטוטוקסי ולכן הוא מסוגל להרוס במהירות תאי פלזמה ממאירים ותאי MCL, ניתן להבחין בסיבוכים מתסמונת פירוק הגידול. חולים בסיכון לפתח תסמונת תמוגה של הגידול הם אלה שהראו נטל גידול גבוה לפני תחילת הטיפול. יש לעקוב בקפידה אחר מטופלים אלה ולנקוט באמצעי זהירות.
מתן תרופות במקביל
יש לעקוב בקפידה אחר מטופלים המקבלים טיפול במקביל עם בורטזומיב ומעכבי CYP3A4 חזקים. יש לנקוט משנה זהירות בעת מתן שיתוף של מצעי בורטזומיב ו- CYP3A4 או CYP2C19 (ראה סעיף 4.5).
יש לאשר תפקוד כבד תקין בחולים המקבלים היפוגליקמיה אוראלית ולטפל בזהירות (ראה סעיף 4.5).
תגובות פוטנציאליות של מערכת חיסון מורכבת
דיווחו על תגובות קשורות למורכבות חיסונית, כגון מחלת סרום, פוליארתריטיס עם פריחה וגלומרולונפריטיס שגשוג. יש להפסיק את השימוש ב- bortezomib במקרה של אירועים חמורים.
04.5 אינטראקציות עם תרופות אחרות וצורות אינטראקציה אחרות -
חינוך בַּמַבחֵנָה מצביעים על כך שבורטזומיב הוא מעכב חלש של איזואנזים של ציטוכרום P450 (CYP) 1A2, 2C9, 2C19, 2D6 ו- 3A4. לאור התרומה המוגבלת (7%) של האיזואנזים CYP2D6 לחילוף החומרים של בורטזומיב, הוא סבור כי פנוטיפ נמוך של חילוף החומרים אינו משפיע על הזמינות הכוללת של בורטזומיב.
מחקר אינטראקציה בין תרופות לתרופות, המבוסס על נתונים של 12 חולים, לחקר ההשפעה של קטוקונזול, מעכב CYP3A4 רב עוצמה, על הפרמקוקינטיקה של בורטזומיב (מוזרק תוך ורידי) הראתה עלייה ממוצעת ב- AUC. 35% בורטזומיב (90% CI [ לכן, יש לעקוב מקרוב אחר מטופלים המקבלים טיפול במקביל עם בורטזומיב ומעכבי CYP3A4 חזקים (למשל קטוקונזול, ריטונוויר).
במחקר אינטראקציה בין תרופות לתרופות, המבוסס על נתונים מ -17 חולים, לחקור את ההשפעה של אומפרזול, מעכב CYP2C19 רב עוצמה, על הפרמקוקינטיקה של בורטזומיב (מוזרק תוך ורידי) לא נמצאה עדות להשפעה משמעותית על הפרמקוקינטיקה של בורטזומיב. .
מחקר קליני של אינטראקציה בין תרופות לתרופות, המבוסס על נתונים של 6 מטופלים, לחקר ההשפעה של ריפמפיצין, מעורר CYP3A4 רב עוצמה, על הפרמקוקינטיקה של בורטזומיב (מוזרק תוך ורידי) הראתה ירידה ממוצעת ב- AUC. 45% בורטזומיב. לכן, במקביל השימוש ב- bortezomib עם גורמי CYP3A4 חזקים (למשל rifampicin, carbamazepine, phenytoin, phenobarbital ו- Wort Wort) אינו מומלץ שכן היעילות עשויה להיות מופחתת.
באותו מחקר קליני אינטראקציה בין תרופות לתרופות, על נתונים מ -7 חולים, לאמת את ההשפעה של דקסמתזון, גורם מעורר חלש של CYP3A4, על הפרמקוקינטיקה של בורטזומיב (מוזרק תוך ורידי) לא הייתה השפעה משמעותית על הפרמקוקינטיקה של בורטזומיב.
מחקר אינטראקציה בין תרופות לתרופות, המבוסס על נתונים מ -21 חולים, להערכת ההשפעה של מלפלן-פרדניזון על הפרמקוקינטיקה של בורטזומיב (מוזרק תוך ורידי), הראה עלייה ב- AUC של בורטזומיב ב -17%.
זה לא נחשב רלוונטי מבחינה קלינית.
בניסויים קליניים, דיווחו על היפוגליקמיה והיפרגליקמיה באופן נדיר בחולי סוכרת שקיבלו תרופות היפוגליקמיות דרך הפה. מטופלים המטופלים בטיפול אנטי -סוכרתי דרך הפה, עשויים לדרוש ניטור מדויק של גלוקוז בדם והתאמת המינון של תרופות נוגדות סוכרת.
04.6 הריון והנקה -
אמצעי מניעה אצל גברים ונשים
גברים ונשים בגיל הפוריות חייבים להשתמש באמצעי מניעה נאותים במהלך הממשל ולמשך 3 חודשים לאחר הטיפול.
הֵרָיוֹן
אין נתונים קליניים על חשיפה לבורטזומיב במהלך ההריון. הפוטנציאל הטרטוגני של בורטזומיב לא נחקר במלואו.
במחקרים פרה -קליניים, מתן בורטזומיב במינונים המרביים שסופגה על ידי האם לא הראה כל השפעה על התפתחות העובר על חולדות וארנבות. לא נערכו מחקרים בבעלי חיים על מנת לקבוע השפעות כלשהן על לידה והתפתחות לאחר הלידה (ראה סעיף 5.3). אין להשתמש ב- VELCADE במהלך ההריון אלא אם מצבה הקליני של המטופלת מחייב את השימוש בו.
יש ליידע את המטופלת לגבי הסיכונים האפשריים לעובר אם ניתנת VELCADE במהלך ההריון, או אם המטופלת נכנסת להריון במהלך הטיפול.
תלידומיד הוא טרטוגן רב עוצמה בבני אדם וגורם למומים מולדים חמורים ומסכנים חיים. תאלידומיד אסורה במהלך ההיריון ובנשים בפריון, אלא אם מתקיימים כל התנאים של התוכנית למניעת הריון תאלידומיד. מטופלים המקבלים VELCADE בשילוב עם תלידומיד חייבים לדבוק התכנית למניעת הריון תאלידומיד עיין בסיכום מאפייני המוצר של תאלידומיד למידע נוסף.
זמן האכלה
לא ידוע אם בורטזומיב מופרש בחלב האדם. בשל הפוטנציאל לתגובות שליליות חמורות של VELCADE בתינוקות יונקים, יש להפסיק את ההנקה במהלך הטיפול ב- VELCADE.
פוריות
מחקרי פוריות לא נערכו עם VELCADE (ראה סעיף 5.3).
04.7 השפעות על יכולת הנהיגה וההתנהלות במכונות -
VELCADE עשויה להשפיע באופן מתון על יכולת הנהיגה או השימוש במכונות.
VELCADE עשוי להיות קשור בדרך כלל לעייפות, לרוב לסחרחורת, לא פעם עם סינקופה, בדרך כלל עם לחץ דם אורתוסטטי / יציב או ראייה מטושטשת. על המטופלים לנקוט משנה זהירות בעת נהיגה ברכבים או שימוש במכונות (ראה סעיף 4.8).
05.0 נכסים פרמקולוגיים -
05.1 "תכונות פרמקודינמיות -
קבוצה פרמקותרפית: תרופות אנטי -אופלסטיות, תרופות אנטי -אופלסטיות אחרות.
קוד ATC: L01XX32.
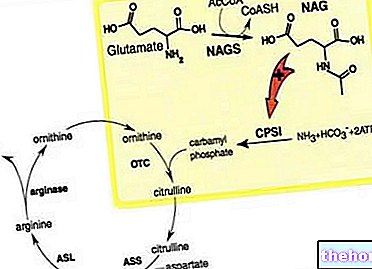
מנגנון הפעולה
בורטזומיב הוא מעכב פרוטאזום. מצוין במיוחד לעכב את הפעילות הדומה לכימוטריפסין של הפרוטאזום 26S בתאי יונקים. הפרוטאזום 26S הוא קומפלקס פוליפפטיד גדול, האחראי על התדרדרות חלבונים בכל מקום. המסלול המטבולי של ubiquitin-proteasome ממלא תפקיד חיוני בשליטה על המחזור של חלבונים ספציפיים, ובכך לשמור על הומאוסטזיס בתאים. עיכוב הפרוטאזום 26S מונע פרוטאוליזה ממוקדת זו ומשפיע על העברת האותות בתוך התא, מה שמוביל למוות של תאים סרטניים.
בורטזומיב סלקטיבי ביותר לפרוטאזום. בריכוזים של 10 מיקרוגרם, בורטזומיב אינו מעכב אף אחד מהרצפטורים והפרוטאזות הרבים הנבדקים והוא סלקטיבי יותר מ -1,500 פעמים לפרוטאזום מאשר אנזים המטרה השני. קינטיקה של עיכוב פרוטוזום הוערכה בַּמַבחֵנָה ובורטזומיב מתנתק מהפרוטאזום עם חצי שעה של 20 דקות, ובכך מוכיח כי עיכוב בורטזומיב הפיך.
לעיכוב של Bortezomib של הפרוטאזום יש השפעות רבות על תאים סרטניים, כולל, אך לא רק, שינוי החלבונים הרגולטוריים השולטים בהתקדמות מחזור התאים ו"הפעלת גורם גרעיני kB (NF-kB). L "עיכוב של פרוטאזום מוביל למעצר מחזור התא ולאפופטוזיס.
NF-kB הוא גורם שעתוק שהפעלתו נדרשת בשלבים רבים של סרטן, כולל צמיחת התא והישרדותו, אנגיוגנזה, אינטראקציה של תאים וגרורות. במיאלומה, בורטזומיב משפיע על יכולתם של תאי מיאלומה לקיים אינטראקציה עם המיקרו -סביבה של מח העצם.
ניסויים הראו כי בורטזומיב הוא ציטוטוקסי לסוגים רבים של תאים סרטניים ושתאים אלה רגישים הרבה יותר להשפעות הפרו -אפופטיות של עיכוב פרוטאזום מאשר רגילים. בורטזומיב גורם לירידה בצמיחת הגידול. in vivo במודלים רבים של סרטן פרה -קליני, כולל מיאלומה נפוצה.
נתונים במבחנה, לשעבר vivo ובמודלים של בעלי חיים מצביעים על כך שבורטזומיב מגביר את הבידול והפעילות האוסטאובלסטית ומעכב את התפקוד האוסטאוקלסטי.השפעות אלו נצפו בקרב חולי מיאלומה נפוצה עם מחלה אוסטיאוליטית מתקדמת שטופלו בבורטזומיב.
יעילות קלינית במיאלומה נפוצה שטרם טופלה
מחקר בינלאומי, אקראי (1: 1), פתוח, פרוספקטיבי, שלב III (MMY-3002 VISTA) נערך בקרב 682 מטופלים כדי להעריך האם VELCADE (Vc) (1.3 מ"ג / מ"ר מוזרק תוך ורידי) בשילוב עם מלפלן ( M) (9 מ"ג / מ"ר) ופרדניזון (P) (60 מ"ג / מ"ר) שיפרו את הזמן להתקדמות (TTP) בהשוואה למלפלן (9 מ"ג / מ"ר) ופרדניזון (60 מ"ג / מ"ר) בחולים עם מיאלומה נפוצה שטרם טופלה בעבר. . הטיפול ניתן למשך עד 9 מחזורים (כ -54 שבועות) והופסק מוקדם במקרה של התקדמות מחלה או רעילות בלתי קבילה. במחקר, הגיל החציוני של החולים היה 71 שנים, 50% היו גברים, 88% היו קווקזים, וציון הסטטוס הביצועי החציוני של קרנופסקי היה 80. לחולים היו מיאלומה של IgG / IgA / שרשרת קלה ב- 63% / 25 % / 8% מהמקרים, חציון המוגלובין של 105 גרם / ליטר וחציון טסיות טסיות של 221.5 x 109 / l. בשתי הקבוצות, אחוז החולים עם סיקול קריאטינין ≤ 30 היה דומה. מ"ל / דקה ( 3% בכל זרוע).
בזמן הניתוח ביניים כמתוכנן, נקודת הסיום העיקרית, הזמן להתקדמות, הושגה וחולים בזרוע M + P הציעו טיפול Vc + M + P. המעקב החציוני עמד על 16.3 חודשים. לאחר חציון מעקב נתון ההישרדות הסופי עודכן במשך 60.1 חודשים. נצפתה יתרון הישרדותי מובהק סטטיסטית לטובת קבוצת הטיפול ב- Vc + M + P (HR = 0.695, p = 0.00043) למרות הטיפולים הבאים הכוללים משטרי VELCADE. חציון הישרדות בטיפול Vc + M + P הקבוצה הייתה 56.4 חודשים לעומת 43.1 חודשים בקבוצת הטיפול ב- M + P. תוצאות היעילות מוצגות בטבלה 11.
טבלה 11: תוצאות יעילות לאחר עדכון סופי של נתוני הישרדות VISTA
חולים מועמדים להשתלת תאי גזע
שני מחקרים אקראיים, פתוחים, שלב III, רב-מרכזיים (IFM-2005-01, MMY-3010) נערכו כדי להדגים את בטיחות ויעילות VELCADE בשילוב כפול ומשולש עם תרופות כימותרפיות אחרות כטיפול אינדוקציה לפני השתלת תאי גזע בחולים. לא טופל בעבר עבור מיאלומה נפוצה.
במחקר IFM-2005-01 VELCADE בשילוב עם dexamethasone [VcDx, n = 240] הושווה ל- vincristine-doxorubicin-dexamethasone [VDDx, n = 242]. מטופלים בקבוצת VcDx קיבלו ארבעה מחזורים של 21 יום, שכל אחד מהם כלל VELCADE (1.3 מ"ג / מ"ר מנוהל תוך ורידי פעמיים בשבוע בימים 1, 4, 8 ו -11) ודקסמתזון אוראלי (40 מ"ג / מ"ר). ימים 1 עד 4 ובימים 9 עד 12, במחזורים 1 ו -2, ובימים 1 עד 4 במחזורים 3 ו -4).
מאה תשעים ושמונה חולים (82%) ו -208 חולים (87%) בקבוצות VDDx ו- VcDx, בהתאמה, עברו השתלת תאי גזע אוטולוגיים; רוב החולים עברו השתלה אחת. הדמוגרפיה של המטופלים ומאפייני המחלה הבסיסיים היו דומים בין שתי קבוצות הטיפול. במחקר, הגיל החציוני של החולים היה 57 שנים, 55% היו גברים ו -48% מהחולים היו בעלי סיכון ציטוגנטי גבוה. משך הטיפול החציוני היה 13 שבועות עבור קבוצת VDDx ו -11 שבועות בקבוצת VDDx. מספר המחזורים החציוני שקיבלו שתי הקבוצות היה 4 מחזורים.
נקודת סיום היעילות העיקרית של המחקר הייתה שיעור תגובה לאחר אינדוקציה (CR + nCR). הבדל מובהק סטטיסטית ב- CR + nCR נצפה לטובת קבוצת VELCADE בשילוב עם דקסמתזון. נקודות קצה יעילות משניות כללו תגובת שיעורים (CR + nCR, CR + nCR + VGPR + PR) לאחר ההשתלה, הישרדות ללא התקדמות והישרדות כוללת תוצאות היעילות העיקריות מוצגות בטבלה 12.
טבלה 12: תוצאות יעילות במחקר IFM-2005-01
במחקר MMY-3010 VELCADE בשילוב עם תלידומיד ודקסמתזון [VcTDx, n = 130] הושווה לתאלידומיד-דקסמתזון [TDx, n = 127]. מטופלים בקבוצת VcTDx קיבלו שישה מחזורים של 4 שבועות, שכל אחד מהם כלל VELCADE (1.3 מ"ג / מ"ר מנוהל פעמיים בשבוע בימים 1, 4, 8 ו -11, ואחריו תקופת מנוחה של 17 ימים 12 עד 28), דקסמתזון (40 מ"ג הניתנים דרך הפה בימים 1 עד 4 ובימים 8 עד 11), ותאלידומיד (50 מ"ג ליום הניתן דרך הפה בימים 1-14, כאשר המינון גדל ל -100 מ"ג בימים 15-28 ולאחר מכן ב -200 מ"ג לכל יְוֹם).
מאה וחמישה חולים (81%) ו -78 חולים (61%) בקבוצות VcTDx ו- TDx, בהתאמה. הם עברו השתלת תאי גזע אוטולוגיים בודדים. הדמוגרפיה של המטופלים ומאפייני המחלה הבסיסיים היו דומים בין שתי קבוצות הטיפול. לחולים בקבוצות VcTDx ו- TDx, בהתאמה, היה גיל חציוני של 57 ו -56 שנים, 99% ו -98% מהחולים היו קווקזים; 58% ו -54% היו גברים. בקבוצת VcTDx 12% מהחולים סווגו ציטוגנטית כסיכון גבוה לעומת 16% מהחולים בקבוצת TDx. משך הטיפול החציוני היה 24.0 שבועות והמספר החציוני של מחזורי הטיפול שהתקבלו היה 6.0 והיה עקבי בין קבוצות הטיפול.
נקודות הסיום העיקריות של המחקר היו שיעורי תגובה לאחר ההשראה ואחרי ההשתלה (CR + nCR). נצפה הבדל מובהק סטטיסטית ב- CR + nCR לטובת קבוצת הטיפול ב- VELCADE בשילוב עם דקסמתזון ותלידומיד. נקודות קצה של יעילות משנית כללו הישרדות ללא התקדמות והישרדות כוללת. תוצאות היעילות העיקריות מוצגות בטבלה 13.
טבלה 13: תוצאות יעילות ממחקר MMY-3010
יעילות קלינית בחולים עם מיאלומה נפוצה חוזרת או עקשן
פרופילי הבטיחות והיעילות של VELCADE (מוזרק תוך ורידי) הוערכו בשני מחקרים במינון המומלץ של 1.3 מ"ג / מ"ר: מחקר שלב 3 (APEX) אקראי מבוקר של דקסמתזון שנערך ב -669 חולים עם מיאלומה נפוצה חוזרת ונשנית. , שעברו 1 עד 3 קווי טיפול קודמים ומחקר שלב II בזרוע אחת, שנערך ב -202 חולים עם מיאלומה נפוצה חזרה ושקופה, שעברו לפחות שני קווי טיפול קודמים עם התקדמות המחלה לאחר הטיפול האחרון.
במחקר שלב III, בכל החולים, כולל אלה שקיבלו קו טיפול אחד בלבד, הטיפול ב- VELCADE הביא להארכת זמן משמעותית להתקדמות, להארכה משמעותית של הישרדות ועלייה משמעותית בשיעור התגובה. בהשוואה לטיפול בדקסמתזון (ראה טבלה 14).
בהתבסס על הנתונים העולים מתוך "ניתוח ביניים וועדת המעקב, שתוכננה מראש, המליצה על הפסקת טיפול בדקסמטזון לטובת טיפול ב- VELCADE לכל החולים שאקראו לטיפול בדקסמתזון, ללא קשר למצב המחלה. בשל הצלבה מוקדמת זו, משך החציון של מעקב אחר מטופל חי היה 8.3 חודשים. בזרוע הטיפול ב- VELCADE, ההישרדות הכוללת הייתה ארוכה יותר ושיעור התגובה היה גבוה יותר הן בחולים שהיו עקשנים מהטיפול האחרון שלהם והן באלו שלא.
מתוך 669 החולים שנרשמו, 245 (37%) היו בני 65 ומעלה. פרמטרי התגובה כמו גם ה- TTP היו טובים יותר באופן משמעותי עבור VELCADE ללא קשר לגיל. כל פרמטרי היעילות (זמן להתקדמות, הישרדות כוללת ושיעור תגובה) שופרו באופן משמעותי בזרוע VELCADE, ללא קשר לרמות. של b2-microglobulin בתחילת המחקר.
באוכלוסיית עקשן של מחקר שלב II, התגובות הוערכו על ידי ועדה בלתי תלויה וקריטריוני התגובה שהוחלו הן אלה שנקבעו. על ידי קבוצת השתלות מח עצם האירופאי. ההישרדות הכוללת הממוצעת של כל החולים שנרשמו למחקר הייתה 17 חודשים (טווח סטטוס ביצועים, ממעמד המחיקה של כרומוזום 13, או ממספר או סוג הטיפולים הקודמים. שיעור ההיענות של מטופלים שכבר עברו 2-3 או יותר מ -7 קווי טיפול זה היה 32% (10/32) ו -31% (21/67), בהתאמה.
טבלה 14: סיכום תוצאות היעילות ממחקרי שלב III (APEX) ו- II
במחקר שלב II, מטופלים שלא השיגו תגובה אופטימלית לטיפול יחיד מסוג VELCADE טופלו במינונים גבוהים של דקסמתזון ו VELCADE. הפרוטוקול אפשר למטופלים שהשיגו תגובה פחות אופטימלית לטיפול יחידני ב- VELCADE לקבל דקסמתזון.
בסך הכל 74 מטופלים הניתנים להערכה טופלו ב- dexamethasone ו- VELCADE. הטיפול המשולב אפשר לקבל תגובה או שיפור בתגובה [MR 11% או יחסי ציבור 7%] אצל 18% מהחולים.
יעילות קלינית בחולים עם מיאלומה נפוצה חוזרת ונשנית עם מתן תת עורית של VELCADE
מחקר קליני שלב III אקראי, שאינו נחיתות, פתוח ואקראי, השווה את היעילות והבטיחות של מתן תת-עורי של VELCADE לעומת מתן תוך ורידי. מחקר זה כלל 222 מטופלים עם מיאלומה נפוצה / עקשן, רנדומלית ביחס של 2: 1 לקבלת 1.3 מ"ג / מ"ר של VELCADE תת עורית או תוך ורידית במשך 8 מחזורים. לאותם מטופלים שלא השיגו תגובה אופטימלית ל- VELCADE בלבד (פחות מתגובה מלאה [CR]) לאחר 4 מחזורים, הם הורשו לקבל 20 מ"ג דקסמתזון ביום. של VELCADE ויום שאחרי. חולים עם נוירופתיה פריפריאלית בדרגה בסיסית ≥ 2 או ספירת טסיות
מחקר זה עמד במטרה העיקרית של אי נחיתות הנבדקת על שיעור התגובה (CR + PR) לאחר 4 מחזורים של טיפול יחידני ב- VELCADE הן לדרכי הניהול התת עוריות והן לוריד, עם שיעור תגובה של 42% בשניהם. בנוסף, נקודות קצה של יעילות משנית. הקשור לתגובה וזמן לאירוע הראו תוצאות עקביות הן עבור המסלולים התת עוריים והן תוך ורידי (טבלה 15).
טבלה 15: סיכום ניתוחי יעילות השוואת הממשלים התת עוריים והווריד של VELCADE
טיפול ב- VELCADE בשילוב עם דוקסורוביצין ליפוזומלי מפוגל (מחקר DOXIL-MMY-3001)
מחקר פתוח, אקראי, מקבוצת שלב III, רב-מרכזי, נערך בקרב 646 חולים שהשוו בין הבטיחות והיעילות של VELCADE בתוספת פוקילציה ליפוזומלית של דוקסורוביצין לעומת VELCADE חד-פעמי בחולי מיאלומה נפוצה שקיבלו טיפול אחד לפחות בעבר ולא קיבלו טיפול הראה התקדמות מחלה במהלך הטיפול באנתרציקלין. נקודת הסיום העיקרית של היעילות הייתה הזמן להתקדמות (TTP) ואילו נקודות הסיום של היעילות המשנית היו הישרדות כוללת (OS) ושיעור התגובה הכולל (ORR: (תגובה מלאה + תגובה חלקית) תוך שימוש בקריטריונים של "הקבוצה האירופית לדם ומח השתלה (EBMT).
התוצאות של "ניתוח ביניים פרוטוקול מוגדר (מבוסס על 249 אירועי TTP) הוביל לסיום מוקדם של המחקר לצורך יעילות. ניתוח ביניים זה הראה הפחתה של 45% בסיכון ל- TTP (95% CI; 29-57%, עמ '
הניתוח הסופי להישרדות כוללת (OS) שנעשה לאחר חציון מעקב של 8.6 שנים לא הראה הבדל משמעותי במערכת ההפעלה בין שתי זרועות הטיפול. חציון מערכת ההפעלה היה 30.8 חודשים (95% CI; 25.2-36.5 חודשים) לחולים ב- VELCADE טיפול חד-פעמי ו -33.0 חודשים (95% CI; 28.9-37.1 חודשים) למטופלים המטופלים בטיפול משולב עם VELCADE ו- doxorubicin liposomal pegylated.
טיפול ב- VELCADE בשילוב עם דקסמתזון
בהעדר השוואה ישירה בין VELCADE ל- VELCADE בשילוב עם דקסמתזון בחולים עם מיאלומה נפוצה פרוגרסיבית, בוצע "ניתוח סטטיסטי זוגי" להשוואת תוצאות הזרוע הלא אקראית של VELCADE בשילוב עם דקסמתזון (מחקר שלב II תווית פתוחה MMY-2045), עם תוצאות המתקבלות בזרועות הטיפול VELCADE לטיפול יחידני מניסויים אקראיים שלב III (M34101-039 [APEX] ו- DOXIL MMY-3001) באותה אינדיקציה.
ניתוח התאמה-התאמה היא שיטה סטטיסטית בה מטופלים בקבוצת הטיפול שנחקרה (למשל VELCADE בשילוב עם דקסמתזון) וחולים בקבוצת ההשוואה (למשל VELCADE) ניתנים להשוואה ביחס לגורמים מבלבלים באמצעות זיווג אישי של נבדקי מחקר. שיטה זו ממזערת את ההשפעות של גורמים מבלבלים שנצפו בעת הערכת השפעות הטיפול באמצעות נתונים לא אקראיים.
זוהו 127 זוגות חולים משויכים. הניתוח הראה שיפור בשיעור התגובה הכולל (ORR: CR + PR) (יחס סיכויים 3.769; 95% CI 2.045-6.947; p
קיים מידע מוגבל על טיפול חוזר ב- VELCADE במיאלומה נפוצה חוזרת.
מחקר שלב II MMY-2036 (RETRIEVE), בעל זרוע אחת פתוחה, נערך על מנת לקבוע את היעילות והבטיחות של טיפול חוזר ב- VELCADE. מאה ושלושים חולים (גיל ≥ 18 שנים) עם מיאלומה נפוצה שבעבר היו לה לפחות חלק חלקי אחד תגובה למשטר המכיל VELCADE נסוגה לאחר התקדמות. לפחות 6 חודשים לאחר הטיפול הקודם, VELCADE הוחל במינון האחרון של 1.3 מ"ג / מ"ר (n = 93) או ≤ 1.0 מ"ג / מ"ר (n = 37) וניתן בימים 1, 4, 8 ו -11 כל 3 שבועות למשך עד 8 מחזורים, או כטיפול יחיד או בשילוב עם דקסמתזון בהתאם לתקן הטיפול. Dexamethasone ניתנה בשילוב עם VELCADE ל -83 חולים במחזור 1 ו -11 חולים נוספים קיבלו dexamethasone במהלך מחזורי ההחזרה הבאים של VELCADE.
נקודת הסיום העיקרית הייתה התגובה הטובה ביותר לאישור הטיפול מחדש על פי קריטריוני EBMT. שיעור התגובה הכולל הטוב ביותר (CR + PR) לטיפול חוזר בקרב 130 חולים היה 38.5% (95% CI: 30.1; 47)., 4).
יעילות קלינית בחולים שטרם טופלו עם לימפומה של תאי מעטה (MCL)
LYM-3002 הוא מחקר שלב 3, אקראי, בעל תווית פתוחה, המשווה את היעילות והבטיחות של השילוב של VELCADE, rituximab, cyclophosphamide, doxorubicin ו- prednisone (VcR-CAP; n = 243) לאלה של rituximab. Cyclophosphamide, doxorubicin, וינקריסטין ופרדניזון (R-CHOP; n = 244) בחולים מבוגרים שטרם טופלו ב- MCL (שלב II, III או IV). חולים בזרוע הטיפול ב- VcR-CAP קיבלו VELCADE (1.3 מ"ג / מ"ר; בימים 1, 4, 8, 11, תקופת מנוחה 12-21), ריטוקסימאב 375 מ"ג / מ"ר IV ביום הראשון; ציקלופוספמיד 750 מ"ג / מ"ר IV ביום הראשון; doxorubicin 50 מ"ג / מ"ר IV ביום הראשון ופרדניזון 100 מ"ג / מ"ר דרך הפה בימים 1 עד 5 של מחזור הטיפול ב- VELCADE בן 21 הימים. מטופלים עם תגובה ראשונה מתועדת למחזור 6 קיבלו שני דרכי טיפול נוספות.
נקודת הסיום העיקרית של היעילות הייתה הישרדות ללא התקדמות המבוססת על הערכת ועדת סקירה עצמאית (IRC). נקודות קצה משניות כללו זמן להתקדמות (TTP), זמן לטיפול הבא נגד לימפומה (TNT), משך "מרווח ללא טיפול (TFI) ), שיעור התגובה הכולל (ORR) ושיעור התגובה המלא (CR / CRu), ההישרדות הכוללת (OS) ומשך התגובה.
מאפייני הדמוגרפיה ומאפייני המחלה היו בדרך כלל מאוזנים היטב בין שתי זרועות הטיפול: הגיל החציוני של החולים היה 66 שנים, 74% היו גברים, 66% היו קווקזים ו -32% אסיאתיים, 69% מהחולים. / או ביופסיה של מח עצם חיובי MCL, ל -54% מהחולים היה ציון מדד פרוגנוסטי בינלאומי (IPI) ≥ 3, ו -76% סבלו ממחלה שלב IV. משך הטיפול (חציון = 17 שבועות) ומשך המעקב (חציון = 40 חודשים) היו דומים בשתי זרועות הטיפול. חולים בשתי זרועות הטיפול קיבלו חציון של 6 מחזורים עם 14% מהנבדקים בקבוצת VcR-CAP ו -17% מהחולים בקבוצת R-CHOP שקיבלו את 2 המחזורים הנוספים. רוב החולים בשתי הקבוצות סיימו טיפול, 80% בקבוצת VcR-CAP ו -82% בקבוצת R-CHOP. תוצאות היעילות מוצגות בטבלה 16:
טבלה 16: תוצאות יעילות ממחקר LYM-3002
חציון ה- PFS כפי שנקבע על ידי החוקר היה 30.7 חודשים בקבוצת VcR-CAP ו -16.1 חודשים בקבוצת R-CHOP (יחס סכנה [HR] = 0.51; p
משך החציון של התגובה המלאה היה 42.1 חודשים בקבוצת VcR-CAP לעומת 18 חודשים בקבוצת R-CHOP. משך התגובה הכולל היה ארוך יותר ב- 21.4 חודשים בקבוצת VcR-CAP (חציון של 36.5 חודשים לעומת 15.1 חודשים בקבוצת R-CHOP). במהלך חציון מעקב של 40 חודשים, חציון ההישרדות הכוללת (OS) הייתה לטובת VcR-CAP (56.3 חודשים בקבוצת R-CHOP ולא הושגה בקבוצת VcR-CAP), (אומדן HR = 0.80; p = 0.173). הייתה מגמה של הישרדות כוללת ממושכת לטובת קבוצת VcR-CAP; שיעור ההישרדות המשוער ל -4 שנים היה 53.9% בקבוצת R-CHOP ו -64.4% בקבוצת VcR-CAP.
חולים עם עמילואידוזיס שטופלו בעבר בשרשרת קלה (AL)
נערך מחקר שלב I / II שאינו אקראי, על מנת לקבוע את בטיחות VELCADE בחולים עם עמילואידוזיס שטופלו בעבר בשרשרת קלה (AL). במהלך המחקר לא נצפו בעיות בטיחות חדשות ובמיוחד, VELCADE לא הוביל להחמרה בנזקי האיברים (לב, כליות וכבד).
בניתוח יעילות חקרנית, עבור שתי קבוצות המינון הקשורות, דווח על שיעור תגובה של 67.3% (מתוכן 28.6% תגובה מלאה) במונחים של תגובה המטולוגית (חלבון M), ב -49 מטופלים הניתנים להערכה שטופלו במינונים המרביים ביותר של 1.6 מ"ג / מ"ר פעם בשבוע ו -1.3 מ"ג / מ"ר פעמיים בשבוע. עבור שני קורסי המינון הקשורים, הישרדות לשנה הייתה 88, 1%.
אוכלוסיית ילדים
סוכנות התרופות האירופית ויתרה על החובה למסור את תוצאות המחקרים עם VELCADE בכל קבוצות המשנה של אוכלוסיית הילדים עם מיאלומה נפוצה ותאי מעטפת (ראה מידע על שימוש בילדים בסעיף 4.2).
05.2 "תכונות פרמקוקינטיות -
קְלִיטָה
לאחר מתן בולוס תוך ורידי של 1.0 מ"ג / מ"ר ו -1.3 מ"ג / מ"ר ל -11 מטופלים עם מיאלומה נפוצה וערכי פינוי קריאטינין העולים על 50 מ"ל לדקה, ממוצע ריכוזי הפלזמה המרבי של בורטזומיב במינונים הראשונים היו 57 ו -112 ננוגרם / מ"ל , בהתאמה. במינונים הבאים, ממוצע ריכוזי הפלזמה הנצפים נע בין 67 ל- 106 ng / mL למינון 1.0 מ"ג / מ"ר ובין 89 ל- 120 ng / mL למינון 1.3 מ"ג / מ"ר.
לאחר בולוס תוך ורידי או הזרקה תת עורית של מינון של 1.3 מ"ג / מ"ר בחולים עם מיאלומה נפוצה (n = 14 בקבוצה תוך ורידית, n = 17 בקבוצה התת עורית), חשיפה כוללת לסמים מערכתית (AUClast) הייתה שווה ערך לתת עורית ודרכי מתן תוך ורידי. Cmax לאחר מתן תת עורי (20.4 נ"ג / מ"ל) היה נמוך יותר מהווריד (223 נ"ג / מ"ל). יחס ממוצע גיאומטרי AUC היה 0.99 ועם 90% מרווחי הביטחון הם היו 80.18% - 122.80%.
הפצה
בחולים עם מיאלומה נפוצה, נפח ההפצה הממוצע של בורטזומיב נע בין 1659 ל 3294 ליטר לאחר מינון תוך ורידי חד פעמי או חוזר על 1.0 מ"ג / מ"ר או 1.3 מ"ג / מ"ר. זה מצביע על כך שהבורטזומיב מופץ באופן נרחב ברקמות היקפיות. בטווח ריכוז bortezomib של 0.01 עד 1.0 מיקרוגרם / מ"ל, מחייב לחלבוני פלזמה אנושיים בַּמַבחֵנָה הוא עמד על ממוצע של 82.9%. חלקו הקשור לחלבון הפלזמה של בורטזומיב לא היה תלוי בריכוז.
ביו טרנספורמציה
חינוך בַּמַבחֵנָה על מיקרוזומים של הכבד האנושי ועל איזואנזים של ציטוכרום P450 המתבטאים על ידי c-DNA אנושי מצביעים על כך שהבורטזומיב עובר בעיקר מטבוליזם חמצוני באמצעות אנזימי ציטוכרום P450, 3A4, 2C19 ו- 1A2. המסלול המטבולי העיקרי מורכב מדבורונציה המובילה לשני מטבוליטים deboronated אשר לאחר מכן מועברים הידרוקסילציה למטבוליטים שונים. המטבוליטים הבורונים של בורטזומיב אינם פעילים כמעכבי פרוטוזום 26S.
חיסול
ממוצע מחצית החיים של חיסול (t1 / 2) של בורטזומיב במהלך טיפול במינון מרובה נע בין 40 ל -193 שעות. בורטזומיב מתנקה מהר יותר לאחר המנה הראשונה מאשר במינונים הבאים. ממוצע המרווח הכולל היה 102 ו -112 ליטר / שעות לאחר המנה הראשונה של 1.0 מ"ג / מ"ר ו -1.3 מ"ג / מ"ר, בהתאמה, ובין 15 ל -32 ליטר לשעה ובין 18 ל -32 ליטר לשעה למינונים עוקבים של 1.0 מ"ג / מ"ר ו -1.3 מ"ג / מ"ר, בהתאמה.
אוכלוסיות מיוחדות
אי ספיקת כבד
ההשפעה של אי ספיקת כבד על הפרמקוקינטיקה של בורטזומיב נחקרה במחקר קליני שלב א 'ב -61 חולים עם גידולים מוצקים ראשוניים בדרגות שונות של ליקוי בכבד ומטופלים במינונים של בורטזומיב הכוללים בין 0.5 ל -1.3 מ"ג / מ"ר.
אי ספיקת כבד קלה לא שינתה את ה- AUC מנורמל במינון של בורטזומיב בהשוואה לזה שנראה בחולים עם תפקוד כבד תקין. עם זאת, ערכי AUC ממוצעים מנורמלים עלו במינון של כ- 60% בחולים עם ליקוי בכבד בינוני או חמור. מומלץ להתחיל במינון התחלתי נמוך יותר בחולים עם ליקוי בכבד בינוני או חמור. ויש לפקח על מטופלים כאלה בקפידה (ראה סעיף 4.2, טבלה 6).
אי ספיקת כליות
מחקר פרמקוקינטי נערך בחולים עם דרגות שונות של ליקוי בכליות, אשר סווגו לפי ערכי פינוי קריאטינין (CrCL) לקבוצות הבאות: רגיל (CrCL ≥60 מ"ל / דקה / 1.73 מ"ר, n = 12), קל ( CrCL = 40-59 mL / min / 1.73 m², n = 10), בינוני (CrCL = 20-39 mL / min / 1.73 m², n = 9), וחמור (CrCL תוך ורידי במינונים שנעים בין 0.7 ל- 1.3 מ"ג / מ"ר פעמיים בשבוע. חשיפת VELCADE (מינון מנורמל AUC ו- Cmax) הייתה דומה בכל קבוצות המטופלים (ראה סעיף 4.2).
05.3 נתוני בטיחות פרה -קליניים -
בריכוזים
בורטזומיב לא הראה גנוטוקסיות בבדיקת המוטגניות בַּמַבחֵנָה (בדיקת איימס), וגם לא בבדיקת המיקרו -גרעין in vivo מתבצע בעכברים.
במחקרי רעילות התפתחותית שנערכו בחולדות וארנבות, התמותה העוברית -גופנית הוכחה במינונים רעילים מצד האם, אך לא הייתה רעילות עוברית מתחת למינון הרעיל של האם. לא נערכו מחקרי פוריות, אולם הערכה של רקמות הרבייה בוצעה במחקרי רעילות כלליים. במחקר של שישה חודשים בחולדות נמצאו השפעות ניווניות הן על האשכים והן על השחלות. לכן סביר שלבורטזומיב עשויה להיות השפעה פוטנציאלית על פוריות הגבר והנקבה. מחקרים על התפתחות לידה ואחרית הלידה לא נערכו.
מחקרי רעילות כללית מרובים שנערכו בחולדות ובקופים גילו כי איברי המטרה העיקריים היו: מערכת העיכול, וכתוצאה מכך הקאות ו / או שלשולים; רקמות המטופויטיות ולימפה, וכתוצאה מכך ציטופניה בדם ההיקפי, ניוון רקמת הלימפה והתא -תא תאי של מח העצם; נוירופתיה היקפית (נראית אצל קופים, עכברים וכלבים) המשפיעה על האקסונים של העצבים החושים; ושינויים קלים בכליה. לאחר הפסקת הטיפול, כל איברי המטרה הללו הראו החלמה חלקית עד מלאה.
בהתבסס על מחקרים בבעלי חיים, מעבר הבורטזומיב על מחסום מוח הדם נראה מוגבל והרלוונטיות בבני אדם אינה ידועה.
מחקרים פרמקולוגיים לבטיחות לב וכלי דם שנערכו בקופים וכלבים מראים כי מתן תוך ורידי של מנות מ"ג / מ"ר פי 2 עד המינון המומלץ קלינית מביא לירידה בקצב הלב, ירידה בהתכווצות הלב, תת לחץ דם ומוות. אצל כלבים, ירידה בהתכווצות הלב ובלחץ הדם נשלטו על ידי טיפול חריף בסוכנים אינוטרופיות חיוביות או בכלי הדם ונצפתה עלייה קלה במרווח ה- QT המתוקן.
06.0 מידע פרמצבטי -
06.1 מרכיבים -
מניטול (E421)
חַנקָן
06.2 חוסר התאמה "-
אין לערבב תרופה זו עם מוצרים אחרים למעט אלה המוזכרים בסעיף 6.6.
06.3 תקופת תוקף "-
בקבוקון לא נפתח
3 שנים.
פתרון משוחזר
יש להשתמש בפתרון המחודש מיד לאחר ההכנה.
אם לא נעשה בו שימוש מידי, באחריות המשתמש לציית לתנאים ולזמני האחסון של המוצר לפני השימוש.
עם זאת, היציבות הפיזית והכימית של הפתרון המשוחזר הודגמה במשך 8 שעות בטמפרטורה של 25 מעלות צלזיוס כאשר היא מאוחסנת בבקבוקון המקורי ו / או במזרק. זמן האחסון הכולל של התרופה המשוחזרת לפני הניהול לא יעלה על 8 שעות.
06.4 אמצעי זהירות מיוחדים לאחסון -
יש לאחסן בטמפרטורה שלא תעלה על 30 מעלות צלזיוס.
שמור את הבקבוקון בקרטון החיצוני כדי להגן על התרופה מפני אור.
לתנאי אחסון לאחר שחזור המוצר, ראה סעיף 6.3.
06.5 אופי האריזה המיידית ותכולת האריזה -
בקבוקון 10 מ"ל מזכוכית מסוג I, עם פקק ברומבוטיל אפור ואטם אלומיניום, עם מכסה כחול רויאל מכיל 3.5 מ"ג בורטזומיב.
הבקבוקון נמצא בתוך שלפוחית שקופה המורכבת ממגש עם מכסה.
כל אריזה מכילה בקבוקון אחד לשימוש חד פעמי.
06.6 הוראות שימוש וטיפול -
אמצעי זהירות כלליים
בורטזומיב הוא חומר ציטוטוקסי. לכן, יש להקפיד במיוחד על טיפול והכנת VELCADE. מומלץ ללבוש כפפות ובגדי מגן אחרים למניעת מגע עם העור.
הטיפול ב- VELCADE חייב להיעשות תוך הקפדה על טכניקות אספטיות בשל היעדר חומרים משמרים.
היו מקרים של מוות לאחר מתן אינטראקלי תוך -כווני של VELCADE. אבקת VELCADE 1 מ"ג לתמיסה להזרקה מיועדת לשימוש תוך ורידי בלבד, ואילו אבקת VELCADE 3.5 מ"ג לתמיסה להזרקה מיועדת לשימוש תוך ורידי או תת עורי. אין לתת VELCADE תוך -עורית.
הוראות הכנה מחדש
VELCADE חייב להיערך מחדש על ידי רופא מומחה.
זריקה תוך ורידית
כל בקבוקון של 10 מ"ל המכיל אבקת VELCADE 3.5 לתמיסה להזרקה חייב להיות מורכב מחדש עם 3.5 מ"ל של תמיסת נתרן כלוריד 9 מ"ג / מ"ל (0.9%) להזרקה. פירוק האבקה הנוגלית לוקח פחות משתי דקות. לאחר הכינון מחדש, כל מיליליטר של תמיסה מכיל 1 מ"ג בורטזומיב. התמיסה המחודשת היא צלולה וחסרת צבע, עם pH סופי בין 4 ל 7. יש לבדוק את התמיסה המחודשת לפני הניהול כדי לבדוק אם יש חלקיקים או שינוי צבע. בנוכחות חלקיקים או שינוי בצבע. אין להשתמש בתמיסה ויש להשליך אותה.
זריקה תת עורית
כל בקבוקון של 10 מ"ל המכיל אבקת VELCADE 3.5 לתמיסה להזרקה חייב להיות מורכב מחדש עם 1.4 מ"ל של נתרן כלורי 9 מ"ג / מ"ל (0.9%) תמיסה להזרקה. פירוק האבקה הנוגלית לוקח פחות משתי דקות. לאחר הכינון מחדש, כל מיליליטר של תמיסה מכיל 2.5 מ"ג בורטזומיב. התמיסה המחודשת היא צלולה וחסרת צבע, עם pH סופי בין 4 ל 7. יש לבדוק את התמיסה המחודשת לפני הניהול כדי לבדוק אם יש חלקיקים או שינוי צבע. בנוכחות חלקיקים או שינוי בצבע. אין להשתמש בתמיסה ויש להשליך אותה.
רְשׁוּת
VELCADE מיועד לשימוש חד פעמי בלבד.
יש להשליך תרופות שאינן בשימוש ופסולת מתרופה זו בהתאם לתקנות המקומיות.
07.0 מחזיק "רשות השיווק" -
JANSSEN-CILAG INTERNATIONAL N.V.
Turnhoutseweg, 30
B-2340 בארס
בלגיה
08.0 מספר אישור השיווק -
האיחוד האירופי/1/04/274/001
036559019
09.0 תאריך האישור הראשון או חידוש האישור -
תאריך האישור הראשון: 26 באפריל 2004
תאריך החידוש האחרון של ההרשאה: 26 באפריל 2014
10.0 תאריך עדכון הטקסט -
04/2015